Les composés organiques oxygénés et la synthèse des molécules

Chapitre 17. Cours 1re S
Les composés organiques oxygénés
et la synthèse des molécules et de nouveaux matériaux.
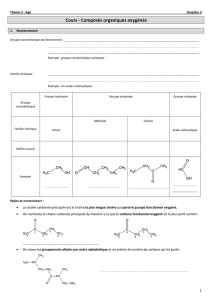
I. Quelques familles de composés organiques oxygénés.
1. Les alcools. (voir chapitre 13)
On distingue trois classes d'alcools :
- les alcools primaires (où le C portant le OH est lié à 2 H). Ex : le butan-1-ol
CH3CH2CH2CH2OH
;
- les alcools secondaires (où le C portant le OH n'est lié qu'à 1 H). Ex : le butan-2-ol
CH3CH CH2CH3
OH
;
- les alcools tertiaires (où le C portant le OH est lié à aucun H). Ex : le 2-méthylbutan-2-ol
CH3C CH2CH3
OH
CH3
.
2. Les acides carboxyliques.
Ils sont caractérisés par le groupe
C
O
OH
soit –COOH soit encore –CO2H .
Nomenclature : à partir du nom de l'alcane, le
e
final est remplacé par le suffixe
oïque
et l'ensemble est précédé
de
acide
.
Exemples :
H C
O
OH
est l'acide méthanoïque (ou acide formique).
CH3C
O
OH
(ou CH3-COOH ) est l'acide
éthanoïque (ou acide acétique, l'acide du vinaigre).
Les acides carboxyliques sont des espèces chimiques acides : lorsqu'ils sont dans l'eau pHsolution < 7 .
Aide à l'identification : utilisation de papier pH ou d'un indicateur coloré acido-basique.
3. Les aldéhydes.
Ils sont caractérisés par le groupe
C
O
H
soit –CH=O soit encore –CHO .
Nomenclature : à partir du nom de l'alcane, le
e
final est remplacé par le suffixe
al
.
Exemples : CH3-CH=O (ou CH3-CHO ) est l'éthanal, CH3-CH2-CH=O (ou CH3-CH2-CHO ) est le propanal.
4. Les cétones.
Ils sont caractérisés par le groupe
C
O
où C n'est lié à aucun H ou plutôt
C C C
O
.
Nomenclature : à partir du nom de l'alcane, le
e
final est remplacé par le suffixe
one
.
Exemple :
CH3C CH3
O
est la propanone (ou acétone).

Chapitre 17. Cours 1re S
II. Oxydations.
1. Oxydation brutale.
L'oxydation brutale d'une espèce chimique organique se fait avec rupture complète de la chaîne carbonée.
Exemple de l'oxydation brutale (combustion complète) de l'éthanol en présence de dioxygène :
CH3-CH2-OH + 3 O2 → 2 CO2 + 3 H2O .
2. Oxydation ménagée.
L'oxydation ménagée est une oxydation sans rupture de la chaîne carbonée.
On utilise des oxydants relativement forts tels que les ions permanganates MnO4- en milieu acide (solution
aqueuse acidifiée de permanganate de potassium).
a) L'oxydation ménagée de l'aldéhyde
R C
O
H
donne l'acide carboxylique
R C
O
OH
(couple redox acide
carboxylique/aldéhyde).
b) L'oxydation ménagée de la cétone
R
CR'
O
ne peut pas se faire ; les cétones ne sont pas oxydables (par
oxydation ménagée).
c) L'oxydation ménagée de l'alcool primaire
CH2OHR
donne l'aldéhyde
R C
O
H
(couple redox
aldéhyde/alcool I),
lui-même rapidement oxydé en acide carboxylique
R C
O
OH
(couple redox acide carboxylique/aldéhyde).
Bilan : on a le couple redox acide carboxylique/alcool I.
d) L'oxydation ménagée de l'alcool secondaire
R CH R'
OH
donne la cétone
R
CR'
O
(couple redox
cétone/alcool II).
e) L'oxydation ménagée de l'alcool tertiaire
R C R'
OH
R''
ne peut pas se faire ; les alcools III ne sont pas
oxydables (par oxydation ménagée).
1
/
2
100%