Le système nerveux - aup1perdu.nancy

http://aup1perdu.nancy.free.fr/ par TiV et Billou Cours du Pr. Leheup 1
Histologie
Le système nerveux
Introduction
Le système nerveux est divisé en 2 parties principales :
Système nerveux central : comprenant le cerveau et la moelle épinière
Système nerveux périphérique : nerfs qui relient le cerveau aux autres tissus, et des relais
nerveux appelés ganglions.
Le tissu nerveux comprend essentiellement 4 catégories cellulaires : les neurones, les cellules
de la névroglie, les macrophages et les cellules souches neurales.
Les neurones ne composent que 10% des cellules du système nerveux. Néanmoins, leur rôle
est essentiel puisqu’ils sont le support de l’activité cérébrale et de la pensée. On considère
donc que les neurones sont les unités fondamentales du système nerveux.
Le neurone est une cellule noble, excitable, qui transmet le PA (voir cours de physiologie)
Il élabore, modifie, transmet l’influx nerveux.
Certains neurones : activité élastique rythmique
Modification par synapses activatrices ou inhibitrices.)
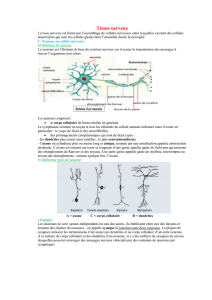
Un neurone est divisé en plusieurs régions ayant chacune une fonction propre.
Généralement, il se compose d’un péricaryon (peri= autour, karuon= noyau) et
d’expansions (neurites): un axone et des dendrites, l’axone transmettant l’influx nerveux vers
sa partie terminale, partie appelée bouton synaptique, qui entre en contact avec une autre
cellule → Jonctions synaptiques. Les dendrites sont en contact avec les boutons synaptiques
d’autres neurones.
Un neurone est une cellule mononucléée.
Mise en évidence par :
- imprégnation argentique (pH alcalin)
- bleu de méthylène
- bleu d’aniline
Mr Golgi : cartographie de l’organisation neuronale, par la technique d’imprégnation
argentique (avec prétraitement au bichromate de potassium)
Plusieurs types de neurones ont été décrits à partir de caractéristiques anatomiques: la forme,
la grandeur des neurones, la forme des embranchements, etc. Aujourd’hui, les neurones sont
décrits aussi en fonction de leur position dans le circuit neuronal, de leur patron d’activité et
des gènes qu’ils expriment.

http://aup1perdu.nancy.free.fr/ par TiV et Billou Cours du Pr. Leheup 2
Corps cellulaire de taille variable :
Grande taille
- c pyramidale
Petite taille
- c mitre
- c granulaire
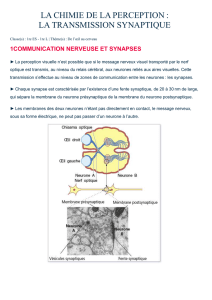
Forme du neurone avec ses expansions : variable :
- c unipolaire
Expansions identiques. Dentrites + axone.
Rare chez vertébrés supérieurs
- c bipolaire
Pôle dendritique – pôle axonal
- c pseudo unipolaire
Un seul tronc commun
- c multipolaire
Ramification dendritiques primaires, puis secondaires, puis tertiaires.
On trouve des neurones
- fusiformes
- planaires (cellules de Purkinje, en espalier) avec une branche qui part de l’axone et
qui remonte vers le corps cellulaire.
- en corbeille (« basket ») (dans le cervelet par exemple)
- multipolaire an-axonal : avec uniquement des dendrites (c amacrine de la rétine)
Classification des neurones basée sur la longueur (par Mr Golgi) :
- I : axone long → neurone de projection
Volume neuronal surtout dendritique ou axonal
- II : axone court → interneurone (= neurone d’association)
A- Le péricaryon
Taille :
Les plus petites cellules se trouvent dans l’hypothalamus : 4µm
Elles forment un noyau parvocellulaire
Les plus grosses se trouvent dans le cortex moteur : 120 à 150µm
Organisation :
Les neurones ont un aspect cytologique caractéristique, reflétant une activité métabolique
importante. Ils ont un métabolisme très actif car non seulement ils entretiennent une surface
étendue de membrane plasmique, mais ils ont constamment besoin d’énergie pour maintenir
des gradients électrochimiques
Noyau :
→ peu d’Hétérochromatine car très faible nombre de gènes non exprimés.
Cytoplasme :

http://aup1perdu.nancy.free.fr/ par TiV et Billou Cours du Pr. Leheup 3
Beaucoup de ribosomes
Corps de Nissl (Ce sont des amas de citernes de réticulum endoplasmique granulaire
entre lesquels se trouvent de nombreux ribosomes libres). En MO (au bleu d’aniline) : occupe
l’ensemble du cytoplasme sauf au niveau du cône d’émergence axonique.
Si souffrance cellulaire → chromatolyse → reflet de la désorganisation, défaut de synthèse
ARN → nécrose.
Appareil de golgi : périnucléaire – continuité avec le RE par des vésicules
Mitochondries : dans tout le cytoplasme
Cytosquelette : organisation neurofibrillaire mise en évidence par imprégnation
argentique.
Si on utilise le ME : → neurofilament (grande affinité pour les sels d’argent)
→ neurotubule (associé aux MAP (2), TAU (TAU est
impliquée dans la dégénérescence neuronale : Alzheimer))
Lysosomes
Pigments :
Mélanine
Lipofuscine : augmente avec l’âge. Résidu lysosomal
Neurosecrétions (comme au niveau de l’hypothalamus)
Neuromédiateurs
Centriole : 1 ou 2 complexes
Cil primitif : relief polarisant la cellule.
B- Dendrite
… prolongement du soma sans nette démarcation
Contient :
Corps de Nissl
Ribosomes libres (dont le nombre diminue jusqu’au bout)
Mitochondries (sauf à l’extrémité distale)
Cytosquelette : µfilamentaire, µtubulaire
→ Transport dendritique 3mm/H, inhibé par la Colchicine
Les dendrites, avec le corps cellulaire, reçoivent et intègrent les informations reçues
provenant d’autres neurones. La forme de l’arborisation des dendrites détermine grandement
la sensibilité et le champ-récepteur du neurone.
Sur les dendrites, des expansions cytoplasmiques en forme de bourgeon, nommées
épines dendritiques, permettent la connexion par synapses avec le neurone pré-synaptique.
Chaque épine dendritique établit une synapse. Un neurone typique a plusieurs dizaines de
milliers d’épines dendritiques formant des synapses. L’activation de ces récepteurs sur ces
épines génère un courant électrique dans l’épine et la dendrite qui stimule ou inhibe le
neurone.
Ces épines ont un aspect pédonculé : tige avec une expansion distale.
- la tige : 0,5 à 1µm de longueur, contient des microtubules.
- L’expansion distale : 2 µm de diamètre, cytoplasme amorphe. Différenciation de la
région membranaire avec épaississement membranaire.
On peut observer des régressions anormales de l’épine dendritique dans des retards mentaux
(avec mutation de protéines associées au cytosquelette)

http://aup1perdu.nancy.free.fr/ par TiV et Billou Cours du Pr. Leheup 4
C- L’axone.
Elément UNIQUE.
L’axone est un long prolongement du corps cellulaire qui relie ce dernier aux
synapses. La longueur de l’axone est très variable: quelques dizaines de microns, pour un
neurone qui se projette sur son voisin, plusieurs décimètres s’il transporte une information du
cerveau à la moelle épinière ou d’une partie du corps à la moelle épinière. Il peut même
atteindre un mètre. Les neurones ayant le plus long axone sont, bien entendu, ceux partant des
pieds et allant jusqu’à la moelle épinière. Le diamètre de l’axone est généralement stable sur
toute sa longueur, entre 5 à 10 microns.
L’axone est divisible en 3 parties.
- Cône d’émergence (= cône d’implantation)
Pauvre en REG (… donc pas de corps de Nissl) et en REL
Regroupement des microtubules en faisceaux.
Condensation sous membraneuse commence à s’organiser
- Segment initial (ou intermédiaire) pour un axone myélinisé :
C’est la zone se situant entre le cône d’émergence et la zone de début de myélinisation.
Absence de ribosome et REG.
Condensation sous membranaire a un aspect granulaire.
Les microtubules sont organisés en faisceaux. On y trouve des protéines ancrées qui
les lient. Ces liaisons se font perpendiculairement par rapport au grand axe du segment.
Mitochondries : partout.
C’est la zone qui génère le PA : Seuil bas d’excitabilité.
Il se trouve surtout au niveau du SNC. Il est absent sur les axones sensitifs, idem dans les
ganglions rachidiens.
- Prolongement axonal
Il est enveloppé par les expansions des cellules gliales.
Il ne contient que peu d’organites, quelques mitochondries, des lysosomes. Il contient du
REL ! Ce REL participe au transit des précurseurs des vésicules synaptiques.
On y trouve 2 transports axonal : flux antérograde (orthograde) et flux rétrograde.
Le flux antérograde :
- flux rapide : 400/500mm/j.
Celui-ci permet un flux de protéines, ou d’organites (vésicules dérivés du REL), le long des
microtubules par les Kinésines → transport ATP dpdt.
- flux lent : 0,2 à 8 mm/j.
Il participe soit au renouvellement du cytoplasme et de la membrane plasmique de l’axone
soit à l’élongation des axones observée au cours de la croissance nerveuse ou des processus de
régénération axonale. → Rôle dans la STRUCTURE.
Ce phénomène de restructuration est bien connu au niveau du SNP : si section accidentelle, ça
permet la régénération de l’extrémité. (Les cellules gliales elles, qui entouraient le bout de
l’axone qui aurait dégénéré, ne dégénère pas.)
Le flux rétrograde :
Un seul flux → rapide : 100 à 300 mm/j. Par des Dynéines.

http://aup1perdu.nancy.free.fr/ par TiV et Billou Cours du Pr. Leheup 5
Ce flux permet le transport vers le soma de deux types de structures. On s’intéresse ici
particulièrement aux corps plurivésiculaires.
Ces corps transportent des molécules membranaires qui seront dégradées par les enzymes
lysosomales, ou qui exerceront un effet biologique au niveau du corps cellulaire. C’est le cas
par exemple de molécules indispensables à la survie neuronale, ainsi qu'à la pousse axonale
au cours du développement : les neurotrophines. Les neurotrophines sont essentiellement
synthétisées par les cellules de la névroglie et en particulier par les astrocytes et les cellules de
Schwann. Elles sont captées par des récepteurs membranaires spécifiques exprimés au niveau
de la membrane axonale et c’est l’ensemble neurotrophine couplée à son récepteur qui est
transportée par voie rétrograde jusqu’au corps cellulaire neuronal. Par exemple, on connaît
une neurotrophine appelée FGF.
Outre les neurotrophines, de nombreuses molécules captées dans le milieu extracellulaire par
les terminaisons axonales sont également transportées jusqu'au corps cellulaire. Ces
molécules permettent d'informer le neurone sur le milieu extracellulaire. Dans certains cas,
des molécules toxiques sont captées et transportées jusqu'au corps cellulaire. Ce mécanisme
pourrait être en cause dans certaines pathologies neurodégénératives. Par ailleurs, des agents
infectieux sont également capables de se disséminer par voie axonale rétrograde. C'est le cas
en particulier du virus de la rage (→ virux neurotrope). Ce virus remonte vers la Moelle, puis
vers l’encéphale.
Les facteurs neurotropes sont indispensables, sinon les cellules cibles dégénèrent.
D- Synapse
La synapse est le lieu de connexion entre, par exemple, 2 neurones. Il s’agit d’un exemple, car
elle existe entre d’autres types de cellules.
1) Types
Elle est interneuronale, ou neuromusculaire, ou autonome (entre un neurone et une cellule
musculaire lisse). Elle peut encore être neuro-glandulaire, ou encore neuro-vasculaire.
2) Ultrastructure
Elément pré-synaptique : bouton synaptique.
Il contient les vésicules synaptiques. Elles renferment un neurotransmetteur et des protéines
spécifiques nécessaires au fonctionnement des synapses. Parmi ces protéines, citons la
chromogranine, protéine impliquée dans l’ « emballage » des neurotransmetteurs, et la
synaptophysine qui est une glycoprotéine de la membrane vésiculaire.
On y trouve également des mitochondries, du cytosquelette.
Les vésicules synaptiques :
Petites vésicules :
• 50nm
• Centre clair, cœur dense
• Protéine spécifique : Synaptophysine (et pas de chromogranine, attention …)
Grandes vésicules :
• 70nm
• Cœur dense.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
1
/
12
100%