Lire l'article complet

La Lettre du Neurologue - n° 1 - vol. IV - février 2000 29
MISE AU POINT
e syndrome du retard mental avec X-fragile est la
cause la plus fréquente de retard mental héréditaire,
avec une incidence estimée à environ 1/4 000 chez
les hommes, mais est également responsable de retard mental
léger à modéré chez environ une femme sur 7 000. Il représente
près de 15 % des retards mentaux liés au chromosome X (1). Il
est encore sous-diagnostiqué, en raison de la méconnaissance
du syndrome, résultant en particulier de la variabilité de ses
formes cliniques.
Bien que la première famille fût décrite en 1943 par Martin et
Bell, que la mise en évidence d’un marqueur cytogénétique sur
le chromosome X date de 1969 et que la mise au point de tech-
niques de culture nécessaires à l’expression du marqueur ait été
réalisée dès 1977, il faut se rappeler que ce syndrome n’a été
réellement reconnu qu’à partir de 1982.
SYMPTOMATOLOGIE
La maladie se manifeste initialement, chez les garçons, par un
retard de langage et des anomalies de comportement (hyper-
activité, troubles de l’attention, impulsivité, comportement de
type autistique). Dans la forme typique, le visage est long et
étroit avec de larges oreilles décollées et mal ourlées, et un pro-
gnathisme du maxillaire inférieur. Le front est large, quadrangu-
laire, et il existe une relative macrocéphalie. Les lèvres sont
épaisses et éversées. Chez l’adulte, on observe dans 70 à 75 %
des cas une macro-orchidie, parfois une macrogénitostomie
avec hyperpigmentation du scrotum. Certains signes inconstants
ont été décrits : palais ogival (52 %), strabisme (36 %), myopie
(22 %), scoliose, thorax creux, pieds plats (71 %), hyperlaxité
des articulations métacarpophalangiennes (67 %), hyperlaxité
du pouce (53 %), callosités du dos de la main (29 %), pli pal-
maire unique (25 %), convulsions (22 %), tics moteurs (19 %),
clic cardiaque (18 %) (2). Ces signes évocateurs ne sont toute-
fois ni suffisamment spécifiques, ni suffisamment constants
pour établir ou réfuter le diagnostic. Ainsi, dans certains cas, le
retard mental est le seul symptôme d’appel (QI = 35-55 chez
l’enfant et QI = 20-40 chez l’adulte en moyenne). Par ailleurs,
la caractérisation du gène a permis de regrouper sous une même
entité génétique des phénotypes aussi hétérogènes que le clas-
sique syndrome de Martin-Bell, l’autisme infantile et le mor-
photype “pseudo-Prader-Willi”.
Chez les femmes, l’expression clinique est très variable. Un
tiers des femmes présentant l’allèle muté sont cliniquement nor-
males et deux tiers souffrent d’un retard mental léger à modéré
(QI < 85), accompagné de troubles du comportement et de la
relation. Les symptômes sont peu typiques : visage long, pro-
gnathisme du maxillaire inférieur et front haut. Récemment, il a
été suggéré que les femmes présentant un allèle prémuté ont un
risque majeur de survenue d’une ménopause précoce (< 40 ans).
DIAGNOSTIC CRYTOGÉNÉTIQUE
C’est en 1969 que Lubs repère un chromosome marqueur chez
quatre hommes retardés mentaux appartenant à trois généra-
tions d’une même famille. Ce marqueur apparaît sous forme
d’une petite cassure à l’extrémité distale du chromosome X.
Trois femmes hétérozygotes pour cette anomalie, exemptes de
troubles psychiques, ont été considérées alors comme des vec-
trices saines. Toutefois, ce n’est qu’à partir de 1977 que l’im-
portance de cette observation a été reconnue, grâce à la mise au
Le syndrome de l’X-fragile
● T. Bienvenu*, C. Beldjord*
L
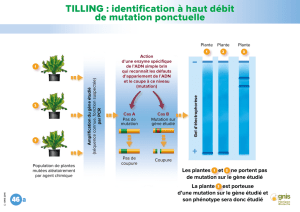
■ Premier exemple de transmission génétique ne répon-
dant pas aux lois de Mendel.
■Grande hétérogénéité clinique.
■Amplification de triplets CGG dans la région 5’transcrite
non codante du gène FMR1.
■Au-delà de 200 triplets CGG, apparition d’une méthyla-
tion de l’îlot CpG en amont du gène FMR1 et inactivation
du gène FMR1.
■Depuis 1991, fiabilité (proche de 100 %) du diagnostic
moléculaire du syndrome de l’X-fragile.
■Fonction de la protéine FMRP encore inconnue avec cer-
titude, bien qu’elle se fixe sur les transcrits et assure le
transport de ceux-ci vers la machinerie traductionnelle.
POINTS FORTS
POINTS FORTS
* Laboratoire de biochimie et génétique moléculaire, hôpital Cochin, Paris.

MISE AU
POINT
La Lettre du Neurologue - n° 1 - vol. IV - février 2000
30
point par Sutherland (1977) d’un test cytogénétique mettant en
évidence de manière fiable le site fragile (dénommé
FRAXAq27*RFA ; R = rare et FA = acide folique) à l’extrémi-
té distale du bras long du chromosome X en Xq27.3 (3). Ce der-
nier n’est détecté que dans des conditions particulières d’analyse
du caryotype (culture en milieu pauvre en acide folique et en
thymidine, ou culture en présence de méthotrexate ou de fluoro-
désoxyuridine). Chez les garçons atteints, ces cassures sont
constantes, mais leur fréquence varie de 5 à 50 % des mitoses
examinées. Chez les filles atteintes cliniquement, il est habituel
de trouver une moindre fréquence de cassures. Chez certaines,
il est même impossible de les mettre en évidence. Ainsi, la
détection de ce site fragile, par l’analyse de 50 à 100 cellules
chez les hommes et de 75 à 150 cellules chez les femmes, per-
mettait le diagnostic cytogénétique du syndrome avec une assez
bonne fiabilité chez les patients présentant un retard mental
(bien que certains faux négatifs aient été identifiés) mais ne per-
mettait d’identifier que moins de 50 % des femmes conductrices
obligatoires et, de plus, était très difficilement utilisable avec
sécurité en diagnostic prénatal. Les premières possibilités de
diagnostic prénatal, bien qu’imparfaites, ont été proposées en
1984 aux couples présentant un risque de un sur deux. À cette
époque, l’analyse cytogénétique conduisait à respecter toutes
les grossesses de fœtus de sexe féminin (faute de pouvoir dis-
cerner les déficiences mentales potentielles) et à proposer une
interruption médicale de grossesse pour tous les résultats posi-
tifs obtenus chez les fœtus de sexe masculin quel que soit le
pourcentage de mitoses FRAXA identifiées. De plus, l’existence
d’autres sites fragiles X dans la région distale du bras long du
chromosome X (FRAXD, FRAXE, FRAXF), cytogénétique-
ment difficiles à distinguer de FRAXA en absence des outils de
biologie moléculaire (FISH), pouvait compliquer l’interpréta-
tion de l’examen cytogénétique (figure 1) et rendre le conseil
génétique particulièrement ardu. L’intérêt de l’analyse du
caryotype réside aujourd’hui dans la détection d’autres rema-
niements chromosomiques, dont la prévalence est estimée à
environ 3 % des retards mentaux.
DIAGNOSTIC MOLÉCULAIRE DIRECT
L’identification, en 1991, du gène en cause (FMR1) a révélé un
mécanisme mutationnel original qui a permis de mieux com-
prendre les caractéristiques de la transmission de ce syndrome
et de développer des méthodes fiables de diagnostic de l’affec-
tion (4). En effet, ce syndrome du retard mental avec X-fragile
présente un mode atypique de transmission dominant lié à l’X
avec pénétrance incomplète, puisqu’on retrouve toujours un
risque accru de développer la maladie au cours des générations
successives dans une même famille (paradoxe de Sherman,
décrit en 1985).
Les mutations sont essentiellement des expansions instables
d’une répétition du trinucléotide CGG, localisé dans le premier
exon du gène FMR1, qui en comporte 17 étendus sur 38 kb
(tableau I). Dans la population normale, cette répétition, située
69 nucléotides en amont du codon AUG initiateur de la traduc-
tion, est polymorphe, avec un nombre de CGG variant de 6 à
54 et une valeur moyenne de 30. Chez les patients avec retard
mental, hommes ou femmes, les mutations dites “complètes”
(full mutation pour les Anglo-Saxons) correspondent à de
larges amplifications de ce triplet (200 à plus de 1 000 CGG)
générant, dans ce cas, une hyperméthylation des séquences
d’ADN avoisinantes, dont la conséquence est l’arrêt d’expres-
sion du gène FMR1. Chez la majorité des femmes conduc-
trices, mais aussi chez des hommes sans retard mental, dits
“hommes normaux transmetteurs”, sont retrouvées des expan-
sions plus modérées de la région (52 à 193 CGG environ) sans
méthylation, dénommées “prémutations”. À l’heure actuelle,
on n’a jamais pu observer le passage d’un allèle normal à un
allèle prémuté.
Tableau I. Effet des amplifications du triplet CGG dans le gène FMR1
(M = hommes ; F = femmes).
Nombre de triplets Protéine FMRP Retard mental
Normal (CGG) n = 6-54 Normale -
Prémutation (CGG) n = 52-93 Normale -
Mutation (CGG) n > 200 Absente/ 100 % M
complète Réduite > 50 % F
Figure 1. Localisation des quatre sites fragiles situés à l'extrémité distale
du chromosome X. Le site fragile FRAXD en Xq27 et les deux sites fra-
giles FRAXE et FRAXF localisés en Xq28 sont cytogénétiquement diffi-
ciles à distinguer du site FRAXA.
q26
q27
q28
CHR.X
DXS98
DXS477
DXS308
DXS296
FRAXD
FRAXA
FRAXE
FRAXF

La Lettre du Neurologue - n° 1 - vol. IV - février 2000 31
La transition de prémutation à mutation complète ne sur-
vient qu’après passage obligatoire d’une méiose féminine,
avec un risque qui dépend de la taille de la prémutation.
Ainsi, une femme avec une prémutation de 60 CGG a un
risque faible d’avoir des enfants atteints, alors que ce risque
devient très important pour des prémutations de 90 CGG ou
plus (tableau II) (5). La prédiction de l’instabilité de la
répétition pour des valeurs de 45 à 55 CGG (“grey zone”)
sera fonction du nombre d’interruptions par des triplets
AGG (en moyenne tous les 10 CGG), la répétition n’étant
pas parfaite. Un homme porteur d’une prémutation la trans-
mettra à toutes ses filles qui seront alors conductrices obli-
gatoires, le risque d’avoir des enfants atteints survenant à la
génération suivante.
Le diagnostic le plus fiable du statut génétique d’un individu
repose aujourd’hui sur les méthodes de biologie moléculaire. La
méthode considérée comme la plus fiable reste à ce jour l’ana-
lyse par la technique de Southern blot. Cette technique permet
en général :
– de mettre en évidence le fragment d’ADN renfermant la suc-
cession de triplets CGG ;
– d’estimer le degré de méthylation de l’îlot CpG en amont du
gène FMR1 chez les sujets atteints.
En pratique, l’ADN, extrait généralement à partir des cellules
nuclées du sang, est digéré par les enzymes de restriction EcoRI
et EagI. Cette stratégie permet de distinguer les grandes prému-
tations sans méthylation des petites mutations complètes avec
méthylation. Les fragments d’ADN sont alors séparés par élec-
trophorèse sur un gel d’agarose à 0,8 %, transférés sur une
membrane et hybridés avec la sonde StB12, fournie par l’équi-
pe de J.L. Mandel (Strasbourg). Le marquage de la sonde peut
être radioactif ou non radioactif (chimioluminescence).
L’enzyme de restriction EcoRI délimite un fragment génomique
de 5,2 kb, et l’enzyme de restriction EagI explore l’état de
méthylation de l’îlot CpG localisé dans ce fragment en amont
du gène FMR1. Une méthylation de cet îlot CpG inhibe la cou-
pure par l’enzyme EagI du fragment de 5,2 kb en deux frag-
ments, dont l’un a une taille de 2,8 kb (figure 2).
Dans ces conditions, les résultats observés sont chez les
hommes :
– un fragment unique de 2,8 kb (“X actif” non méthylé) chez un
homme normal ;
– un fragment unique de 3-4 kb (prémutation sur le “X actif”
Tableau II. Risque de transition de prémutation à mutation complète
en fonction de la taille de la prémutation maternelle (d'après [5]).
Taille de la prémutation Risque de transition
(en nombre de CGG) (estimation en %)
50-60 2-5
60-70 5-25
70-80 20-55
80-90 55-90
90-100 90-100
>100 100
Figure 2. a) Carte de restriction de la région avoisinante du gène FMR1. b) Diagnostic moléculaire du syndrome X-fragile par Southern blot par double
digestion de l'ADN génomique par EcoRI et EagI et hybridation avec la sonde StB12.3. Une mutation complète se traduit par une traînée (“smear”)
constituée de fragments génomiques de poids moléculaire élevé supérieur à 6 kb.
Centromère Télomère
Bgl II Eagl HindIII EcoRI EcoRI HindIII EcoRI HindIII Bgl II
Nrul SacII Xhol BamHI PstI HindIII
EcoRI PstI Eagl Pstl HindIII EcoRI
1 kb
pfxa1 / pE5.1
pfxa2
pfxa3 / Ox0.55
StB12.3 / pfxa7
Ox1.9
ccGn
ab

MISE AU POINT
La Lettre du Neurologue - n° 1 - vol. IV - février 2000
32
non méthylé) chez “homme normal transmetteur” sans expres-
sion clinique ;
– des fragments instables oscillant entre 6 et 10 kb s’accompa-
gnant de méthylation chez un homme atteint d’un retard mental.
Chez les femmes, la situation est un peu plus complexe, puis-
qu’elle fait intervenir le second chromosome X. C’est pourquoi
on observe :
– deux fragments, un fragment de 5,2 kb (“X normal inactif”
méthylé) et un fragment de 2,8 kb (“X actif” non méthylé) chez
une femme normale ;
– quatre fragments, un de 5,2 kb (“X normal inactif”), un de 5,5-
6 kb (“X inactif” amplifié), un de 2,8 kb (“X actif” non méthy-
lé non amplifié) et un de 3-3,5 kb (“X actif” non méthylé ampli-
fié) chez une femme conductrice obligatoire ;
– des fragments dont la taille varie de 6 à 10 kb (“X inactif et
actif” amplifiés), un fragment de 2,8 kb (“X actif” non méthy-
lé et non amplifié) et un fragment de 5,2 kb (“X inactif”
méthylé et non amplifié) chez une femme portant une muta-
tion complète. Un déséquilibre de méthylation est fréquem-
ment observé.
Environ 15 à 40 % des individus porteurs d’une mutation
complète présentent également une prémutation. Cette obser-
vation correspond à la coexistence de cellules avec prémuta-
tion et de cellules avec mutation complète (mosaïcisme).
Cela permet de mieux comprendre l’hétérogénéité clinique
de ce syndrome et les discordances observées entre l’image
autoradiographique du Southern blot et le degré de l’atteinte
clinique. Par ailleurs, il a été décrit l’existence d’hommes
intellectuellement normaux présentant une proportion élevée
(> 60 %) de leucocytes avec mutation complète sans méthy-
lation.
Plus rarement, d’autres anomalies moléculaires, telles que des
mutations ponctuelles (cinq cas rapportés entre 1991 et 1997)
(tableau III) et des délétions emportant en partie ou en totalité
le gène FMR1 (une vingtaine de cas répertoriés depuis 1991),
ont été identifiées, essentiellement dans des formes sporadiques
de l’affection (6). La rareté des mutations ponctuelles dans ce
gène rend difficile à ce jour, en termes de coût-efficacité, la
recherche systématique des mutations ponctuelles dans les
retards mentaux sporadiques inexpliqués.
DIAGNOSTIC PRÉNATAL
Diagnostic prénatal direct
Actuellement, il n’existe pas d’autres moyens de prévention
du syndrome de l’X-fragile. Le diagnostic prénatal du syn-
drome de l’X-fragile peut être proposé aux femmes ayant une
prémutation et à celles ayant une mutation complète. Il peut
être réalisé à partir de l’ADN provenant d’une biopsie de vil-
losités choriales, voire d’amniocytes (délai de réponse plus
long, mais étude de la méthylation) ou de sang fœtal (prati-
quement abandonné).
La méthylation n’étant pas encore définitive chez le fœtus de
12 semaines, le résultat de l’analyse de l’ADN provenant de vil-
losités choriales comporte un certain risque d’erreur. L’analyse
est dans ce cas généralement réalisée par Southern blot après
une simple digestion par EcoRI ou par d’autres enzymes de res-
triction comme PstI, BglII ou HindIII. Ce diagnostic moléculai-
re doit être reservé aux laboratoires qui maîtrisent parfaitement
cette méthode, une mutation hétérogène (mosaïque somatique)
caractérisée par une traînée (smear pour les Anglo-Saxons)
étendue, étant difficilement détectable si le bruit de fond est
important.
Diagnostic prénatal indirect
Dans quelques rares cas (diagnostic prénatal précoce), le dia-
gnostic prénatal moléculaire peut être effectué de manière indi-
recte en utilisant les polymorphismes de répétition de type
microsatellite localisés de part et d’autre du gène FMR1
(notamment DXS548, FRAXAC1 et FRAXAC2, ces deux der-
niers étant localisés à 10 kb de part et d’autre du gène). La fré-
quence de l’hétérozygotie est estimée pour ces deux derniers
marqueurs à 44 et 71 %, respectivement. L’utilisation de ces
marqueurs devrait permettre la réalisation du diagnostic préim-
plantatoire (7). Cette technique, autorisée en France depuis le
24 mars 1998 (décret n° 98-216), vise à un transfert sélectif
d’embryons dépourvus de l’anomalie génétique préalablement
identifiée.
Tableau III. Principales mutations ponctuelles (2) et principaux
variants identifiés dans le gène FMR1.
Nature Localisation Nombre
de cas
Mutations
373 delA exon 5 1
(ACT->CT au codon 125)
23714-23715 GG->TA** intron 1 - exon 2 1
R546H (1856 G->A) exon 15 1
(AGA->AAA au codon 546)
IVS10+14 C->T intron 10 3
I304N (1100 T->A) exon 11 1
(ATT->AAT au codon 304)
Variants**
14100 delCT intron 1 1
23603 A->G intron 1 (14,3 %)*
30584 G->A exon 5 (8,6 %)*
(CGG->CGA au codon 138)
13979 G->T exon 1 1
(GTG->GTT au codon 6)
* Fréquence observée dans la population générale.
** position par rapport à la séquence nucléotidique génomique (GSDB
Acc#L690074).

La Lettre du Neurologue - n° 1 - vol. IV - février 2000 33
Cette stratégie de diagnostic moléculaire indirect nécessite très
peu d’ADN fœtal, et les résultats peuvent être obtenus en
48 heures s’ils sont informatifs. Il est toutefois indispensable de
disposer de l’ADN du sujet atteint (cas index), de la mère et du
père (dans le cas d’un fœtus féminin). La description de rares
cas de conversion génique et de recombinaison avec le locus
DXS548 confirme toutefois la nécessité, lorsque cela est pos-
sible, de vérifier par une analyse directe tout résultat suggérant
un fœtus sain.
TECHNIQUES ALTERNATIVES DE DIAGNOSTIC
PCR (Polymerase Chain Reaction)
La méthode de Southern blot est une technologie lourde,
longue et délicate, ne permettant pas de déterminer avec préci-
sion le nombre de triplets CGG. Ainsi, de nombreux labora-
toires ont essayé depuis quelques années de développer des
méthodes plus simples et plus rapides de diagnostic moléculai-
re. La méthode d’amplification in vitro (PCR) apparaissait ini-
tialement difficilement réalisable en raison du nombre élevé de
triplets et de la nature de ces triplets (en effet, les répétitions
CGG sont difficilement amplifiables). Toutefois, l’utilisation
de certains artifices technologiques a permis d’amplifier les
allèles normaux et les petites prémutations mais n’a pas pu
résoudre complètement le problème posé, notamment par les
mutations complètes. Cette méthode présente l’avantage de
pouvoir estimer avec précision la taille de la prémutation (8).
Ces techniques PCR, qui sont aujourd’hui proposées comme
méthodes de criblage rapide, risquent toutefois d’être des
méthodes délicates à mettre au point et ne peuvent être utilisées
que par des mains expertes.
Analyse de la protéine FMRP
Une dernière alternative repose sur la détection de la protéine
codée par le gène FMR1, dénommée FMRP, soit par Western
blot, soit par immunocytochimie sur un frottis sanguin. Cette
alternative a été rendue possible grâce au développement
d’excellents anticorps monoclonaux. La protéine est absente
chez les hommes, avec mutation complète, atteints d’un
retard mental. En cas de mosaïque associant mutation com-
plète/prémutation, un taux très réduit peut être observé
(expression hétérogène en immunohistochimie). Chez une
femme porteuse d’une mutation complète, l’inactivation au
hasard du chromosome X entraîne la présence de la protéine
dans une proportion variable de cellules, ce qui rend ce dia-
gnostic délicat.
En ce qui concerne l’utilisation de cette méthode en diagnos-
tic de routine sur villosités choriales dans le cadre d’un dia-
gnostic prénatal, une validation est en cours d’évaluation (9).
Néanmoins, il est difficile aujourd’hui d’imaginer que cette
approche puisse concerner les sujets transmetteurs, ce qui
limite son intérêt dans le cadre du conseil génétique.
FONCTION DE LA PROTÉINE FMRP
En 1993, deux équipes ont caractérisé et localisé chez l’homme
les produits d’expression du gène FMR1. De manière inatten-
due, les premiers anticorps spécifiques utilisés en Western blot
ont permis de révéler la présence de cinq bandes, dont les
masses relatives varient de 67 à 74 kDa pour une équipe et de
70 à 80 pour l’autre. Ces bandes sont présentes chez les sujets
normaux et ceux présentant une prémutation, mais elles sont
absentes chez les patients porteurs d’une mutation complète
sans mosaïsisme.
Des études immunocytochimiques et d’hybridation in situ mon-
trent que la protéine a essentiellement une localisation cellulai-
re cytoplasmique. Une isoforme est toutefois retrouvée dans le
noyau cellulaire. La protéine FMRP est exprimée à un taux
élevé dans les neurones, les spermatogonies du sujet adulte et
certains tissus épithéliaux.
Cette protéine FMRP présente deux domaines “K homology”
(KH) et un domaine RGG, impliqués dans la liaison à l’ARN, ce
qui a conduit à la définir comme une “RNA Binding Protein”.
Récemment, elle a été retrouvée associée à la sous-unité riboso-
male 60S, suggérant un rôle direct ou indirect de la protéine
FMRP dans la traduction de certaines protéines. Toutes ces
observations suggèrent qu’elle serait impliquée dans le transport
de certains ARN messagers du noyau dans le cytoplasme, parti-
cipant ainsi à la régulation de la fonction de nombreux gènes.
CONCLUSION
Depuis l’observation originale de Martin et Bell en 1943, des
progrès considérables ont été réalisés notamment dans le
domaine du diagnostic du syndrome de l’X-fragile. Les
méthodes de biologie moléculaire ont ainsi permis :
– de faciliter le diagnostic du syndrome X-fragile, souvent délicat ;
– de dépister les sujets prémutés, c’est-à-dire les femmes
conductrices et les hommes transmetteurs sains ;
– d’évaluer le risque de transition prémutation/mutation com-
plète pour les descendants d’une femme conductrice ;
– de réaliser avec fiabilité un diagnostic prénatal.
Toutefois, le développement de ces méthodes ne permet toujours
pas de prévoir in utero le phénotype des fœtus féminins porteurs
d’une mutation complète. En effet, le risque de retard mental
léger à modéré peut être estimé dans ces cas à environ 60 %.
La recherche systématique de cette anomalie chez les sujets pré-
sentant un retard mental inexpliqué est aujourd’hui justifiée :
par la fréquence élevée de ce syndrome, par le risque significa-
tif posé pour les autres membres de la famille et par le bénéfice
apporté en termes de santé publique.
Sur le plan fondamental, de nombreux mystères restent à éclair-
cir, comme le mécanisme précis de l’expansion des triplets
CGG et l’expression clinique majeure restreinte au cerveau et
aux testicules. L’obtention d’un modèle de souris par recombi-
naison homologue en cellules ES, dans lequel le gène FMR1 a
été détruit, devrait nous permettre de répondre à certaines de ces
questions. ■
 6
6
1
/
6
100%