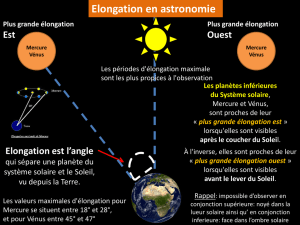
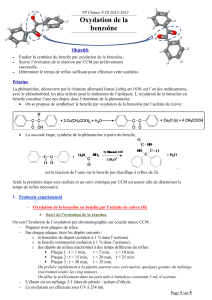
Synthèse du trans-cyclohexane-1,2-diol : Examen de chimie

1/9
BTS CHIMISTE Code Sujet : CHEXP-P06
Session 2006
EPREUVE FONDAMENTALE DE CHIMIE
- Pratique expérimentale -
Durée : 6 heures Coef. : 7
SYNTHESE DU TRANS-CYCLOHEXANE-1,2-DIOL
NBS
H2O
OH
Br
NaOH OHOH
OH
et son énantiomère et son énantiomère
On donne la formule semi-développée du N-bromosuccinimide (NBS) :
NBr
O
O
1. MODE OPÉRATOIRE
Il est conseillé de mener les deux synthèses en parallèle.
1.1. Préparation de l’époxyde du cyclohexène : le 1,2-époxycyclohexane
1.1.1. Obtention du trans-2-bromocyclohexanol
• Dans un erlenmeyer de 100 mL équipé d’un barreau aimanté, placer 6,16 g de cyclohexène.
• Additionner 20 mL d’eau et 25 mL de tétrahydrofuranne (THF).
• Ajouter par portions de 1 g et sous agitation vigoureuse 14,7 g de N-bromosuccinimide.
Maintenir la température du mélange réactionnel à 25-30 °C lors de l’addition. [durée environ
20 min].
• Poursuivre l’agitation 40 min après l’addition en maintenant la température vers 25-30 °C, puis
transférer le mélange dans une ampoule à décanter.
• Diluer par 25 mL d’éther diéthylique et 25 mL d’une solution saturée de chlorure de sodium.
Décanter et séparer les deux phases.
• Retraiter la phase aqueuse par deux fois 20 mL d’éther diéthylique.
• Laver les phases organiques réunies par trois fois 30 mL de solution saturée de chlorure de
sodium.
SUJET N° 6

2/9
1.1.2. Obtention de l’époxyde
• Dans un ballon tricol de 250 mL équipé d’un réfrigérant vertical, d’une ampoule de coulée et
d’un thermomètre, placer 25 mL d’une solution à 5 mol.L-1 d’hydroxyde de sodium.
• Sous agitation et chauffage à 40 °C, additionner goutte à goutte, en 40 min environ, la solution
éthérée de trans-2-bromocyclohexanol précédemment obtenue.
• Poursuivre l’agitation 35 min à température ambiante puis transférer le mélange dans une
ampoule à décanter.
• Séparer la phase organique et la sécher sur sulfate de magnésium anhydre.
• Filtrer.
• Éliminer l'éther diéthylique à l'évaporateur rotatif puis rectifier le résidu.
• Stocker le produit dans un récipient étiqueté. Peser (masse m1).
1.2. Préparation du trans-cyclohexane-1,2-diol
• Placer 5,82 g de 1,2-époxycyclohexane commercial dans un ballon de 100 mL équipé d’une
agitation.
• Ajouter 10 mL d’eau et 1 mL d’une solution 1 mol.L-1 d’acide sulfurique, adapter un
réfrigérant et agiter vigoureusement pendant 1 h au moins. La réaction est exothermique et
une solution limpide doit être obtenue.
• Neutraliser jusqu’à pH 7 par addition goutte à goutte d’une solution saturée
d'hydrogénocarbonate de sodium.
• Éliminer l’eau par distillation simple.
• Ajouter 50 mL d'éthanoate d'éthyle au résidu et porter au reflux (il pourra rester un petit résidu
insoluble que l’on éliminera par filtration à chaud sur büchner).
• Concentrer la phase organique grâce à l'évaporateur rotatif sous vide.
• Cristalliser le diol par simple refroidissement. Filtrer si nécessaire. Sécher.
• Stocker le produit dans un récipient étiqueté. Peser (masse m2).
1.3. Analyses
• Réaliser une analyse CPG de l'époxyde obtenu.
• Enregistrer le spectre IR de l'époxyde obtenu après rectification.
• Mesurer la température de fusion du trans-cyclohexane-1,2-diol obtenu.

3/9
2. DONNÉES
Toutes les températures de changement d'état sont données sous une pression de 1,013 bar.
Produit Données physico-chimiques Phrases R et S
Cyclohexène M = 82,15 g.mol-1
Teb = 83 °C
Insoluble dans l'eau
Soluble dans le THF et l'éther diéthylique
R : 11-21/22
S : 16-23-33-36/37
Tétrahydrofuranne Teb = 64 – 66 °C R : 11-19-36/37
S : 16-29-33
N-bromosuccinimide M = 177,99 g.mol-1
Tfus = 174 - 179 °C
Soluble dans l'eau
R : 22-36/37/38
S : 26-36
Éther diéthylique Teb = 35 °C
R : 12-19-22-66-67
S : 9-16-29-33
Hydroxyde de sodium M = 40,00 g.mol-1
R : 35
S : 26-37/39-45
1,2-époxycyclohexane M = 98,15 g.mol-1
Teb = 130 - 132 °C
Très peu soluble dans l’eau. Soluble dans
l’éthanol, l’éther diéthylique.
R : 10-20/21/22-34
S : 26-36/37/39-45
Acide sulfurique R : 35
S : 26-30-45
Éthanoate d'éthyle Teb = 77 °C
R : 11-36-66-67
S : 16-26-33
Trans-cyclohexane-1,2-diol M = 116,16 g.mol-1
Tfus ≈ 100 °C Les propriétés toxicologiques de ce produit ne sont pas
encore précisées. Le risque de propriétés dangereuses ne
peut donc pas être écarté. Par conséquent, manipuler la
substance avec les précautions d’usage pour les produits
chimiques dangereux.

4/9
3. QUESTIONS
3.1. Préparation du 1,2-époxycyclohexane
Q1- Écrire les équations des deux réactions conduisant à l’époxyde (la première réaction forme la
bromhydrine souhaitée et du succinimide ou butanimide).
Q2- En utilisant la solubilité des réactifs, préciser le rôle du THF.
Q3- Préciser le rôle de l’éther diéthylique.
Q4- Calculer la masse théorique du 1-2-époxycyclohexane attendue (mth1), sachant que le NBS réagit
mole à mole avec le cyclohexène. En déduire l’expression du rendement R1 de cette première synthèse,
puis le rendement corrigé R1c après analyse chromatographique.
Remplir la feuille de résultats
3.2. Préparation du trans-cyclohexane-1,2-diol
Q5- Écrire l’équation de la synthèse à partir de l’époxyde.
Q6- Expliquer pourquoi une solution limpide doit être obtenue à la fin de la réaction.
Q7- Calculer la masse de diol théoriquement attendue (m2). En déduire l’expression du rendement R2
de cette deuxième synthèse.
Q8- En déduire le rendement global R de la préparation du diol à partir du cyclohexène.
Remplir la feuille de résultats
3.3. Contrôle de la qualité des produits obtenus
Q9- Commenter l’analyse par CPG de l’époxyde.
Q10- Commenter le spectre IR du 1,2-époxycyclohexane enregistré.
3.4. Spectroscopie
Q11- Attribuer au cyclohexène, au 1,2-époxycyclohexane et au trans-cyclohexane-1,2-diol les spectres
IR correspondants (annexe 1, page 6/9). Justifier la réponse.
Q12- Analyser le spectre RMN du 1H du 1,2-époxycyclohexane (annexe2).

5/9
NOM : Prénom : Poste :
FEUILLE DE RÉSULTATS
1. SYNTHESE DU 1,2-EPOXYCYCLOHEXANE
Masse de produit : m1 =
Aspect :
Teb =
Pureté CPG :
Expression littérale Calcul
Rendement en
1,2-époxycyclohexane
R1 = R1 = R1corrigé =
2. SYNTHESE DU TRANS-CYCLOHEXANE-1,2-DIOL
Masse de produit : m2 =
Aspect :
Tfus =
Expression littérale Calcul
Rendement en
trans-cyclohexane-1,2-diol
R2 = R2 =
Expression littérale Calcul
Rendement global de la
réaction
R = R = Rcorrigé =
 6
6
 7
7
 8
8
 9
9
1
/
9
100%