Lire l'article complet

La Lettre de l’Infectiologue - Tome XXII - n° 3 - mai-juin 2007
Mise au point
Mise au point
93
7jaaZi^c|gZckdnZgXdbeaiZiVXXdbeV\cYjg\aZbZci|:Y^bVg`H6HÄ'!gjZHV^ciZ"BVg^ZÄ.')&-8djgWZkd^Z8ZYZm
Vous êtes:
Raison sociale : ....................................................................................................................................
(si collectivité : association, administration, société…)
M, Mme, Mlle : ......................................................................................................................................
Prénom: ....................................................................................................................................................
Pratique :
?
hospitalière
?
libérale
?
autre: ........................................................
(cochez)
E-mail (indispensable pour bénécier de nos services internet : archives, newsletters…) :
Votre adresse postale : .................................................................................................................
............................................................................................................................................................................
Ville: ..............................................................................................................................................................
Code postal: ...................................................Pays : ...........................................................................
Tél. : ..................................................................... Fax : ...........................................................................
En cas de réabonnement, de changement d’adresse ou de demande de renseignements,
merci de joindre votre dernière étiquette-adresse.
Votre abonnement prendra eet dans un délai de 3 semaines à réception de votre règlement.
Un justicatif de paiement vous sera adressé.
Votre tarif pour UN AN d’abonnement (6 numéros) :
(Cochez la case qui vous correspond)
?
Collectivité : 108 € TTC
?
Particulier : 90 € TTC au lieu de 120 € (tarif au numéro)
?
Étudiant : 54 € TTC
Vous devez régler :
VOTRE TARIF TTC (inscrivez celui que vous avez coché)................................................................
Port :
Votre revue vous sera envoyée :
?
En France / DOM TOM, Europe, Afrique : (GRATUIT) ..........................
?
En Asie, Océanie, Amérique : 10 € TTC .....................................
TOTAL PORT INCLUS TTC (= + ) ...............................................................
Si vous souhaitez recevoir une reliure pour archiver annuellement votre
revue, nous consulter.
Vous réglez par(cochez) :
?
Carte bancaire VISA,EUROCARD/MASTERCARD
N°
I I I I I I I I I I I I I I I I I
Date d’expiration
I I I I I
Date :
Signature : N° C V V I I I I
(obligatoire) (Trois derniers chires au dos de votre carte bancaire)
?
Prélèvement automatique
(remplir l’autorisation ci-dessous et joindre votre RIB, RIP
ou RICE). France métropolitaine uniquement.
?
Chèque à l’ordre de « La Lettre de l’Infectiologue »
?
Virement bancaire à réception de facture (réservé aux collectivités).
)
Conformément à la Loi Informatique et Liberté du 6 janvier 1978, vous disposez d’un droit d’accès et de rectication des données que vous avez
transmises, en adressant un courrier à Edimark SAS. Les informations requises nous sont nécessaires pour la mise en place de votre abonnement.
Optez pour le prélèvement automatique !
Paiement diéré : Votre abonnement sera prélevé en 3 fois sans frais (sur les
3 mois qui suivent la prise d’abonnement). A réception de votre autorisation de
prélèvement dûment remplie, vous recevrez une facture précisant les échéan-
ces de paiement.
Liberté : Un courrier vous parviendra un mois avant l’échéance de renouvelle-
ment. Sur simple appel, par e-mail ou courrier, vous pouvez refuser le renouvel-
lement et suspendre votre abonnement, ou changer de mode de règlement.
(Remplissez)
J’autorise l’établissement teneur de mon compte à prélever sur ce dernier, si sa
situation le permet, tous les prélèvements ordonnés par le créancier désigné
ci-dessous. En cas de litige sur un prélèvement, je pourrai en faire suspendre
l’exécution par simple demande à l’établissement teneur de mon compte.
Je règlerai le diérend directement avec le créancier.
Titulaire du compte à débiter
Nom: .................................................................................................................
Prénom: .............................................................................................................
Adresse: .............................................................................................................
...........................................................................................................................
Code postal : I I I I I I Ville : ...............................................................
Compte à débiter
Code établissement Code guichet N° de compte Clé RIB
II I I I I I I I I I I I I I I I I I I I I I III
Date ........................... Signature obligatoire :
COMMENT REMPLIR CE DOCUMENT
IMPORTANT : il est indispensable de joindre votre relevé d’identité bancaire (RIB),
postal (RIP) ou de caisse d’épargne (RICE) à cette autorisation dûment remplie.
Nom et adresse de l’établissement teneur du compte à débiter
.........................................................................................................................
.........................................................................................................................
N°: ......................Rue: .....................................................................................
Code postal: I I I I I I Ville: ....................................................................
3
6jidg^hVi^dcYZegakZbZciVjidbVi^fjZ
Organisme créancier
EDIMARK SAS
2, rue Sainte-Marie
92418 COURBEVOIE Cedex
Inscrivez vos nom,
prénom et adresse.
Inscrivez les coordonnées
de votre compte.
Indiquez le nom de votre banque
ainsi que le nom et l’adresse
de votre agence.
Datez et signez (obligatoire).
N° national d’émetteur
512397
Tome XXII - L I N° 3
Bulletin à découper
DJ>!_ZbÉVWdccZedjgjcVc
|
AVAZiigZYZaÉ>c[ZXi^dad\jZ
39ZhfjZhi^dch4
contactez-nous par téléphone au 01 46 67 63 00 (Service abonnements), par E-mail : c[email protected]r ou par fax au 01 46 67 63 09
Zi_ZWcÒX^ZYZaÉd[[gZZmXZei^dccZaaZ;B8
ABO-LI-06.indd 2 22/06/07 10:37:13
Syndrome d’activation macrophagique
Hemophagocytic syndrome
O. Lambotte*, F. Méchaï*
* Service de médecine interne, CHU du Kremlin-Bicêtre, 94275 Le Kremlin-Bicêtre.
RÉSUMÉ
Le syndrome d’activation macrophagique (SAM), ou
syndrome d’hémophagocytose, associe des signes clini-
ques – èvre, hépato-splénomégalie, adénopathies – et
des anomalies biologiques (bi- ou tricytopénies, cytolyse
hépatique, élévation des LDH, coagulopathie) à une image
d’hémophagocytose sur un prélèvement cytologique
ou histologique. Aucun de ces signes n’est spéci que.
Cependant, l’association à une hypertriglycéridémie et à
une hyperferritinémie est très fortement évocatrice du SAM.
Ce syndrome peut être primaire chez l’enfant ou secondaire
à diverses a ections à tout âge. Les infections virales par les
herpès virus (surtout Epstein-Barr et cytomégalovirus), par
les germes intracellulaires (tuberculose), mais aussi par les
bactéries pyogènes sont, avec les néoplasies (lymphomes
principalement) et certaines maladies auto-immunes
(lupus et Still), les principales causes de SAM à rechercher.
La physiopathologie du SAM est mieux comprise grâce
à l’étude des formes primaires. Le SAM est lié à une activa-
tion excessive et/ou à un défaut de cytotoxicité des lympho-
cytes T CD8 et des cellules natural killer (NK) qui sécrètent
de grandes quantités d’interféron γ, activant les cellules
macrophagiques de la moelle osseuse et du système réti-
culo-endothélial, qui libèrent à leur tour des cytokines pro-
in ammatoires.
En dehors des traitements symptomatiques et étio-
logiques, le traitement spéci que du SAM repose prin-
cipalement sur les corticoïdes, les immunoglobulines
intraveineuses et le VP16. Il reste néanmoins mal codi é,
car aucune étude prospective n’est disponible chez l’adulte.
Dans les formes primaires, le VP16 et la ciclosporine ont fait
la preuve de leur e cacité dans l’attente d’une allogre e
de moelle, seul traitement curatif. Le pronostic des SAM est
variable selon l’étiologie, mais la mortalité moyenne est de
50 %. Une telle gravité impose un diagnostic et un traite-
ment précoces, même en l’absence d’image d’hémophago-
cytose, parfois di cile à retrouver.
Mots-clés : Activation macrophagique - Hémophagocy-
tose - Virus d’Epstein Barr - Lymphome.
SUMMARY
The macrophagic activation syndrome or hemophago-
cytic syndrome (HS) is the combination of clinical features,
fever, hepatosplenomegaly and lymphadenopathy; laboratory
abnormalities (cytopenia, liver cytolysis, LDH increase, coagu-
lopathy) associated with an hemophagocytosis picture. No
sign is specifi c. The combination of hypertriglyceridemia and
hyperferritinemia is highly suggestive of the diagnosis. HS
may be primary in children or secondary at any age. Main
causes of HS are infections, especially viral ones by Herpes
viruses (Epstein-Barr, cytomegalovirus), by intracellular germs
(tuberculosis), by pyogenes, neoplasia, mainly lymphomas,
and auto-immune diseases (lupus and Still disease).
The physiopathology of the HS is going to be understood
with the study of the primary forms. HS is due to an excessive
activation and/or a cytotoxicity defect of CD8 T lymphocytes
and NK cells which produce large amounts of Interferon γ which
leads to the activation of bone marrow macrophages and
reticulo-endothelial cells which in turn produce pro-infl am-
matory cytokines.
The treatment is symptomatic and is the treatment of
the cause. In addition, specifi c treatments may be required to
control the HS: steroids, etoposide and intravenous immuno-
globulins. However, the best treatment is not clearly defi ned as
no prospective, randomized trial has been performed, at least
in the adult setting. In primary HS, evidence of the effi cacy of
etoposide and ciclosporin was obtained, to wait for an allogenic
bone marrow allograft as a curative treatment. The prognosis of
HS depends on the etiology but the average mortality is about
50%. Early diagnosis and treatment, despite the possible lack of
the hemophagocytosis picture, which may be diffi cult to fi nd,
are essential to avoid such a severe prognosis.
Keywords: Hemophagocytosis - Epstein-Barr virus - Lymphoma.
En 1979, Risdall et al. (1) individualisaient une entité
clinique caractérisée par de la fi èvre, une hépato-splé-
nomégalie et une pancytopénie. Des adénopathies,
un exanthème et une atteinte pulmonaire étaient souvent
présents. La moelle osseuse et les ganglions étaient infi ltrés par
des macrophages de morphologie normale, qui phagocytaient
des érythrocytes, des plaquettes et des leucocytes. L’autopsie

La Lettre de l’Infectiologue - Tome XXII - n° 3 - mai-juin 2007
Mise au point
Mise au point
94
de six cas mortels montrait une infi ltration méningée et hépa-
tique avec une nécrose hépatocytaire. Il s’agit de la première
description précise du syndrome d’activation macrophagique
(SAM), ou syndrome d’hémophagocytose.
Cette entité associe des signes cliniques dont les principaux sont
la fi èvre et une hépato-splénomégalie, des anomalies biologi-
ques (cytopénies) et une image cytologique caractérisée par des
macrophages phagocytant des éléments nucléés du sang. Cet
aspect d’“hémophagocytose” permet d’affi rmer le diagnostic.
Il est important de noter qu’aucun de ces éléments cliniques
ou biologiques pris isolément n’est spécifi que d’un SAM, et que
ces signes peuvent aussi être ceux d’une maladie sous-jacente
qui est à l’origine du SAM. En outre, comme on le verra, l’image
d’hémophagocytose elle-même doit être interprétée en tenant
compte du contexte clinique. À l’inverse, cette image peut être
très diffi cile à détecter alors même que les autres éléments du
SAM sont présents.
Après l’avoir longtemps considérée comme une prolifération
maligne de la lignée monocytaire, la majorité des auteurs s’ac-
cordent aujourd’hui à dire qu’il s’agit d’une prolifération réac-
tionnelle. Ce syndrome peut être primaire ou secondaire. L’étude
des formes primaires a permis d’avancer dans la compréhension
de la physiopathologie de ce syndrome. Les SAM réactionnels
surviennent principalement au cours d’infections diverses,
notamment virus du groupe Herpès, et de néoplasies. La gravité
de ce syndrome, dont la mortalité selon les séries varie entre 20
et 60 %, impose une enquête étiologique exhaustive, un retard
thérapeutique étant délétère. Cet article s’attachera en parti-
culier aux SAM secondaires aux infections et à la conduite
thérapeutique, qui reste sujette à discussion.
DIAGNOSTIC POSITIF
Clinique
Un SAM peut survenir à tout âge. Néanmoins, les SAM primaires
débutent pendant la petite enfance, voire l’adolescence. Les
formes primaires de révélation tardive (> 20 ans) restent tout
à fait exceptionnelles. L’installation est souvent brutale, mais
l’apparition progressive des symptômes sur 2 à 3 semaines
est possible. Les principaux symptômes sont décrits dans le
tableau I, regroupant les 9 séries publiées depuis 1990, sans
critère de sélection autre que l’âge (2-10).
Il existe de manière quasi constante une fi èvre et une asthénie.
La fi èvre est généralement oscillante, avec des pics atteignant
parfois les 40 °C. Elle peut s’accompagner de frissons et de
sueurs nocturnes. L’asthénie est souvent marquée. La perte de
poids est variable du fait de la fréquence d’œdèmes. Il existe en
eff et une vasoplégie plus ou moins importante qui, combinée
à l’hypoalbuminémie fréquente, peut au maximum réaliser un
tableau d’anasarque. Il s’y associe souvent une organomégalie
avec une hépatomégalie, une splénomégalie, et plus rarement,
des adénopathies périphériques.
D’autres manifestations ont été décrites : des lésions cutanées,
généralement à type d’exanthème maculo-papuleux, une atteinte
pulmonaire avec dyspnée et infi ltrats interstitiels bilatéraux
pouvant conduire à un œdème lésionnel, des manifestations
neurologiques (confusion, convulsions), des troubles digestifs
divers (diarrhées, nausées, douleurs abdominales). La vasoplégie
responsable d’une hypotension, l’œdème pulmonaire lésionnel,
une myocardite, des troubles de conscience peuvent conduire le
malade en réanimation. Les formes pédiatriques sont marquées
par une plus grande fréquence de défaillances cardiorespiratoires
par rapport aux formes adultes (9, 10).
En pratique, un SAM doit être suspecté devant un malade
fébrile “septique” avec une organomégalie et des cytopénies.
Néanmoins, aucune manifestation clinique n’est spécifi que
d’un SAM.
Biologie
Les principaux signes sont détaillés dans le tableau I. Une
cytopénie est présente dans 100 % des cas. Elle est de degré
variable et touche en règle générale au moins deux lignées. Les
lignées plaquettaire et érythrocytaire sont les plus fréquemment
atteintes. La thrombopénie est parfois sévère avec un syndrome
hémorragique variable. Une anémie normocytaire normochrome
pas ou peu régénérative est présente dans 85 à 100 % des cas.
La leucopénie est moins fréquente et souvent plus tardive. Au
maximum, on observe une pancytopénie. Ces cytopénies sont
multifactorielles : hémophagocytose, mais surtout inhibition
de l’hématopoïèse par l’interféron γ (11). Le taux de lympho-
cytes est variable, parfois augmenté. Le frottis peut mettre en
évidence de grands lymphocytes bleutés atypiques, l’existence
d’un syndrome mononucléosique orientant vers les étiologies
virales. L’hypofi brinogénémie est un bon élément d’orientation.
Elle est le plus souvent isolée mais peut être associée à un allon-
gement des temps de coagulation. Une CIVD est un facteur de
mauvais pronostic.
Une cytolyse hépatique est fréquente, et ce indépendamment
de l’étiologie sous-jacente. Elle est souvent modérée, mais peut
être majeure et conduire au décès dans le cadre d’une hépatite
fulminante. Il peut exister une élévation de la bilirubine, associée
ou non à une cholestase.
Les LDH sont élevées dans la majorité des cas, parfois de façon
importante. Elles n’ont cependant pas de valeur pronostique ni
diagnostique. On peut rencontrer une insuffi sance rénale ainsi
qu’une hyponatrémie.
Deux éléments biologiques sont utiles au diagnostic car ils sont
fréquents et assez spécifi ques d’un SAM. Il s’agit, d’une part,
d’une hypertriglycéridémie sans hypercholestérolémie, consé-
quence d’une inhibition de la lipoprotéine lipase (11) par les
cytokines pro-infl ammatoires (TNF, IL-6, IL-1). D’autre part,
il faut noter l’élévation de la ferritine, souvent très importante.
Libérée par les macrophages activés et la nécrose hépatocy-
taire, elle est un bon refl et de l’activité du syndrome. La frac-
tion glycosylée est fréquemment abaissée dans cette situation
(12). Ce point doit être connu car une hyperferritinémie avec
fraction glycosylée abaissée est souvent considérée comme un
marqueur diagnostique de la maladie de Still, maladie elle-même
compliquée de SAM.

La Lettre de l’Infectiologue - Tome XXII - n° 3 - mai-juin 2007
Mise au point
Mise au point
95
IL-1,
IL-6,
TNFB
CD/MF
EBV, LMNH
LT8
Défaut de cytotoxicité
BK
1 Activation T
incontrôlée
3 Activation Mф
incontrôlée
2 Production excessive
de cytokines (IFNH+++,
IL-2, M-CSF, IL-18)
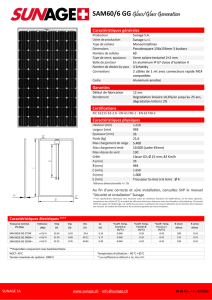
Figure 1.
Hypothèse physiopathologique.
Un facteur initial (infection virale, lymphome, etc.
) induit l’activation des cellules
T et/ou NK qui prolifèrent et produisent de l’IFNγ. Le défi cit de cytotoxicité est
responsable de la persistance du facteur déclenchant et des cellules présen-
tatrices d’antigènes activées (cellules dendritiques [CD] et macrophages)
et d’une activation T incontrôlée (1). Il en résulte un relargage massif (2) de
cytokines pro-infl ammatoires (IL-1, IL-6, TNFα) responsables de l’activation
macrophagique (3) et des manifestations cliniques et biologiques. Ces cyto-
kines et la persistance de CD activées entretiennent l’activation des lympho-
cytes T CD8 et des cellules NK qui produisent de l’IFNγ. Certaines infections
comme la tuberculose pourraient activer directement les macrophages.
Les anomalies éventuelles du bilan immunologique (pic mono-
clonal, autoanticorps) dépendent de la pathologie sous-jacente. La
recherche de facteurs antinucléaires doit néanmoins être systéma-
tique devant un SAM sans étiologie claire, car le lupus érythémateux
disséminé est la seule maladie auto-immune, en plus de la maladie
de Still, à être associée à un SAM spécifi que (13, 14).
Cytologie et histologie
✓ Intérêt diagnostique
La cytologie permet d’affi rmer le diagnostic en montrant l’infi l-
tration des tissus par des histiocytes matures d’aspect cytologique
bénin avec des images d’hémophagocytose (fi gure 1). Ces histio-
cytes comportent des inclusions cytoplasmiques contenant des
cellules hématopoïétiques. Cette hémophagocytose peut concerner
l’ensemble des lignées hématopoïétiques, les lignées érythroïde et
mégacaryocytaire étant les plus fréquemment atteintes.
L’infi ltration histiocytaire peut concerner l’ensemble des tissus
hématopoïétiques (moelle osseuse, rate, ganglions, foie), plus
rarement d’autres organes (système nerveux central [SNC],
peau dans les lymphomes T cutanés).
Au niveau de la moElle osseuse, l’infi ltration est variable, le
myélogramme étant plus sensible que la biopsie ostéomédullaire
(BOM). Les macrophages représentent souvent plus de 5 %
des cellules nucléées. Pour certains auteurs, le pourcentage de
Tableau I.
Fréquence des principales anomalies cliniques et biologiques du SAM (analyse de 9 séries récentes sans critère de sélection autre que l’âge).
Albert (2)
1992
Wong (3)
1992
Tiab (4)
1996
Sailler (5)
1997
Kaito(6)
1997
Tsuda (7)
1997
Takahashi
(8) 2001
Palazzi (9)
2003
Chen (10)
2004
Nombre de patients 45 40 23 99 34 23 52 19 18
Enfants/adultes NR 3/37 6/17 9/90 1/33 0/23 0/52 19/0 18/0
Clinique
Fièvre (%) 100 100 100 61 100 100 100 100 100
Splénomégalie (%) 60 33 76 37 62 35 69 95 61
Hépatomégalie (%) 73 33 50 39 68 35 62 95 89
Adénopathies périphériques (%) 40 25 33 30 41 70 NR 68 44
Lésions cutanées (%) NR 12.5 21 3 NR 26 22.5 58 56
Symptômes respiratoires (%) NR NR NR 0 NR NR NR 90 33
Signes neurologiques (%) NR NR 13 7 NR 0 NR NR NR
Biologie
Thrombopénie (en % ou x109/l) 89 % *67 96 % *100 74 % 91 % **44 79 % 56 %
Anémie (en % ou g/dl) 82 % *9,2 88 % *9,4 53 % 82 % **10 84 % NR
Leucopénie (en % ou x 109/l) 61 % *3,47 76 % *7,3 47 % 65 % **2,2 42 % 50 %
Anomalie du bilan hépatique (%) NR 66 59 97 48 NR 83
– élévation transaminases (%) 75 50 90
– élévation des PAL (%) 97
– hyperbilirubinémie (%) 29 80
Hypofi brinogénémie/coagulopathie (%) 54 33 66 19 NR 30 NR 62 79/81
Hyperferritinémie/hypertriglycéridémie (%) NR/63 NR 90/100 NR/59 NR NR 100/NR 100/44 NR/87
Mortalité (%) 62 45 73 50 59 22 32 53 61
• Deux travaux ne sont pas détaillés dans ce tableau : ceux de Dhote et al. (13) et ceux de Stéphane et al. (14), qui décrivent les SAM survenus au cours de maladies systémiques respectivement chez l’adulte et l’enfant.
• NR : non rapporté ; PAL : phosphatases alcalines ; * : moyenne ; ** : médiane.

La Lettre de l’Infectiologue - Tome XXII - n° 3 - mai-juin 2007
Mise au point
Mise au point
96
macrophages est un critère diagnostique, mais aucune étude
ne retrouve de corrélation entre le nombre de macrophages
médullaires et la gravité. De plus, l’infi ltration histiocytaire n’est
pas homogène et les images d’hémophagocytose peuvent être
absentes des prélèvements, qu’il ne faut pas hésiter à répéter en
cas de forte suspicion de SAM. D’autres anomalies peuvent s’as-
socier à cette infi ltration. L’hypocellularité est variable. Il existe
fréquemment une hypoplasie de la lignée granuleuse et une
érythroblastose témoignant de l’érythropoïèse réactionnelle.
L’histologie hépatique est souvent positive en cas de SAM. Elle
montre une infi ltration des sinusoïdes et des espaces portes par
des histiocytes, et des cellules de Kupff er hypertrophiées avec
hémophagocytose (15). Une infi ltration des espaces portes par des
lymphocytes T CD8 est également commune, de même qu’une
nécrose hépatocytaire, non corrélée à l’élévation des transaminases.
Enfi n, il n’existe généralement pas d’atteinte des canaux biliaires.
Il est important de noter que des images d’hémophagocytose
peuvent se rencontrer en l’absence de SAM au cours de nombreuses
hémopathies et après transfusions. Dans une série de 107 autopsies
consécutives de patients décédés en réanimation en l’absence de
SAM clinique, les auteurs retrouvent des images d’hémophagocy-
tose dans 64 % des biopsies ostéomédullaires post-mortem, avec
comme principaux facteurs associés les transfusions et l’existence
d’un sepsis (16). L’histologie est donc indissociable de la clinique.
✓ Intérêt étiologique
Dans le cas d’un malade chez qui un SAM est suspecté, les examens
cytologiques et histologiques peuvent aider, en plus du diagnostic
positif, à poser le diagnostic étiologique. Les colorations usuelles
permettent de visualiser sur un myélogramme ou une cytologie
ganglionnaire des agents infectieux (tuberculose, histoplasmose,
cryptococcose, leishmaniose). La biopsie ostéomédullaire, mais aussi
ganglionnaire, est souvent plus rentable que le myélogramme pour la
recherche d’une cause néoplasique et doit être pratiquée chaque fois
qu’un lymphome est suspecté. Elle peut aussi montrer des granulomes.
La biopsie de toute lésion suspecte cutanée est systématique. Enfi n,
la biopsie hépatique permet souvent d’obtenir le diagnostic, mais elle
est plus diffi cile à réaliser en raison des troubles de l’hémostase.
Les critères diagnostiques et la pratique…
En raison des diffi cultés pour établir le diagnostic de SAM (images
d’hémophagocytose dans des situations cliniques sans fi èvre ou
sans cytopénie ou fi èvre et cytopénies sans image, etc.), plusieurs
auteurs ont proposé des critères diagnostiques (tableau II). Ces
derniers étaient aussi nécessaires pour inclure les enfants atteints
de SAM primaires dans des essais thérapeutiques et avoir des
populations homogènes. Dans ces critères, l’image d’hémo-
phagocytose est nécessaire, mais pas suffi sante pour affi rmer le
diagnostic. Ces critères, ceux de l’Histiocyte Society comme ceux
d’Imashuku (17, 18), ont été validés en pédiatrie mais pas chez
l’adulte. De plus, selon ces critères, on ne peut parler de SAM que
si l’image cytologique est présente. Or il existe des situations où
le tableau clinico-biologique est évocateur mais où la cytologie
reste négative. Ne pas traiter pour cette raison alors que le malade
est dans un état critique serait déraisonnable.
DIAGNOSTIC ÉTIOLOGIQUE
L’existence d’une immunosuppression sous-jacente au SAM,
acquise ou constitutionnelle, est un facteur important que l’on
retrouve dans la plupart des séries.
Les SAM primaires
Quatre syndromes héréditaires d’activation macrophagique et
lymphocytaire ont été décrits. Il s’agit de la lymphohistiocytose
familiale, du syndrome de Chediak-Higashi, du syndrome de
Griscelli et du syndrome de Purtilo. Tous ces syndromes ont
en commun un défaut de cytotoxicité des lymphocytes T et/ou
des cellules natural killer (NK) [19]. Ils se révèlent chez l’enfant
ou l’adulte jeune souvent à l’occasion d’une infection inter-
currente. L’évolution est fatale sans traitement. Les anomalies
génétiques responsables du défi cit immunitaire observé dans
le SAM sont pour la plupart individualisées et permettent de
mieux comprendre la physiopathologie des SAM.
✓ La lymphohistiocytose familiale
Il s’agit de la pathologie la plus fréquente parmi les SAM primaires.
Pathologie autosomique récessive, elle se révèle dans la petite
enfance. La présentation clinique est celle d’un SAM, mais il
faut noter la fréquence des atteintes du SNC (50 %), de mauvais
pronostic. La base génétique de la lymphohistiocytose familiale
est diverse, composée de mutations inactivatrices du gène codant
pour la perforine, protéine clé de la cytotoxicité (40 % des cas),
de mutations du gène Munc 13-4, impliqué dans la sécrétion des
Tableau II.
Critères diagnostiques des SAM.
Histiocyte Society 1991 (tous les critères sont exigés) [17]
Critères cliniques
· Fièvre > 7 jours avec pics > 38,5 °C
· Splénomégalie
Critères biologiques
· Cytopénie sur deux ou trois lignées (Hb < 9 g/dl, PNN < 1 000/mm3,
plaquettes < 100 000/mm3) non expliquée par une moelle pauvre ou
hypoplasique
· Hypertriglycéridémie (> 2 mmol/l) et/ou hypofi brinogénémie (< 1,5 g/l)
Critères histologiques
· Image d’hémophagocytose
· Absence de signe de malignité
Critères d’Imashuku (18) 1997 (tous les critères sont exigés)
Critères cliniques
· Fièvre > 7 jours avec pics > 38,5°C
Critères biologiques
· Cytopénie sur deux ou trois lignées (Hb < 9 g/dl, PNN < 1 000/mm3,
plaquettes < 100 000/mm3) non expliquée par une moelle pauvre ou
hypoplasique
· Hyperferritinémie plasmatique (> 3N ou >1 000 ng/ml)
· Augmentation des LDH (> 3N ou > 1 000 UI/l)
Critères histologiques
· Image d’hémophagocytose

La Lettre de l’Infectiologue - Tome XXII - n° 3 - mai-juin 2007
Mise au point
Mise au point
97
lysosomes (20-30 %) et d’observations sans anomalie génétique
retrouvée. C’est dans cette pathologie qu’ont été réalisés les seuls
essais thérapeutiques conduits dans les SAM et qui ont montré
l’importance de la chimiothérapie et des immunosuppresseurs
pour contrôler le SAM. La guérison chez ces enfants ne peut être
obtenue qu’avec une allogreff e de moelle.
✓ Le syndrome de Chediak-Higashi
Ce syndrome, caractérisé par un SAM, un albinisme partiel
cutané et oculaire et la présence de grandes granulations intra-
cytoplasmiques, est dû à des mutations dans le gène LYST
impliqué dans l’adressage des protéines intracellulaires. Les
protéines impliquées dans la cytotoxicité s’accumulent dans les
lysosomes, expliquant les granulations observées.
✓ Le syndrome de Griscelli
Syndrome identique à celui de Chediak-Higashi sans granu-
lations intracytoplasmiques, il est dû à une mutation dans le
gène Rab27 impliqué dans l’exocytose des vésicules intracyto-
plasmiques.
✓ Le syndrome lymphoprolifératif lié à l’X ou syndrome
de Purtilo
C’est un défi cit immunitaire rare, lié à l’X, caractérisé par une
susceptibilité anormale à l’infection par le virus d’Epstein-Barr
(EBV). Le mode de révélation est une mononucléose fulminante
chez la moitié des enfants, fatale le plus souvent. Les autres
modes de révélation sont une hypogammaglobulinémie ou
une agammaglobulinémie, un lymphome malin non hodgki-
nien. Des vascularites ont également été rapportées. Le gène
responsable de ce syndrome est connu : il s’agit du gène codant
pour la protéine SAP SLAM-associated protein. Cette protéine
est exprimée sur les lymphocytes T, B et NK. Elle permet la
transduction d’un signal d’activation conduisant à une activité
cytotoxique des lymphocytes T CD8 et NK et semble jouer un
rôle clé dans la cytotoxicité anti-EBV.
Les SAM secondaires
Le SAM peut également être réactionnel. C’est toujours le cas
chez l’adulte. Infections, néoplasies et maladies de système
peuvent ainsi se compliquer de SAM. Les principales étiologies
sont détaillées dans le tableau III.
✓ Infections
C’est en 1979 que Risdall et al. décrivaient 19 cas de lymphohis-
tiocytose bénigne secondaire à une infection virale. Les germes
impliqués dans la survenue de SAM sont listés dans le tableau III
et leurs fréquences respectives dans les tableaux IV et V, respecti-
vement chez l’adulte et l’enfant. Pratiquement toutes les infections
virales, bactériennes, fongiques et parasitaires ont été associées à la
survenue d’un SAM, mais il s’agit le plus souvent de cas isolés (20).
Ces observations correspondent vraisemblablement aux formes
“malignes” décrites pour chaque maladie infectieuse dans les anciens
traités de médecine. Plusieurs agents infectieux peuvent être identi-
fi és chez un même patient au même moment, cela d’autant plus que
de nombreux malades sont immunodéprimés de façon chronique
(greff é, infection par le VIH, chimiothérapie, traitement immuno-
suppresseur pour une maladie systémique). Néanmoins, imputer
la survenue du SAM à une infection donnée n’est pas toujours
aisé, car les infections peuvent compliquer une maladie elle-même
responsable de SAM, telle que lymphome, lupus, etc. Ainsi, le SAM
des lymphohistiocytoses familiales est souvent déclenché par une
infection virale. D’autre part, l’immunodépression liée au SAM
(neutropénie) favorise la survenue d’infections.
Tableau III.
Principales étiologies de SAM.
Infections
– Virales
– Bactériennes
· mycobactéries
· autres
– Fongiques
– Parasitaires
Herpesviridae (EBV, CMV, HSV, VZV, HHV-6 et HHV-8), VIH, parvovirus B19, adénovirus, entérovirus, hépatite A, B, C,
virus parainfl uenzae, infl uenzae, oreillons, rubéole, dengue, hantavirus, virus amaril…
Mycobacterium tuberculosis, mycobactéries atypiques
Entérobactéries, Salmonella typhi, staphylocoques, streptocoques, Haemophilus in uenzae, Pseudomonas, Legionella,
rickettsioses, brucellose, borréliose, leptospirose, Coxiella burnetii,
mycoplasme, Chlamydia, syphilis, Ehrlichia, Corynebacterium, Bartonella
Candidose, Histoplasma capsulatum, cryptococcose, Aspergillus fumigatus, Penicillium marne ei
Leishmaniose, Plasmodium, babésiose, Pneumocystis jiroveci, toxoplasmose
Néoplasies
– Hémopathies
– Cancers solides
Lymphome non hodgkinien T, NK, B ; maladie de Hodgkin, leucémie aiguë
Maladies de système
– SAM spécifi que de la maladie
– SAM dans le cadre de complications
infectieuses
Lupus érythémateux aigu systémique, arthrite chronique juvénile, Still de l’adulte
Polyarthrite rhumatoïde, connectivite mixte, syndrome de Gougerot-Sjögren, sarcoïdose, périartérite noueuse,
Kawasaki
Réaction d’hypersensibilité médicamenteuse
 6
6
 7
7
 8
8
 9
9
 10
10
1
/
10
100%