Mise au point C Leptine et reproduction Leptin and reproduction

Métabolismes Hormones Diabètes et Nutrition (VIII), n° 4-5, juillet/octobre 2004
Mise au point
Mise au point
Leptine et reproduction
Leptin and reproduction
M. Caprio*
C
hez les mammifères, la fonction reproductive est
strictement dépendante des disponibilités énergé-
tiques environnementales. Il est bien connu que des
modifications aiguës de l’état métabolique sont capables
d’altérer la fonction de l’axe hypothalamo-hypophyso-
gonadique (HHG). Dans plusieurs modèles animaux et
chez l’homme, le jeûne et la restriction calorique déter-
minent la suppression rapide de la sécrétion pulsatile
de l’hormone lutéinisante (LH) et l’hormone folliculo-
stimulante (FSH). Un tel mécanisme prévient probable-
ment la dépense d’énergie dans des conditions où le succès
reproductif est très improbable. Par ailleurs, le stockage
excessif des réserves métaboliques, notamment dans le
cas de l’obésité, interfère aussi avec une régulation correcte
de l’axe reproductif. Dans le cadre de ces interactions
délicates avec l’environnement, l’état métabolique et la
fonction reproductive, le tissu adipeux joue un rôle de
relais, informant directement les structures cérébrales
supérieures des réserves énergétiques disponibles à travers
ses produits de sécrétion. La découverte de la leptine et
de son récepteur ainsi que l’existence de modèles ani-
maux de déficience ou de résistance à la leptine ont beau-
coup apporté à la compréhension des relations entre
réserves d’énergie, tissu adipeux et fonction reproduc-
tive. Par ailleurs, les centres de contrôle hypothalamiques
de l’axe reproductif sont localisés à proximité des centres
anatomiques qui contrôlent la faim.
Leptine et récepteur
La leptine est une protéine de 16 kDa, produite principa-
lement par le tissu adipeux blanc (1), mais aussi par le pla-
centa (2), l’estomac (3) et le muscle squelettique. Elle est
codée par le gène Lep 1, qui comprend trois exons ; sa struc-
ture protéique ressemble à celle des cytokines et des hor-
mones lactogènes. La leptine est constituée de 167 acides
aminés et circule dans le sang en concentrations pro-
portionnelles à la masse grasse. Elle inhibe l’appétit au
niveau hypothalamique à travers son action stimulante
sur la production cérébrale de peptides anorexigènes,
* INSERM U478, faculté de médecine Xavier-Bichat, Paris. Chaire d’endocrino-
logie, département de médecine interne, université de Tor Vergata, Rome, Italie.
179
▲
▲La leptine est une protéine de 16 kDa, produite
principalement par le tissu adipeux blanc.
▲
▲La leptine circule dans le sang en concentrations
proportionnelles à la masse grasse et agit comme
facteur anorexigène au niveau hypothalamique.
▲
▲Le récepteur de la leptine (Ob-R) appartient à la
famille des récepteurs des cytokines. Il existe sous
différentes isoformes et est principalement exprimé
dans l’hypothalamus.
▲
▲Ob-R est aussi exprimé par les tissus périphériques
de l’axe reproductif (hypophyse, ovaire, testicule,
surrénale), ce qui suggère que la leptine joue un
rôle dans le contrôle de la fonction reproductive à
plusieurs niveaux anatomiques.
▲
▲La souris
ob/ob
, porteuse d’une mutation homo-
zygote inactivatrice sur le gène de la leptine, est très
obèse et infertile. Le traitement avec leptine permet
de restaurer une composition corporelle normale
ainsi que la fertilité. Cela indique que la leptine est
nécessaire dans le contrôle de la reproduction.
▲
▲Des études in vitro ont montré que la leptine, à
concentrations élevées, inhibe directement la
stéroïdogenèse ovarienne et testiculaire chez plu-
sieurs modèles animaux.
▲
▲Dans l’anorexie mentale, une aménorrhée est
observée lorsque les taux de leptine circulante sont
en dessous d’un certain seuil.
▲
▲Dans l’obésité, qui est caractérisée par des taux très
élevés de leptine circulante, on observe souvent des
troubles de la reproduction, notamment une infer-
tilité, un hypogonadisme et des taux réduits de
stéroïdes sexuels.
▲
▲Chez la femme, les taux de leptine sont plus élevés
pendant la grossesse, déclinent après l’accou-
chement et restent bas pendant la lactation, ce qui
suggère un rôle important de l’hormone dans ces
phases de la vie reproductive.
▲
▲Des taux de leptine situés dans une fourchette très
étroite sont nécessaires pour le bon fonctionnement
et le maintien de l’axe reproductif.
Mots-clés : Leptine – Stéroïdes sexuels – GnRH – Testicule.
points FORTS
1. La nomenclature officielle pour le gène codant pour la leptine est LEP
pour le gène humain et Lep pour son homologue murin.

180
Métabolismes Hormones Diabètes et Nutrition (VIII), n° 4-5, juillet/octobre 2004
Mise au point
Mise au point
notamment la pro-opiomélanocortine (POMC) et ses pro-
duits de clivage, parmi lesquels la mélanocortine. De plus,
elle inhibe l’expression de peptides orexigènes, comme
le neuropeptide Y (NPY) et l’Agouti-Related Protein
(AgRP) (4). Sa sécrétion est pulsatile et synchronisée
avec celle de la LH, montrant un rythme circadien, avec
une augmentation nocturne qui atteint son pic entre 1 h
et 2 h. Les taux plasmatiques de leptine ne dépendent pas
seulement de la masse adipeuse, mais sont aussi contrôlés
par des facteurs hormonaux et nutritionnels. La prise
alimentaire détermine une élévation rapide des concen-
trations plasmatiques de leptine (d’environ 40 %) ; en
revanche, l’expression du gène Lep et les taux de leptine
circulants sont rapidement réduits par le jeûne (5). Sous
condition d’équilibre métabolique, les taux sériques de
leptine dépendent donc des réserves adipeuses ; cepen-
dant, ils varient de façon indépendante de la masse grais-
seuse pendant les modifications aiguës de la balance
énergétique.
Le récepteur de la leptine (Ob-R), codé par le gène Lepr,
appartient à la famille gp130 des récepteurs des cyto-
kines. Il présente un seul domaine transmembranaire et
existe sous différentes isoformes (Ob-Ra, Ob-Rb, Ob-Rc,
Ob-Rd, Ob-Re) issues de l’épissage alternatif de l’ARN
messager, qui diffèrent entre elles uniquement dans la
portion C-terminale (figure 1) (6). Seule l’isoforme Ob-Rb
possède un domaine intracellulaire long et transmet le
signal par activation de la voie de signalisation Janus-
kinase (JAK-STAT) en activant signal transducer and
activator of transcription 3 (STAT-3). Cette isoforme est
principalement exprimée dans l’hypothalamus, son taux
d’expression étant beaucoup plus faible dans les tissus
périphériques, où Ob-Ra est la forme prédominante. Ob-Ra
présente un domaine intracellulaire court (< 30 aa) qui
n’est pas capable d’activer la voie de signalisation JAK-
STAT. Des observations récentes suggèrent que Ob-Ra
pourrait activer la cascade des mitogene-activated protein
kinase (MAPK) (7).
Modèles in vivo de déficience, résistance
et excès de leptine
L’existence d’un modèle animal présentant une mutation
homozygote inactivatrice du gène Lep, la souris ob/ob,a
été fondamentale pour la compréhension des liens entre
tissu adipeux et axe reproductif. La souris ob/ob est infer-
tile et présente une interruption majeure de la spermato-
genèse, due à une insuffisance hypothalamo-hypophy-
saire (1). Le traitement par la leptine est capable de
restaurer la fertilité dans les deux sexes (8, 9). En revanche,
la seule restriction calorique n’est pas capable de rétablir
la fonction reproductive, ce qui suggère que l’obésité per
se n’est pas la cause de l’infertilité, et que la leptine
constitue un facteur nécessaire au contrôle de la repro-
duction.
Par ailleurs, dans un autre modèle, la souris db/db, une
mutation du gène Lepr provoque la synthèse d’un récep-
teur ne comportant plus une large partie de sa portion
intracellulaire. La souris db/db présente des troubles de la
reproduction tout à fait similaires à ceux de la souris ob/ob,
mais le traitement à la leptine est incapable de restaurer
sa fertilité. Des mutations inactivatrices des gènes LEP
et LEPR, même si elles sont extrêmement rares, ont aussi
été mises en évidence chez l’homme ; elles induisent des
anomalies très similaires à celles retrouvées chez la souris
ob/ob et db/db (10). La mutation homozygote du gène
LEP provoque une obésité sévère associée à l’absence de
développement pubertaire. Elle se manifeste chez la
femme par une aménorrhée primaire, et par des signes
cliniques d’hypogonadisme chez l’homme, avec un pro-
fil prépubertaire de sécrétion des gonadotrophines. Chez
une patiente de 9 ans ayant un déficit congénital en lep-
tine, le traitement par leptine recombinante a été suivi par
une perte rapide de poids et de masse grasse, associée au
rétablissement de la pulsatilité des gonadotrophines (10).
Des résultats analogues ont été récemment obtenus chez
trois patients adultes traités par de la leptine recombi-
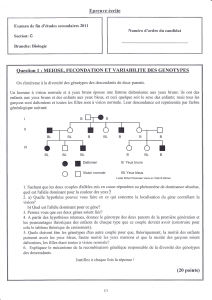
Figure 1. Représentation schématique des iso-
formes du récepteur de la leptine.
Le gène code pour au moins cinq isoformes
connues (Ob-Ra – Ob-Re) par épissage alternatif
de l’ARNm. Toutes les isoformes, à l’exception
de Ob-Re, ont une structure identique jusqu’à la
Lys 889 ; à partir de cette position, les séquences
protéiques divergent. Seul Ob-Rb contient les
deux cassettes protéiques capables d’activer la
cascade JAK-STAT. Ob-Re est identique aux
autres isoformes en amont de l’His 796, et pos-
sède ensuite neuf acides aminés additionnels.
Cette isoforme est probablement de nature
soluble.
Abréviations : aa : acide-aminé ; EC : extracel-
lulaire ; IC : intracellulaire ; TM : transmem-
branaire.
TM
EC
23 aa
Ob-Ra
816 aa 805 aa
Ob-Rb Ob-Rc Ob-Rd Ob-Re
303 aa Lys 889
Cassette 1
Cassette 1 Cassette 2
Cassette 2
EC TM
His 796 Lys 889
IC

181
Métabolismes Hormones Diabètes et Nutrition (VIII), n° 4-5, juillet/octobre 2004
Mise au point
Mise au point
nante (0,01-0,04 mg/kg pendant 18 mois) : parallèlement
à la perte de masse graisseuse, les taux de stéroïdes
sexuels circulants ont significativement augmenté (11).
De la même façon, des cas de femmes porteuses d’une
mutation non-sens du gène LEPR ont été décrits : en plus
de l’obésité précoce, et elles ont une absence de carac-
tères sexuels secondaires et une aménorrhée, avec des
taux très bas d’estrogènes, de LH et de FSH (12). Ces
données indiquent de façon très claire que l’intégrité du
système leptine-récepteur est indispensable pour assurer
un développement correct de la puberté et une fonction
reproductive normale. À la différence des modèles d’obé-
sité monogénique dus à des défauts des gènes LEP et
LEPR, les mutations de l’isoforme 4 du récepteur de la
mélanocortine (MC4-R), qui joue une rôle fondamental
dans les actions inhibitrices de la leptine sur la prise ali-
mentaire, ne modifient pas l’axe reproductif chez la souris
(13) et chez l’homme (14). Les caractères sexuels secon-
daires et la puberté sont normaux, comme le taux circulant
de stéroïdes sexuels et de gonadotrophines. Cela indique
que la fonction des récepteurs MC4-R n’est pas impli-
quée dans les effets neuroendocrines de la leptine sur les
neurones sécrétant la gonadolibérine (GnRH), et donc sur
la fonction reproductive. Afin de tester l’importance de
l’activation de STAT-3 par Ob-R sur les fonctions de la
leptine, un modèle de souris knock-out pour STAT-3 dans
le cerveau a été généré. De façon intéressante, ces souris
étaient hyperphagiques, diabétiques et infertiles, comme
les souris ob/ob et db/db (15). Dans le même but, d’autres
auteurs ont remplacé le gène Lepr par un gène dans lequel
la Tyr 1138 avait été remplacée par une sérine. Ce résidu
est fondamental pour l’activation de la voie de signalisa-
tion JAK-STAT. Les souris porteuses du gène Lepr ainsi
muté étaient hyperphagiques et obèses, mais leur capacité
reproductive était intacte, contrairement à ce que l’on
observe chez les souris knock-out pour STAT-3. Ces
données suggèrent que le contrôle hypothalamique de la
reproduction effectué par la leptine passe aussi par des
voies de signalisation différentes de STAT-3, bien que les
mécanismes intracellulaires par lesquelles Ob-R contrôle
la fonction reproductive au niveau hypothalamique, res-
tent encore obscurs.
La disponibilité d’un modèle murin présentant un taux
constamment élevé de leptine a aussi clarifié certains
aspects de la fonction de cette hormone. Caractérisée par
l’absence de tissu adipeux et par une hyperleptinémie, la
souris femelle transgénique skinny présente une accéléra-
tion de la maturation sexuelle, suivie d’un hypogonadisme
avec réduction de sécrétion de GnRH et de LH (16).
L’hyperleptinémie in vivo semble donc stimuler le début
de la puberté, mais, lorsqu’elle est chroniquement persis-
tante, elle peut aussi inhiber les signaux centraux qui sti-
mulent la fonction reproductive. Il est donc probable qu’il
existe plusieurs niveaux et différents seuils d’action de la
leptine sur la fonction reproductive.
Leptine et sécrétion de gonadotrophines
L’isoforme longue du récepteur de la leptine a été localisée
principalement au niveau hypothalamique, dans les noyaux
arqué et ventromédian, qui contrôlent en même temps la
prise alimentaire et le comportement sexuel. Dans ces
noyaux, la leptine joue le rôle de médiateur entre les mes-
sages périphériques de balance métabolique et la fonction
reproductive. Plusieurs données soulignent que la leptine,
comme signal de jeûne, est responsable des altérations de
l’axe reproductif liées à la sous-nutrition. Cette hypo-
thèse a été confortée par les expériences suivantes : chez
la souris (17) et chez le singe (18), lorsque l’on prévient
la baisse de leptine induite par le jeûne en administrant
cette hormone, on restaure la pulsatilité de la LH et l’on
prévient le retard de l’ovulation chez la femelle. La lep-
tine est donc capable de contrer les effets inhibiteurs du
jeûne sur la sécrétion de gonadotrophines. De plus, lorsque
l’on administre des anticorps antileptine dans les ventri-
cules latéraux de rats nourris de façon normale, dans le
but de mimer la forte baisse de leptine pendant le jeûne,
on observe une diminution de la pulsatilité de la LH et un
arrêt de la cyclicité œstrale. Ces données confirment que
la leptine exerce un effet tonique de facilitation sur les
circuits neuronaux qui contrôlent la sécrétion de gona-
dotrophines. Cependant, dans d’autres modèles animaux,
la leptine n’a pas été capable de corriger l’inhibition
du comportement sexuel observée pendant la restriction
alimentaire (19).
Dans l’anorexie mentale, la sous-nutrition sévère est
associée à des niveaux très faibles de leptine plasmatique
et intracérébrale, à des taux bas et non pulsatiles de
gonadotrophines, à des altérations menstruelles et à une
aménorrhée (20). Une valeur seuil de 1,85 ng/ml a été
identifiée, au-dessous de laquelle on observe régulière-
ment une aménorrhée. Lors de la réascension pondérale
chez ces patientes, la restauration du cycle menstruel est
toujours associée à des valeurs de leptine au-dessus de ce
seuil. Cependant, à la hausse rapide du taux de leptine
plasmatique liée à la prise de poids ne correspond pas
toujours la reprise du cycle menstruel (21). Cela suggère
que d’autres facteurs contribuent à la reprise de la fonction
reproductive, notamment l’activation de l’axe GH-IGF-1,
qui nécessite par ailleurs une période plus longue pour se
rétablir (20). Des taux de leptine au-dessus d’un seuil
minimal pourraient donc être nécessaires, mais pas suffi-
sants, pour la reprise du cycle menstruel chez les patientes
anorexiques.
L’effet de la leptine sur la reproduction pourrait aussi
impliquer le métabolisme intracellulaire et être dépendant
de la disponibilité des réserves énergétiques en périphérie.
Chez le hamster à jeun traité par le 2-désoxyglucose (un
inhibiteur compétitif de l’utilisation du glucose), l’admi-
nistration de leptine n’était pas entièrement capable de
rétablir les cycles menstruels (22). Il est donc possible que
la leptine ne puisse pas rétablir la sécrétion des gonado-

182
Métabolismes Hormones Diabètes et Nutrition (VIII), n° 4-5, juillet/octobre 2004
Mise au point
Mise au point
trophines en présence de stress métaboliques dûs à l’impos-
sibilité d’utiliser les réserves métaboliques périphériques.
Les actions centrales de la leptine pourraient donc s’intégrer
avec différents signaux métaboliques afin de contrôler
l’activité des neurones à GnRH.
Leptine et neurones GnRH
Plusieurs observations in vitro ont montré que des concen-
trations de leptine subnanomolaires stimulent la libéra-
tion de GnRH à partir d’explants d’éminence médiane et
de noyau arqué de rat après une incubation de quelques
minutes (23). Par ailleurs, quand des concentrations plus
élevées de leptine (de l’ordre du micromolaire) étaient uti-
lisées, la sécrétion de GnRH était supprimée. Ces données
ont aussi été confirmées sur une lignée cellulaire immor-
talisée (les cellules GT1-7) sécrétant la GnRH et expri-
mant Ob-R. Dans ce modèle cellulaire, la libération de la
GnRH était stimulée par l’incubation avec des doses faibles
de leptine (10-12 à 10-10 M), mais pas par des concentra-
tions plus élevées (24). L’ensemble des ces données montre
que la leptine agit au niveau central sur l’axe reproductif,
mais que l’effet stimulateur est observé uniquement dans
une fourchette de concentrations de leptine assez étroite.
Il est encore difficile de déterminer si les actions de la
leptine ont lieu directement sur les neurones sécrétant la
GnRH ou à travers un circuit interneuronal. Des études
de double marquage chez le rongeur et le primate n’ont
pas mis en évidence de coexpression de GnRH et de Ob-R
dans les corps cellulaires. L’hypothèse d’intermédiaires
neuronaux entre la leptine et la GnRH est donc envisa-
geable (18). L’expression de Ob-R est abondante dans les
neurones sécrétant la POMC, le NPY et l’AgRP du noyau
arqué chez le rat. Le peptide Cocaine- and Amphetamine-
Related Transcript (CART) a été récemment décrit comme
inhibiteur endogène de la prise alimentaire (25). Il est
impliqué dans l’accélération de la sécrétion pulsatile de
la GnRH et est régulé par la leptine. De façon intéres-
sante, les anticorps anti-CART peuvent annuler les effets
stimulateurs de la leptine sur la pulsatilité de la GnRH
dans des explants hypothalamiques de rat péripubertaire
(26). Ces données suggèrent que CART pourrait être un
facteur intervenant dans l’action de la leptine sur les neu-
rones sécrétant la GnRH, spécifiquement pendant la
phase péripubertaire. Par ailleurs, des études récentes
conduites chez la souris knock-out pour le récepteur Y1
du NPY ont montré que la restriction calorique n’empê-
chait pas la maturation sexuelle dans ce modèle (27) :
l’absence des récepteurs Y1 prévient donc la perception
de l’insuffisance des réserves métaboliques par l’axe
gonadotrope, ce qui suggère un rôle physiologique des
neurones NPY dans les circuits neuronaux responsables
de l’action de la leptine sur les neurones à GnRH in vivo.
Leptine et hypophyse
L’ARN messager codant pour Ob-R a été identifié dans
l’hypophyse de rat adulte, l’hypophyse fœtale humaine
et dans les adénomes hypophysaires. Des études d’im-
munohistochimie ont montré l’expression de la protéine
Ob-R dans les cellules gonadotropes de l’hypophyse
ovine (28). D’autres études ont montré l’expression des
isoformes longues et courtes de Ob-R et de la leptine
dans le tissu hypophysaire humain normal et tumoral
(29). Ces données suggèrent que la leptine pourrait régu-
ler la fonction hypophysaire par des mécanismes endo-
crines et/ou paracrines-autocrines. Des études in vitro ont
montré que l’incubation de tissu hypophysaire de rat avec
la leptine induit la libération de gonadotrophines de façon
dose-dépendante : à doses très faibles (10-10 à 10-9 M), on
observe un effet stimulateur, qui disparaît à des doses
plus fortes (10-8 à 10-7 M) (23). Cela indique que la leptine,
à des concentrations physiologiques, influence positive-
ment la fonction des cellules gonadotropes, amplifiant les
actions stimulatrices sur l’axe reproductif exercées au
niveau hypothalamique. En revanche, à des concentrations
plus élevées (telles qu’on les retrouve chez les patients
obèses) la leptine pourrait réduire la fonction reproductive
au niveau hypophysaire. En accord avec cette hypothèse,
une étude récente réalisée sur une cohorte de 42 adoles-
centes obèses a démontré que l’index de masse corporelle
(IMC) et les taux de leptine étaient des déterminants sta-
tistiques négatifs de la sécrétion de gonadotrophines, cela
suggérant que l’augmentation de la masse grasse et donc
l’excès de leptine autour de la période pubertaire sont
associés à une réduction de la sécrétion de gonadotro-
phines chez la femme. En revanche, cette corrélation n’a
pas été démontrée chez l’homme (30).
Leptine et puberté
Le phénotype reproductif des souris ob/ob et db/db, infer-
tiles et incapables de maturation sexuelle, a indiqué claire-
ment que la leptine pourrait influencer le début de la puberté.
Il y a encore de nombreuses controverses sur le rôle puta-
tif de la leptine dans le contrôle de la puberté, et il est dif-
ficile de corréler les mécanismes complexes de la puberté
aux modifications de signaux isolés, notamment à celles
de la leptine. Il est déjà bien connu que la restriction calo-
rique retarde le début de la puberté et que la réalimenta-
tion abolit ce retard. De plus, les modèles animaux et les
patients atteints de déficience en leptine sont incapables
d’arriver à la puberté. Le traitement par leptine peut rétablir
la sécrétion pulsatile des gonadotrophines (31), caractéris-
tique de la phase précoce de la puberté. La souris femelle
transgénique skinny, qui représente un modèle in vivo
d’hyperleptinémie chronique en l’absence de tissu adi-
peux, arrive précocement à la puberté (16). Les données
sur l’effet de l’administration de leptine sur le début de
la puberté sont controversées. D’une part, il a été montré
que l’administration intracérébroventriculaire de leptine
prévenait le retard de l’ouverture vaginale induit par la

183
Métabolismes Hormones Diabètes et Nutrition (VIII), n° 4-5, juillet/octobre 2004
Mise au point
Mise au point
restriction calorique chronique chez le rat (17). En revanche,
dans un autre modèle, des taux artificiellement élevés de
leptine n’étaient pas suffisants pour abolir le retard du
déclenchement de la puberté dû à la restriction calorique
(32). Il reste aussi à savoir si la leptine agit comme un
facteur permissif (médiateur tonique), dont les concen-
trations au-dessus d’un seuil critique sont nécessaires
pour la puberté, ou plutôt comme un déclencheur (média-
teur phasique), qui détermine la crise pubertaire par une
hausse de sa concentration à un moment précis lors du
développement. La corrélation temporelle entre l’élévation
des concentrations de leptine et le début de la pulsatilité
de la LH pendant la puberté a été étudiée chez plusieurs
espèces. Chez l’homme, les taux de leptine augmentent
d’environ 50 % avant le début de la puberté et diminuent
ensuite jusqu’au niveau basal (33). Chez le singe, les don-
nées sont plus controversées. Plusieurs études ont montré
que les niveaux de leptine ne changent pas significative-
ment chez le singe Rhésus autour de la puberté. En
revanche, une étude conduite chez le singe castré a montré
une hausse des taux nocturnes de leptine juste avant
l’augmentation prépubertaire nocturne de la libération
pulsatile de LH, accompagnée par une augmentation noc-
turne importante de GH et de IGF-1 (34). Il n’est pas aisé
de déterminer si les deux signaux métaboliques agissent
de concert ou si l’un d’entre eux possède un rôle prédomi-
nant. Chez le rongeur, des études récentes ont montré que
les concentrations de leptine ne varient pas de façon majeure
au cours de la maturation sexuelle, ce qui suggère que la
leptine n’est pas le déclencheur principal de la puberté,
mais qu’elle y joue plutôt un rôle permissif (35).
Le dimorphisme sexuel des concentrations de leptine
devient évident après la puberté. Chez l’homme, les niveaux
de leptine augmentent pendant l’enfance, atteignent un pic
dans les phases précoces de la puberté pour décliner ensuite,
alors qu’ils augmentent de façon constante pendant la
maturation sexuelle chez la femme. Par conséquent, les
niveaux de leptine sont trois à quatre fois plus élevés chez
la femme que chez l’homme. Les raisons n’en sont pas
très claires. Chez l’homme, après la puberté, les taux de
testostérone et le volume testiculaire sont inversement
corrélés aux taux de leptine, tandis que chez la femme, après
ajustement à la masse grasse, les taux d’estradiol sont
directement corrélés aux niveaux de leptine (36). Ces
données indiquent que les androgènes et les estrogènes
pourraient expliquer, au moins en partie, les différences
de taux de leptine entre les deux sexes. Cette hypothèse
est aussi confortée par des études in vitro montrant que
les androgènes et les estrogènes inhibent et stimulent,
respectivement, l’expression et la libération de leptine
par les adipocytes humains en culture (37).
La puberté représente donc un moment critique dans le
dimorphisme sexuel concernant la relation entre l’axe HHG
et la leptine, les différences hormonales à l’âge mature
régulant de façon opposée la sécrétion de leptine dans les
deux sexes.
Leptine et stéroïdogenèse gonadique
Leptine et ovaire
L’identification récente du Ob-R dans différents tissus
périphériques (ovaire, testicule, surrénale) a suggéré que
la leptine pourrait influencer directement les cibles endo-
crines en aval de l’axe reproductif. Plusieurs études ont
été conduites sur l’ovaire, où l’expression du Ob-R est
abondante. Les études in vitro sur les cellules de la
thèque et de la granulosa ont montré que la leptine exerce
un effet négatif sur la production de stéroïdes ovariens,
chez les rongeurs et les bovins. En particulier, il a été
montré que la leptine :
✓
✓inhibe la production d’estradiol et de progestérone
induite par l’insuline dans des cellules isolées de la gra-
nulosa bovine (38) ;
✓
✓prévient la sécrétion de la progestérone et de l’andros-
tènedione dans des cellules isolées de la thèque bovine (39) ;
✓
✓empêche la libération de l’estradiol par les cellules de
la granulosa de rat en culture (40).
En accord avec ces données, il a été montré que l’incuba-
tion de cellules de la granulosa de femme fertile avec des
concentrations élevées de leptine (10-100 ng/ml) inhibait
significativement la sécrétion d’estradiol stimulée par la
FSH et l’IGF-1 (41). Ces observations indiquent que la
leptine, à des concentrations identiques à celles retrou-
vées chez les femmes obèses, peut interférer avec la pro-
duction d’estradiol par le follicule dominant in vivo, soit
directement, soit par la réduction des substrats androgé-
niques dérivés des cellules de la thèque. De plus, l’excès
de leptine pourrait altérer la réponse ovarienne aux stimuli
trophiques (pour exemple : IGF-1), produits par le follicule
dominant. Si des niveaux élevés de leptine interfèrent
avec le développement du follicule dominant, un stimu-
lus adéquat pour la sécrétion de la LH devient impossible,
et cela peut déterminer l’anovulation. À l’appui de cette
hypothèse, des études récentes ont montré que l’adminis-
tration in vivo de leptine à des rates immatures et l’expo-
sition in vitro des ovaires intacts à la leptine provoquent
un déclin important de la capacité d’ovulation (42). Globa-
lement, ces données pourraient expliquer l’incidence éle-
vée de dysfonctions reproductives ainsi que la reprise de
l’ovulation après perte de poids chez la patiente obèse.
Par ailleurs, des études plus récentes conduites chez la
rate montrent que Ob-R est aussi exprimé dans les ovo-
cytes, dans les cellules endothéliales et dans le corps
jaune. L’expression ovarienne de leptine et de Ob-R varie
et est régulée par les gonadotrophines pendant le cycle,
avec un pic d’expression pendant l’ovulation, indiquant un
rôle possible de la leptine dans différents aspects de la
fonction ovarienne, comme la maturation ovocytaire,
l’angiogenèse, la rupture folliculaire et la formation du
corps jaune (43).
L’hypothèse a été émise que la leptine puisse jouer un rôle
dans la physiopathologie du syndrome des ovaires poly-
 6
6
 7
7
 8
8
 9
9
 10
10
1
/
10
100%