Lire l'article complet

DOSSIER
La Lettre du Cardiologue - n° 332 - juin 2000
18
es connaissances sur les pathologies aiguës de l’aorte
thoracique ont beaucoup progressé (1, 2, 3, 4), parallè-
lement au développement des techniques d’imagerie :
échocardiographie transthoracique (ETT), transœsophagienne
(ETO), tomodensitométrie, imagerie par résonance magnétique,
si bien que la liste des pathologies aiguës détectables du vivant
du patient s’est élargie (tableau I, figure 1), même si la dissec-
tion aortique reste le drame thoracique le plus fréquent. Un dia-
gnostic précis et précoce est d’autant plus important qu’il sous-
tend une prise en charge thérapeutique appropriée.
Parmi les méthodes ultrasonores, l’échocardiographie transœso-
phagienne est sans conteste la technique la plus fiable dans le
diagnostic positif des pathologies aiguës de l’aorte. Certes, l’écho-
cardiographie transthoracique peut être suffisante pour confirmer
un diagnostic de dissection aiguë dans les cas les plus typiques
lorsque l’aorte ascendante est concernée ; cependant l’étude de
l’aorte thoracique descendante, du fait de la profondeur de la
structure dans le thorax, est essentiellement du ressort de l’ETO.
L’ETO a l’avantage d’être réalisable en service de cardiologie à
toute heure du jour et de la nuit au lit du malade. Rappelons tou-
tefois qu’il s’agit d’un examen semi-invasif qui nécessite une pré-
paration du patient toute particulière dans ces situations de sus-
picion de dissection aortique : parfait contrôle de la tension
artérielle, sédation. Soulignons par ailleurs l’importance d’un
opérateur entraîné compte tenu des pièges (artéfacts) et de cer-
taines lésions discrètes à rechercher avec attention.
DISSECTION AORTIQUE
Le diagnostic de dissection aortique (DA) en ETO répose sur
un signe direct essentiel (6, 7) : la mise en évidence du voile
intimal flottant séparant l’aorte en deux chenaux dont les régimes
circulatoires appréciés au doppler couleur sont différents
(figures 2, 3, 4).
Échocardiographie transœsophagienne
et aorte thoracique douloureuse
●R. Roudaut
L
Tableau I. Principales causes “d’aorte thoracique douloureuse”.
✔Dissection aortique
✔Hématome de paroi aortique
✔Ulcère athéromateux pénétrant
✔Fissuration
✔Rupture traumatique
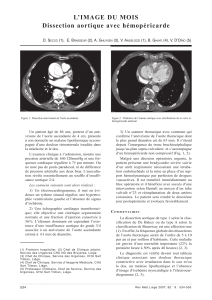
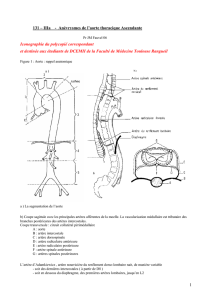
Figure 1. Représentation schématique des trois principaux diagnostics
différentiels : hématome de paroi, dissection aortique, ulcère athéroma-
teux pénétrant.
*Hôpital cardiologique, CHU, Bordeaux.
Figure 2. Dissection aortique, ETO multiplan à 115°. Flap intimal
dédoublant l’aorte ascendante, porte d’entrée située à la partie initiale de
la dissection.

Classiquement, le voile intimal flotte dans la lumière aortique et
peut être suivi sur plusieurs centimètres. La notion d’artéfacts de
réverbérations au niveau de l’aorte ascendante est particulière-
ment importante (8, 9).
Les artéfacts sont fréquents lorsque l’aorte ascendante est dila-
tée, ils correspondent à des échos de réflexion de structures très
réfléchissantes, comme le mur aortique postérieur.
Le diagnostic d’artéfact repose sur quatre éléments principaux :
l’artéfact est localisé, ses mouvements sont de faible amplitude
et strictement parallèles à ceux de la paroi aortique (d’amplitude
souvent double), l’artéfact est à une distance double par rapport
au capteur de la structure qui lui a donné naissance, enfin, le dop-
pler couleur ne met pas en évidence deux couloirs circulants fran-
chement différents (figure 5).
Certains signes indirects ou associés sont importants à recher-
cher en cas de dissection (6) :
✔La dilatation de l’aorte, quasi constante, mais de degré
variable ; une dilatation majeure de l’aorte ascendante représente
un critère de gravité.
✔Une insuffisance aortique, dont le mécanisme doit être pré-
cisé : atteinte valvulaire préexistante, dilatation de l’anneau, capo-
tage d’une sigmoïde du fait de sa désinsertion par l’hématome
disséquant, ou plus rarement prolapsus du voile intimal dans l’ori-
fice aortique en diastole.
✔Enfin, l’épanchement péricardique représente classiquement
un critère de gravité, car il peut témoigner d’une fissuration de
l’aorte ascendante.
Une fois le diagnostic de dissection posé, l’ETO doit en pré-
ciser la topographie et rechercher les portes d’entrée et de
réentrée. Les dissections de type A touchent l’aorte ascendante
et peuvent s’étendre à l’aorte horizontale, voire à l’aorte thora-
cique descendante. Dans la majorité des cas, la porte d’entrée
siège au niveau de l’aorte ascendante quelques centimètres au-
dessus des valves aortiques ; cependant elle peut siéger au niveau
de l’aorte horizontale, voire au niveau de l’isthme (dans ce cas,
l’aorte ascendante est disséquée de façon rétrograde : type III
rétrograde de De Backey).
En échocardiographie, la porte d’entrée apparaît sous forme d’un
trou à l’emporte-pièce au niveau de l’intima disséquée, dont les
berges sont souvent vibrantes. Le doppler couleur montre un jet
systolique en aliasing faisant communiquer vrai chenal et faux
chenal. Les orifices de réentrée sont distaux mais peuvent être
multiples, voire disséminés sur l’aorte.
À la lumière des travaux de la littérature (10-14), entre des mains
entraînées, la sensibilité de l’ETO dans le diagnostic du flap inti-
mal avoisine 98 % et la spécificité 96 %. Le diagnostic précis de
porte d’entrée peut être plus difficile, la sensibilité variant entre
49 et 100 %, mais il est facilité par les sondes multiplan.
Au moindre doute diagnostique, il est capital de compléter par
une autre technique d’imagerie, car la stratégie thérapeutique est
fonction de la topographie des lésions : chirurgie pour les dis-
sections localisées à l’aorte ascendante, traitement médical dans
les autres cas en l’absence de complications.
La Lettre du Cardiologue - n° 332 - juin 2000
19
DOSSIER
Figure 5. ETO : écho linéaire de réverbération au niveau d’une aorte
ascendante dilatée (réflexions des parois de l’artère pulmonaire).
Figure 4. Dissection aortique, même patient. ETO au niveau de l’aorte
isthmique : flap intimal flottant en TM.
Figure 3. Dissection aortique, même patient. ETO à 0° : dédoublement
de l’aorte ascendante.

Au total, le diagnostic de dissection aortique est une urgence
médico-chirurgicale qui a largement bénéficié des progrès dans
le diagnostic et le traitement. Si le pronostic reste particulière-
ment grave dans les dissections de type A, la chirurgie permet
aujourd’hui d’en diminuer notablement la mortalité. Soulignons
toutefois la nécessité de surveiller tous ces patients (opérés ou
non) du fait des risques d’évolution, en particulier anévrismale,
de l’aorte disséquée fragilisée. Cette surveillance doit être
annuelle et faire appel à une technique d’imagerie non invasive.
L’ HÉMATOME DE PAROI AORTIQUE
Il représente pour beaucoup d’auteurs une variante de la dissec-
tion puisque sur le plan anatomopathologique, l’hémorragie siège,
comme dans la dissection, à l’union 2/3 internes, 1/3 externe de
la média au niveau d’une zone de média nécrose kystique
(tableau II). Le tableau clinique est similaire. Cependant, à la
différence de la dissection, il n’y a pas de porte d’entrée ni de
faux chenal perméable (figures 6 et 7). Le terrain est habituelle-
ment celui d’un sujet plus âgé athéromateux. Enfin, cette patho-
logie est plus fréquente au niveau de l’aorte thoracique descen-
dante.
En échocardiographie transœsophagienne, le signe principal
est représenté par l’hématome de la paroi aortique qui
déforme celle-ci en croissant ou la dédouble. L’épaississement
doit, pour S. Mohr-Kahaly (15), être supérieur ou égal à 7 mm
pour être retenu ; le déplacement centro-luminal de calcifications
intimales aide au diagnostic différentiel avec un thrombus mural
sur aorte dilatée.
L’hématome a classiquement un aspect granité (plein). Cepen-
dant, il peut être hypoéchogène et réaliser un aspect kystique en
partie ou en totalité (liquéfaction de l’hématome).
Le diamètre de l’aorte est habituellement dilaté ; la lumière aor-
tique, en revanche, est peu déformée.
Soulignons l’intérêt d’autres techniques d’imagerie (16) lorsque
l’ETO est d’interprétation difficile : le scanner spiralé avec injec-
tion de produit de contraste et en faveur d’un épaississement de
paroi aortique sans opacification du “faux chenal” et sans porte
d’entrée. L’IRM surtout est très évocatrice lorsqu’elle montre un
épaississement de la paroi aortique avec hypersignal en T1 témoi-
gnant de la présence de sang frais.
L’évolution de l’hématome de paroi est souvent compliquée, mais
moins grave que la dissection (19). Selon von Kodolitsch (17), à
partir d’une compilation de 209 cas publiés dans la littérature, la
mortalité à 30 jours est de 24 %. L’hématome peut évoluer pré-
cocement vers une dissection dans 18 % des cas, vers une rup-
ture dans 15 % des cas. À noter cependant que l’hématome peut
se stabiliser, voire régresser ; par ailleurs, une évolution secon-
daire vers une ectasie de l’aorte est possible, d’où la nécessité
d’une surveillance régulière.
Le traitement de l’hématome de paroi reste controversé ;
schématiquement, une chirurgie est proposée lorsque l’aorte
ascendante est concernée, alors qu’un hématome non compliqué
de l’aorte thoracique descendante relève du traitement médical.
Cependant, certains auteurs (18) considèrent qu’il n’est pas utile
d’opérer systématiquement lorsque l’aorte ascendante est concer-
née et réservent la chirurgie aux situations suivantes : présence
d’un anévrisme de l’aorte ascendante, d’un épanchement péri-
cardique, d’un hémomédiastin, mais ceci est très discuté.
La Lettre du Cardiologue - n° 332 - juin 2000
20
DOSSIER
Figure 6. Hématome de paroi en croissant au niveau de l’aorte ascen-
dante. ETO multiplan, plan 12°.
Figure 7. Hématome de paroi, même patient. Le doppler couleur n’opa-
cifie pas l’hématome.
Tableau II. Principaux éléments distinctifs de la dissection de l’héma-
tome de paroi et de l’ulcère athéromateux pénétrant.
Dissection Hématome Ulcère
Définition Voile intimal Hématome Ulcération
Faux chenal pariétale
localisée
Athérosclérose Variable Variable Toujours
(souvent minime) sévère
Thrombus Possible si Hématome Hématome
faux “chenal souvent étendu localisé
thrombosé” possible
Extension lésion Souvent étendue Souvent étendue Localisée

L’ULCÈRE ATHÉROMATEUX PÉNÉTRANT
Il doit être redouté chez un patient âgé athéromateux, se plaignant
d’une douleur thoracique transfixiante mais sans image de dis-
section aortique à l’échocardiographie transœsophagienne.
L’ulcère athéromateux correspond à une perforation cratériforme
de la paroi aortique avec rupture de la limitante élastique interne
et extension dans la média. Cette pathologie prédomine au niveau
de l’aorte thoracique descendante (tableau II, voir page 00). Les
aspects échocardiographiques ont été bien décrits par Vilacosta
(20) à partir d’une série de 12 cas. Le cratère est habituellement
localisé ; il est rarement isolé puisque, dans sa série, il s’associe
à un anévrisme localisé de l’aorte deux fois et à une dissection
localisée trois fois (figure 8).
Par ailleurs, l’ulcère s’accompagne d’un petit hématome de paroi
deux fois et d’une image de faux anévrisme partiellement throm-
bosé deux fois. Les auteurs déplorent deux faux négatifs du fait
du site (aorte ascendante distale, aorte horizontale) et/ou de la
petite taille du cratère. En cas de doute diagnostique, ce qui n’est
pas rare du fait du caractère localisé de la lésion, il est capital de
faire appel à une autre technique d’imagerie : scanner spiralé,
IRM, voire aortographie, qui dans cette pathologie reste très utile
en montrant un aspect en bouton de chemise.
L’évolution de l’ulcère athéromateux perforant peut être
marquée par une rupture externe, ce qui en fait la gravité. Au
niveau de l’aorte ascendante, une indication chirurgicale sera
d’autant plus facile à décider que l’aorte est anévrismale ou dis-
crètement disséquée. En l’absence de fissuration, l’ulcère loca-
lisé à l’aorte thoracique descendante relève du traitement médi-
cal hypotenseur.
LA FISSURATION AORTIQUE
C’est une urgence chirurgicale de diagnostic difficile en dehors
des tableaux précités de dissection d’hématome ou de paroi d’ul-
cère athéromateux pénétrant.
La fissuration complique habituellement une aorte fragilisée, dila-
tée, atteinte par un processus dystrophique ou athéromateux (21,
22). Le diagnostic peut être évoqué en ETT lorsque l’anévrisme
siège au niveau de l’aorte ascendante. L’examen peut mettre en
évidence un aspect direct d’amincissement, de fissuration, de dila-
cération de la paroi, mais ceci est rare (figures 9 et 10). Dans ce
contexte, la présence d’un épanchement péricardique, a fortiori
d’un hématome péricardique, est très évocatrice. L’ETO et les
autres techniques d’imagerie peuvent apporter des arguments
décisifs. Cependant, face à l’urgence vitale extrême souvent
confirmée par la mise en évidence sur la radiographie thoracique
d’un hémothorax, voire d’un hémomédiastin, il ne faut pas tar-
der à prendre une décision opératoire lorsqu’elle est envisageable.
LA RUPTURE TRAUMATIQUE DE L’ISTHME AORTIQUE
Elle représente une complication classique des traumatismes de
la voie publique avec décélération brutale. Le pronostic initial est
sombre, d’autant plus que les patients sont souvent polytrauma-
tisés (20 % de décès dans les six premières heures).
La Lettre du Cardiologue - n° 332 - juin 2000
21
DOSSIER
Figure 8. Ulcère athéromateux pénétrant évoluant vers un faux anévris-
me partiellement thrombosé de l’aorte descendante. ETO à 100°.
Figure 9. Fissuration de l’aorte ascendante au niveau des sinus de
Valsalva. ETO 132°.
Figure 10. Fissuration du sinus de Valsalva, même patient. ETO 46°.

Dans ce contexte, l’ETT n’est d’aucun apport car elle est diffici-
lement réalisable chez un patient souvent intubé et ventilé. L’ETO
peut se justifier, mais bien souvent ces patients bénéficient dès
leur prise en charge d’un scanner corps entier pour réaliser un
bilan précis des lésions. La rupture siège habituellement à
l’isthme, zone soumise à des forces de cisaillement ; elle est clas-
siquement transversale et peut être totale, respectant uniquement
l’adventice, ou partielle, réalisant un faux anévrisme.
En cas de rupture totale, au niveau d’un isthme légèrement dilaté,
l’ETO met en évidence un dédoublement pariétal sous forme d’un
flap épais peu mobile. Le doppler couleur montre un léger alia-
sing sans double chenal vrai.
La rupture partielle constitue un aspect typique de faux anévrisme,
véritable poche accolée à l’aorte par un collet. Cette poche est
souvent partiellement thrombosée (figure 11).
Selon Vignon (23, 24), l’ETO peut être pris en défaut en cas de
déchirure très localisée (< 5 mm) (sensibilité 91 %, spécificité
100 %).
À noter dans l’étude de Vignon, qui porte sur 32 patients suspects
de rupture de l’isthme explorés en ETO, la mise en évidence de
3cas de simples déchirures intimales apparaissant sous forme
d’un fin liseré flottant dont le pronostic semble tout à fait favo-
rable.
CONCLUSION
Face à un grand syndrome douloureux thoracique évocateur de
dissection aortique, il faut savoir évoquer d’autres diagnostics
plus rares, qui posent des problèmes spécifiques.
L’ETO est un examen capital, surtout pour l’exploration de l’aorte
descendante. Au moindre doute, il est nécessaire d’étayer le dia-
gnostic par la réalisation d’autres examens complémentaires. ■
RÉFÉRENCES BIBLIOGRAPHIQUES
1. Wooley CF, Sparks EH, Boudoulas H. Aortic Pain. Prog Cardiovasc Dis 1998 ; 40,
6:563-89.
2. Fuster V, Halperin JL. Aortic dissection : a medical perspective. J Card Surg
1994 ; 9 : 713-28.
3. Roudaut R, Laffort P, Lafitte S, Sempé S, Durrieur-Jaïs C, Coste P. Place de
l’échocardiographie dans le diagnostic des maladies acquises de l’aorte thoracique.
Arch Mal Cœur 1997 ; 90 : 1687-92.
4. O’Gara PT, DeSanctis RW. Acute aortic dissection and its variants. Toward a
common diagnostic and therapeutic approach. Circulation 1995 ; 92, 6 : 1376-8.
5. Guéret P, Sénéchal C, Roudaut R et al. Comparison of transesophageal echocar-
diography in acute aortic dissection. A multicentric prospective study. J Am Coll
Cardiol 1991 ; 17 : 260A.
6. Bansal RC, Schmidt C, Shah PM. Transoesophageal echo in aortic dissection.
Cardiology 1991 : 71-87.
7. Armstrong WF, Bach DS, Carey L, Chen T, Donovan C, Falcone RA, Marcovitz
PA. Spectrum of acute dissection of the ascending aorta : a transesophageal echo-
cardiographic study. J Am Soc Echocardiogr 1996 ; 9 : 646-56.
8. Appelbe AF, Walker PG, Yeoh JK, Bonitatibus A, Yoganathan AP, Martin RP.
Clinical significance and origin of artefacts in transesophageal echocardiography of
the thoracic aorta. J Am Coll Cardiol 1993 ; 21 : 754-60.
9. Evangelista A, Garcia del Castillo H, Gonzalez-Alujas T, Dominguez-Oronoz R,
Salas A, Permanyer-Miralda G, Soler-Soler J. Diagnosis of ascending aortic dissec-
tion by transesophageal echocardiography : utility of M-Mode in recognizing arte-
facts. J Am Coll Cardiol 1996 ; 27 : 102-7.
10. Nienaber CA, Spielmann RP, von Kodolitsch Y, Siglow V, Piepho A, Jaup T,
Nicolas V, Weber P, Triebel HJ, Bleifeld W. Diagnosis of thoracic aortic dissection.
Magnetic resonance imaging versus transoesophageal echocardiography.
Circulation 1992 ; 85 : 434-47.
11. Nienaber CA, von Kodolitsch Y, Nicolas V, Siglow V, Piepho A, Brockhoff C,
Koschyk DH, Spielmann RP. The diagnosis of thoracic aortic dissection by noninva-
sive imaging procedures. N Engl J Med 1993 ; 328 : 1-9.
12. Cigarroa JE, Isselbacher EM, DeSanctis RW, Eagle KA. Diagnostic imaging in
the evaluation of suspected aortic dissection. N Engl J Med 1993 ; 328 : 35-43.
13. Laissy JP, Blanc F, Soyer Ph, Assayag P, Sibert A, Tebboune D, Arrivé L, Brochet
E, Hvass U, Langlois J, Menu Y. Thoracic aortic dissection : diagnosis with transe-
sophageal echocardiography versus MR imaging. Radiology 1995 ; 194 : 331-6.
14. Nishino M, Tanouchi J, Tanaka K, Aoyama T, Miyawaki M, Ito T, Kato J,
Morioka T, Hori M, Yamada Y, Abe H. Transesophageal echocardiographic diagno-
sis of thoracic aortic dissection with the completely thrombosed false lumen : diffe-
rentiation from true aortic aneurysm with mural thrombus. J Am Soc Echocardiogr
1996 ; 9 : 79-85.
15. Mohr-Kahaly S, Erbel R, Kearney P, Puth M, Meyer J. Aortic intramural hemor-
rhage visualized by transesophageal echocardiography : findings and prognostic
implications. J Am Coll Cardiol 1994 ; 23 : 658-64.
16. Nienaber CA, von Kodolitsch Y, Petersen B, Loose R, Helmchen U, Haverich A,
Spielmann RP. Intramural hemorrhage of the thoracic aorta. Diagnostic and thera-
peutic implications. Circulation 1995 ; 92 : 1465-72.
17. von Kodolitsch Y, Nienaber CA. Intramural hemorrhage of the thoracic aorta :
diagnosis, therapy and prognosis of 209 in vivo diagnosed cases.
Z Kardiol 1998 ; 87 : 797-807.
18. Kang DH, Song JK, Song MG, Lee IS, Song H, Lee JW, Park SW, Kim YH, Lim TH,
Park SJ. Clinical and echocardiographic outcomes of aortic intramural hemorrhage
compared with acute aortic dissection. Am J Cardiol 1998 ; 81 : 202-6.
19. Vilacosta I, San Roman JA, Ferreiros J, Aragoncillo P, Mendez R, Castillo JA,
Rollan MJ, Batlle E, Peral V, Sanchez-Harguindey L. Natural history and serial mor-
phology of aortic intramural hematoma : a novel variant of aortic dissection. Am
Heart J 1997 ; 134 : 495-507.
20. Vilacosta I, San Roman JA, Aragoncillo P, Ferreiros J, Mendez R, Graupner C,
Batlle E, Serrano J, Pinto A, Oyonarte JM. Penetrating atherosclerotic aortic ulcer :
documentation by transesophageal echocardiography. J Am Coll Cardiol 1998 ; 32 :
83-9.
21. Svensson LG, Labib SB, Eisenhauer AC, Butterly JR. Intimal tear without hema-
toma. An important variant of aortic dissection that can elude current imaging tech-
niques. Circulation 1999 ; 99 : 1331-6.
22. Al Moussarih A, Lorillard R, Andrivet JC, Deville C, Roudaut R. Rupture spon-
tanée de l’aorte ascendante : une urgence diagnostique et thérapeutique.
À propos de 2 cas. Arch Mal Cœur 1998 ; 91 : 257-61.
23. Vignon P, Guéret P, Vedinne M et al. Role of transoesophageal echocardiography
in the diagnosis and management of traumatic aortic disruption. Circulation 1995 ;
92 : 2959-68.
24. Vignon P, Lang R. Use of transoesophageal echocardiography for the assessment
of traumatic aortic injuries. Echocardiography 1999 ; 16 : 207-19.
La Lettre du Cardiologue - n° 332 - juin 2000
22
DOSSIER
Figure 11. Rupture traumatique partielle de l’isthme aortique. Aspect de
faux anévrisme en ETO.
1
/
5
100%