Oncogériatrie : actualités doSSiEr tHÉMatiQUE Geriatric oncology: what’s new in the management

Réussi
Évaluation gériatrique
spécialisée nécessaire
Sujets
fragiles
Pathologiques,
connés
Usuel
IAD*
* Instrumental activity of daily living (1).
0
20-30 %
= gériatrie
10-15 %50-60 %15-20 %
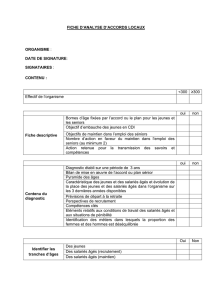
Figure 1. Répartition des sujets âgés en fonction du type de vieillissement.
La Lettre de l’Hépato-gastroentérologue • Vol. XI - n° 4 - juillet-août 2008 | 145
DOSSIER THÉMATIQUE
Oncogériatrie :
actualités
Geriatric oncology: what’s new in the management
of the elderly patient?
É. Boucher*
* Service d’oncologie médicale, centre
Eugène-Marquis, Rennes.
L’oncogériatrie en 2007
Quoi de neuf en oncologie du sujet âgé ? Vraisem-
blablement une évolution vers l’individualisation
de l’oncogériatrie en tant que partie de l’oncologie
générale, au même titre que l’oncologie pédiatrique.
Nombreux ont été les essais thérapeutiques destinés
aux sujets âgés, et nombreuses les publications. J’ai
recensé plus de 2 000 articles publiés en 2007 et
plus de 100 abstracts à l’ASCO 2007 !
Pour reprendre la citation de l’éditorial du dernier
bulletin des réseaux en cancérologie : “Oncogériatrie :
l’âgisme
1
est dépassé”, la pathologie cancéreuse
du sujet âgé est en passe de devenir une discipline
“d’avenir” ; du moins les traitements spécifiques
du cancer sont de plus en plus proposés aux sujets
âgés, et ce n’est qu’un début. Quelques chiffres :
la classe d’âge des plus de 65 ans est celle qui
connaîtra la plus forte croissance démographique
au cours des prochaines années. Elle représentera,
en 2030, 25 % des Européens. En Europe, 800 décès
sur 1 000 surviennent après 65 ans dont 200 sont
liés au cancer. Trente-cinq pour cent des cancers
diagnostiqués le sont chez des personnes âgées de
plus de 75 ans, et 10 % chez des personnes âgées
de plus de 85 ans. On peut considérer les cancers
dont l’incidence connaît un pic autour de 65-70 ans
pour diminuer après (cancer du sein, cancer du
poumon), et ceux dont l’incidence augmente régu-
lièrement avec l’âge (cancer colorectal, cancer de
la prostate). Si après 70 ans les cancers sont plus
fréquents, la probabilité de mortalité spécifique par
cancer diminue en raison de l’association aux autres
pathologies et à leurs morbidités spécifiques. La
survie relative à 5 ans chez un patient âgé de plus
de 75 ans atteint d’un cancer reste inférieure à celle
d’un adulte traité pour la même pathologie (41 %
chez les femmes, 35 % chez les hommes).
Avant de soigner un sujet âgé il faut connaître l’espé-
rance de vie de sa classe d’âge, et garder en mémoire
que si l’âge est une des données, le vieillissement
en est une autre. Les trajectoires de vieillissement
des individus sont différentes (figure 1).
Il faut savoir demander une évaluation gériatrique,
évaluation gériatrique standard (EGS) ou évalua-
tion gériatrique approfondie (EGA), pour les sujets
fragiles, afin de pouvoir adapter la thérapeutique.
Cette évaluation spécialisée permet d’obtenir un
score classant les personnes en trois catégories
principales : pleine forme, intermédiaire, fragile.
Elle comprend de nombreux items :
évaluation sociale ; ➤
nombre de médicaments pris au quotidien ; ➤
nombre de comorbidités ; ➤
1 Discrimination négative liée à l’âge.
Mots-clés
Oncogériatrie
Patients âgés
Keywords
Geriatric oncology
Elderly

Pleine forme
Autonome
Pas de comorbidité
Traitements standards
Fragile
Dépendant
> 3 comorbidités
Soins de confort
Intermédiaire
1 dépendance fonctionnelle
1-3 comorbidités
Cancer < espérance de vie < cancer
Traitement adapté
Évaluation gériatrique
Figure 2. Organigramme de la décision thérapeutique en fonction de l’évaluation gériatrique.
146 | La Lettre de l’Hépato-gastroentérologue • Vol. XI - n° 4 - juillet-août 2008
Oncogériatrie : actualités
DOSSIER THÉMATIQUE
Journée de la FFCD
état nutritionnel (
➤
mini nutritional assessment
[MNA]) ;
mini mental state examination ➤ (MMSE) ;
mini geriatric depression scale ➤ (MGDS) ;
station unipodale ; ➤
évaluation des capacités sensorielles ; ➤
évaluation de l’autonomie. ➤
Cette évaluation permettra d’adapter le traitement
individuellement (figure 2).
Les axes de réflexion actuels en oncogériatrie sont,
entre autres :
dans le cadre du plan cancer, la création d’unités
➤
pilotes de coordination ;
des propositions d’essais thérapeutiques dédiés ➤
ouverts aux patients âgés de plus de 75 ans ;
la validation de scores de toxicité des traitements
➤
oncologiques chez le sujet âgé (essai PAC GERICO
07/0705, coordonné par F. Pein, de Nantes) ;
une révision progressive de la limite d’âge pour ➤
les dépistages organisés.
Apports de la littérature
de l’année 2007 à l’exercice
quotidien de la cancérologie
du sujet âgé : quels traitements,
pour quels bénéfices
et avec quels risques (2-3) ?
En cancérologie digestive, la moyenne d’âge des
patients inclus dans les essais thérapeutiques est
de 62 ans ; or, l’âge moyen de survenue d’un cancer
digestif est de 72 ans. La population évaluée n’est
donc pas celle qui reçoit le traitement, il y a un
décalage entre la théorie et ce que d’aucuns appel-
lent la “vraie vie”.
De nombreuses questions se posent dans le cadre
de l’exercice quotidien de la cancérologie du sujet
âgé.
Quels sont les patients “à risque” pour les trai- ➤
tements spécifiques ?
Les formes évoluées doivent-elles être traitées
➤
par une monothérapie ou par une polychimiothé-
rapie ?
Quel dosage proposer, la dose doit-elle être
➤
réduite d’emblée ?
Quelles sont la place et la morbidité de la radio-
➤
thérapie ?
Quelle est la morbidité de la chirurgie ? ➤
À quel âge l’administration du traitement adju-
➤
vant doit-elle cesser ?
La littérature de 2007 apporte quelques réponses
pertinentes à ces questions. Notons que la majorité
des études a concerné les cancers colorectaux.
Quels sont les patients à risque
pour un traitement oncologique ?
L’évaluation gériatrique n’est pas un score “cancé-
rologique”. Il est nécessaire de valider des scores
de toxicité des traitements oncologiques chez le
sujet âgé. Une étude parue à l’ASCO en 2007 (4) a
inclus sur 3 ans 364 patients atteints d’un cancer
métastatique ou localement évolué, un tiers d’entre
eux présentant une tumeur digestive. Elle avait
pour objectif de juger la faisabilité d’une coopéra-

La Lettre de l’Hépato-gastroentérologue • Vol. XI - n° 4 - juillet-août 2008 | 147
DOSSIER THÉMATIQUE
tion entre oncologues et gériatres sur une région
donnée et sur 14 centres, une évaluation gériatrique
étant réalisée chez tous les patients inclus, ainsi que
d’identifier des facteurs de risque de décès avant
6 mois. Les auteurs ont réussi à inclure rapidement
les patients, et ont identifié en analyse multivariée
deux principaux facteurs de risque de décès précoce :
le stade tumoral (odds-ratio [OR] : 4,2) et le score
nutritionnel bas (OR : 4,5). Ils ont aussi remarqué
que seuls 20 % des patients avaient une fonction
rénale normale et que 30 % avaient un bon état
nutritionnel. L’essai PAC GERICO 07/0705, en cours,
a pour objectif la validation prospective d’un index
prédictif de toxicité propre à chaque patient : le score
CRASH (chemotherapy risk assessment score high age
patients) [EGA + MAX2]. Ce score offre une vision du
risque global de toxicité EGA (évaluation gériatrique
approfondie) et MAX2 (variable spécifique liée à la
toxicité connue et publiée de la chimiothérapie),
permettant une prédiction de la toxicité grave/sévère
de la chimiothérapie chez le patient âgé.
Traitement adjuvant des cancers
du côlon chez le sujet âgé :
faut-il systématiquement réaliser
un traitement adjuvant chez un patient
âgé de plus de 70 ans opéré d’un cancer
du côlon (5-7) ?
Il faut tenir compte de la mortalité du traitement
(0,5 %), de sa morbidité (9 à 25 % d’effets indési-
rables de grade 3-4), de son bénéfice relatif sur la
survie sans maladie et sur la survie globale, ainsi que
de l’espérance de vie du patient (tableau).
Tableau. Espérance de vie en années en fonction de l’âge.
Âge Pleine forme Intermédiaire Fragile
65 ans 20 18,5 9,7
70 ans 15,8 14,8 8,6
75 ans 12,1 11,5 7,3
80 ans 8,8 8,4 5,9
Les patients âgés de plus de 70 ans sont sous-
représentés dans les essais thérapeutiques où ils
ne constituent que 19 % des effectifs. Dans les
études de registres, ils représentent près de 35 %
des patients traités. La cardiopathie (OR : 0,5), la
broncho- pneumopathie chronique obstructive
(BPCO) et le diabète (OR : 0,8) sont les principales
comorbidités qui freinent la réalisation d’un traite-
ment adjuvant.
Le bénéfice d’un traitement adjuvant, en termes de
diminution du taux de récidive, est-il fonction :
de l’âge ?
➤
Le débat est ouvert, et il est difficile
de répondre à cette question. Il semble que non.
Cependant, aucune étude portant sur les patients
âgés de plus de 70-75 ans n’a été réalisée. Dans la
littérature, les quelques éléments de réponse sont
discordants ;
de la durée du traitement ?
➤
Une étude obser-
vationnelle menée sur 3 700 patients âgés de plus
de 65 ans, opérés d’un cancer colique de stade III
et traités entre 1993 et 1999 par une chimiothé-
rapie par 5-FU, fait état de 30 % d’arrêts précoces
du traitement, dont 38 % concernent des patients
âgés de 75 à 79 ans et 52 % des patients âgés de plus
de 80 ans. Les auteurs constatent que, si la durée
de traitement est inférieure à 4 mois, il n’y a pas de
bénéfice du traitement sur la survie sans récidive par
rapport à l’abstention thérapeutique ;
du type de traitement proposé ?
➤
Les mono-
chimiothérapies sont équivalentes, cependant
la capécitabine est moins bien tolérée chez les
patients âgés de plus de 70 ans. L’analyse par sous-
groupe ne montre pas de bénéfice de la bithérapie
(capécitabine/5-FU-oxaliplatine) chez les patients
âgés de plus de 65 ans ;
du stade ?
➤
L’étude anglaise QASAR a inclus
3 239 patients opérés d’un cancer colique de stade II,
dont 20 % de patients âgés de plus de 70 ans. Les
auteurs concluent à un bénéfice du traitement adju-
vant pour les stades II (hazard-ratio [HR] : 0,82),
mais non pour les patients âgés de plus de 70 ans
(HR : 1,13).
Traitement des cancers
du côlon métastatique (8-10)
Une étude randomisée de grande envergure
présentée en juin à l’ASCO, l’étude factorielle 2x2
FOCUS, évaluait le bénéfice tumoral et le bénéfice
sur la qualité de vie de la capécitabine orale versus
le 5-FU en perfusion continue ainsi que l’addition
d’oxaliplatine. Les quatre traitements suivants
étaient possibles : schéma LV5-FU2 simplifié avec
ou sans oxaliplatine (FOLFOX-4, 85 mg/m²), et
capécitabine (J1-J14) avec ou sans oxaliplatine
(CAPOX, 100 mg/m²). Les traitements étaient
commencés systématiquement à 80 % de la dose
et augmentés à 100 % de la dose si la tolérance
était bonne après 12 semaines de thérapie. Tous
les patients ont bénéficié d’une évaluation géria-
trique. Cent quinze patients ont été randomisés

148 | La Lettre de l’Hépato-gastroentérologue • Vol. XI - n° 4 - juillet-août 2008
DOSSIER THÉMATIQUE
Journée de la FFCD Oncogériatrie : actualités
dans chaque groupe (5-FU/capécitabine, FOLFOX/
CAPOX). L’âge moyen était de 75 ans (73-79 ans).
La dose initiale diminuée a permis de maîtriser
la toxicité. Les taux de réponse aux traitements
étaient semblables à ceux des autres études (15 %
pour les monothérapies et 40 % pour les bithé-
rapies), mais les taux de survie sans progression
(3,7 à 5,4 mois) et de survie globale (9 à 12 mois)
étaient significativement plus faibles que chez les
sujets plus jeunes. Cinquante pour cent des patients
traités en monothérapie ont continué le traitement
à pleine dose après 12 semaines, versus seulement
30 % des patients recevant de l’oxaliplatine. La
capécitabine n’a pas amélioré de façon significative
la qualité de vie, et a induit plus de cas de toxicité
digestive et cutanée que le 5-FU. L’addition d’oxali-
platine a augmenté le taux de réponse par rapport
au 5-FU seul et amélioré la survie sans maladie et
la survie globale, mais de façon non significative
(p = 0,06). Le taux de toxicité de grade 3/4 n’était
pas supérieur à celui observé avec le FU seul, mais
les cas de toxicité digestive et neurologique étaient
plus nombreux. La médiane de survie était iden-
tique pour tous les groupes de traitement. Une
étude prospective de phase II a évalué le béné-
fice du tégafur-uracile chez 58 patients d’un âge
moyen de 81 ans, OMS 0/1. Le taux de réponse a
été de 22 %, la survie médiane de 13 mois, et la
survie sans progression de 4,6 mois. Il y a eu 55 %
de cas de toxicité de grade 3/4, essentiellement
digestive, surtout chez les plus âgés.
Une analyse rétrospective portant sur 3 742 patients
(dont 614 âgés de plus de 70 ans) recevant dans le
cadre de 4 essais thérapeutiques un traitement adju-
vant, de première et seconde ligne a constaté que les
patients plus âgés ont eu plus d’effets indésirables
hématologiques, mais non digestifs ni neurologiques.
En revanche, le bénéfice sur la réponse, la survie sans
progression et la survie globale étaient identique
quel que soit l’âge.
Traitement des cancers du rectum :
impact de la radiothérapie préopératoire
et de l’exérèse du mésorectum (11)
Une étude rétrospective néerlandaise a été effectuée
à partir des données du Rectal cancer databases of
the Comprehensive Cancer Centres (4 567 patients,
dont 28 % – 358 âgés de plus de 75 ans) et de celles
d’un essai prospectif, la TME (total mesorectal exci-
sion) study (1 356 patients, dont 17 % – 230 âgés de
plus de 75 ans). Le but était d’étudier l’impact de
la radiothérapie préopératoire et de la chirurgie du
mésorectum sur trois périodes différentes :
période 1, 1990-1995, avant la généralisation
➤
de ces pratiques ;
période 2, 1996-1999, pendant leur mise en
➤
place ;
période 3, 2000-2002, après leur généra-
➤
lisation.
Deux groupes de patients, les patients âgés de plus
de 75 ans et les patients âgés de moins de 75 ans,
ont été individualisés. Le taux de récidives locoré-
gionales entre les périodes 1 et 3 est passé de 11 %
à 5,2 % chez les patients âgés de moins de 75 ans,
et de 14 % à 5,5 % chez les patients âgés de plus
de 75 ans.
La radiothérapie préopératoire et la chirurgie du
mésorectum ont permis une amélioration de la
survie à 5 ans chez les patients de moins de 75 ans :
de 60 % (1990-1995) à 67 % (1996-1999) et 70 %
(2000-2002) [log-rank p < 0,0001]. Les patients
plus âgés n’ont pas eu ce bénéfice (respectivement
41 %, 40 % et 43 % à 5 ans). La radiothérapie préo-
pératoire et la chirurgie du mésorectum ont été
responsables d’une augmentation de la mortalité
à 30 jours (4,8 % lors de la période 1 versus 7,8 %
au cours des périodes 2-3), mais non de la morta-
lité à 6 mois (14 % versus 16 %). La conclusion de
cette étude est le paradoxe suivant : il existe une
amélioration en termes de récidive locorégionale
et de survie spécifique grâce à l’amélioration des
traitements, mais au prix d’une augmentation des
complications. Le risque relatif de décès spécifiques
est de 1,6 chez le sujet âgé versus 5,2 chez le sujet
jeune. Le traitement n’entraîne pas de bénéfice sur
la survie globale.
Chirurgie du cancer gastrique
chez le sujet âgé (12)
Le but de cette étude était d’identifier des facteurs
influençant la morbidité, la mortalité, la qualité de
vie et la survie des patients âgés de plus de 75 ans
après chirurgie gastrique. De janvier 1993 à
décembre 2004, 135 patients ont été opérés, parmi
lesquels 94 (69,6 %) bénéficiaient d’une chirurgie
curative. Ce groupe a été apparié à 71 patients plus
jeunes. Le nombre de comorbidités et le statut
nutritionnel de départ différaient d’un groupe à
l’autre. Les procédures chirurgicales ont été iden-
tiques. La morbidité était de 27,9 %, et la morta-
lité de 8,5 %. Le nombre des comorbidités était le
seul facteur qui influençait la mortalité. La survie

DOSSIER THÉMATIQUE
à 5 ans était de 56,2 % chez les patients plus âgés
versus 62,1 % chez les autres. Seul le stade tumoral
influençait la survie. La qualité de vie postopératoire
était identique dans les deux groupes. Le pronostic
fonctionnel des patients âgés était meilleur en cas
de gastrectomie partielle qu’en cas de gastrectomie
totale.
Radio-chimiothérapie
des cancers de l’œsophage (13)
Une comparaison rétrospective de l’efficacité et
de la toxicité de la radio-chimiothérapie chez les
patients âgés a été effectuée. Trente-trois patients
âgés de plus de 70 ans ont été appariés sur le stade
tumoral à 145 patients âgés de moins de 70 ans. Le
traitement consistait en l’association 5-FU continu/
cisplatine + radiothérapie 50/60 Gy. Les résultats
ont été les suivants : taux de réponse complète iden-
tique (63,6 % versus 63,4 %), taux de récidive après
réponse complète supérieur (47,6 % versus 33,7 %,
p = 0,32), médiane de survie inférieure (14,7 mois
versus 35,1 mois, p = 0,01), réduction de dose ou
interruption de la radiothérapie (57,6 % versus
17,3 %, p = 0,01), taux d’effet indésirable hémato-
logique supérieur, nombre de décès non liés à la
maladie équivalent.
Conclusion
Si les données de la littérature sont nombreuses,
pour les cancers digestifs, la plupart sont rétros-
pectives ou des données de cohortes. Même si elles
peuvent orienter, elles ne peuvent constituer un
standard. Il existe quelques essais de phase II, mais
ceux de phase III sont rares. Les taux de réponse
ne semblent pas altérés avec l’âge ; en revanche,
les données de survie sont moins bonnes que chez
l’adulte plus jeune. La toxicité est généralement
supérieure. Il faut savoir demander une évaluation
gériatrique pour un patient âgé de plus de 75 ans.
Le temps que demande cette évaluation est certai-
nement très inférieur à la durée de l’hospitalisation
que nécessiterait la survenue d’une toxicité. ■
1. Graf C. The lawton instrumental activities of daily living
scale. Am J Nurs 2008;108(4):52-62.
2. Handler SM, Hanlon JT, Perera S et al. Consensus list of
signals to detect potential adverse drug reactions in nursing
homes. J Am Geriatr Soc 2008: [Epub ahead of print].
3. Prince-Paul M. Relationships among communicative acts,
social well-being, and spiritual well-being on the quality
of life at the end of life in patients with cancer enrolled in
hospice. J Palliat Med 2008;11(1):20-5.
4. Soubeyran P, Rainfray M, Mathoulin-Pélissier S et al. Scree-
ning of elderly patients with cancer for early death risk; result of
a prospective multicentric study of 364 patients under chemo-
therapy. J Clin Oncol 2007;25(Suppl. 18):abstract 9040.
5. Labianca R. The role of adjuvant chemotherapy in colon
cancer. Surg Oncol 2007;16(Suppl. 1):S93-6.
6. Bradley CJ. Adjuvant chemotherapy after resection in
elderly medicare and medicaid patients with colon cancer.
Arch Intern Med 2008;168(5):521-9.
7. Quasar Collaborative Group. Adjuvant chemothe-
rapy versus observation in patients with colorectal
cancer: a randomized study. Lancet 2007;370(9604):
2020-9.
8. Seymour MT, Maughan TS, Wasan HS et al. Capecitabine
(Cap) and oxaliplatin (Ox) in elderly and/or frail patients
with metastatic colorectal cancer: the FOCUS2 trial. J Clin
Oncol 2007;25(Suppl. 18):abstract 9030.
9. Hochster HS, Luo W, Popa EC et al. Phase II study of
uracil-tegafur with leucovorin in elderly (> or = 75 years
old) patients with colorectal cancer: ECOG 1299. J Clin
Oncol 2007;25(34):5397-402.
10. Goldberg RM, Tabah-Fis I, Bleiberg H et al. Pooled
analysis of safety and efficacy of oxaliplatin plus fluo-
rouracil/leucovorin administered bimonthly in elderly
patients with colorectal cancer. J Clin Oncol 2006;24(25):
4085-91.
11. Rutten H, den Dulk M, Lemmens V et al. Survival of elderly
rectal cancer patients not improved: analysis of population
based data on the impact of TME surgery. Eur J Cancer 2007;
43(15):2295-300.
12. Pisanu A. Curative surgery for gastric cancer in the
elderly: treatment decisions, surgical morbidity, mortality,
prognosis and quality of life. Tumori 2007;93(5):478-84.
13. Takeuchi S, Ohtsu A, Doi T et al. A retrospective study
of definitive chemoradiotherapy for elderly patients with
esophageal cancer. Am J Clin Oncol 2007;30(6):607-11.
Références bibliographiques
Journées d’Hépato-Gastro Entérologie
Organisateurs :
J. Cosnes, R. Poupon
Informations et inscriptions :
www.b-c-a.fr/hgsa08
Bloc-notes
Paris (Maison de la Chimie - 28, rue Saint-Dominique), les 14 et 15 novembre 2008
1
/
5
100%