P É

ÉDITORIAL
203
La Lettre du Cancérologue - Volume XII - no6 - novembre-décembre 2003
P
our les patientes atteintes de cancer du sein, la fin de
l’année est porteuse d’espoir. Des progrès marquants sont
constatés sur tous les fronts.
✓En hormonothérapie. L’anastrozole (antiaromatase) confirme
son impact en situation précoce.
Chez les patientes ménopausées, RE+, dont la maladie aurait
nécessité une mastectomie, l’étude IMPACT démontre qu’un
traitement conservateur est possible dans près de la moitié des
cas grâce à de l’anastrozole délivré en traitement d’induction.
En adjuvant :
– L’administration d’anastrozole après deux ans de tamoxifène
apporte manifestement un bénéfice clinique par rapport à la pour-
suite du tamoxifène seul.
– L’administration de létrazole après cinq ans de tamoxifène
entraîne une diminution significative du risque de rechute.
✓En chimiothérapie. En situation néoadjuvante, l’adjonction
séquentielle de Taxotere®aux anthracyclines apporte un gain
manifeste de temps jusqu’à progression et en survie.
En situation métastatique, l’utilisation d’une combinaison TAC
(T pour Taxotere®) semble permettre une augmentation significa-
tive de la survie par rapport au FAC avec un gain absolu de 6 %
(81 % à 87 %), soit une augmentation relative de 30 % de la sur-
vie. Cela devrait concerner plus de 1 000 patientes par an en France.
✓En radiothérapie. L’irradiation partielle pourrait amener une
réduction de la toxicité potentielle de la radiothérapie, même si
celle-ci est très faible, avec les techniques actuelles utilisées en
routine. Il peut y avoir un avantage dans les associations avec la
chimiothérapie.
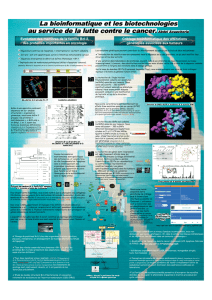
De nouveaux concepts voient le jour
Comme, par exemple, celui des cellules souches du cancer du sein.
Grâce à un modèle expérimental de cellules mammaires humaines
cultivées en surfaces non adhérentes, les “mammosphères”,
l’équipe de l’université du Michigan développe l’hypothèse selon
laquelle des cellules souches ou leurs descendantes immédiates
seraient les cibles initiales de la transformation cancéreuse. Les
thérapeutiques actuelles ne tueraient que des cellules tumorales
plus ou moins différenciées, laissant intactes ces cellules souches
tumorales sources de résistance et de rechute. Ce concept pour-
rait avoir un impact sur de nouvelles stratégies thérapeutiques,
d’autant qu’il semble possible d’identifier le phénotype particu-
lier CD44+, CD24- /low, ESA+ lineage de ces cellules.
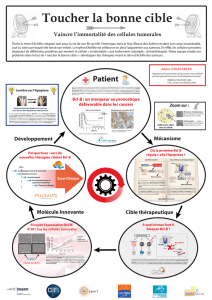
De nouvelles voies thérapeutiques semblent s’ouvrir
dans un avenir prochain
Les thérapeutiques classiques du cancer se sont intéressées jusqu’à
présent au blocage de la prolifération cellulaire. Une autre voie
intéressante pourrait être d’aiguiller les cellules tumorales
“immortalisées” dans la voie de la mort naturelle (apoptose).
Dans le déclenchement de cette apoptose, trois voies semblent
essentielles :
✓la voie de la mitochondrie régulée par la protéine antiapop-
totique Bcl-2 ;
✓la voie du récepteur de la famille TNF (death receptors) ;
✓la voie commune.
Plusieurs stratégies semblent possibles afin de bloquer Bcl-2, la pre-
mière voie : petites molécules antagonistes ciblant la protéine (étude
préclinique) ; oligonucléotides antisens ciblant l’ARNm (essai cli-
nique) ; régulateurs transcriptionnels ciblant le gène.
Parmi ces nouvelles molécules, plusieurs semblent pouvoir
interagir physiquement avec la protéine Bcl-2 au niveau de
trois poches critiques. Le gossypol, molécule issue de la méde-
cine chinoise naturelle, est capable d’induire l’apoptose de cel-
lules tumorales in vitro. Elle a une activité antitumorale dans
des modèles de tumeurs xénogreffées et est actuellement testée
en essai clinique de phase I. Les polyphénols naturels issus du
thé vert ou noir semblent aussi développer des propriétés anti-
cancéreuses in vitro. Leur mécanisme d’action est inconnu.
Leur effet de chimioprévention pourrait être dû à leur activité
anti-Bcl-2. Pour la voie du récepteur de mort : TRAIL (Apo2-
ligand) est un membre de la famille du TNF. Il induit l’apop-
tose de certaines cellules tumorales et peut aussi les sensibiliser
à la chimiothérapie. Il ne semble pas exister de toxicité dans
les études cliniques. TRAIL est requis pour l’activité antitumo-
rale médiée par les cellules NK.
Enfin, pour la troisième voie, les antagonistes IAP semblent induire
une apoptose dans une grande variété de lignes tumorales, et être
plus actifs contre les cellules tumorales que contre les cellules nor-
males. Ces antagonistes peuvent aussi sensibiliser les cellules
tumorales à la chimiothérapie et aux agents biologiques tels que
TRAIL. Ces molécules ont une puissante activité sur les modèles
de tumeurs xénogreffés, et sont bien tolérées chez les rongeurs.
Tous ces progrès majeurs devraient avoir un impact sur la pra-
tique oncologique quotidienne de demain.
Des envoyés de La Lettre du Cancérologue
à San Antonio, États-Unis
Breast Cancer Symposium (San Antonio)
Des progrès… en léger différé
1
/
1
100%