COMMENT JE TRAITE … une hypoglycémie grave chez un patient diabétique

Rev Med Liege 2003; 58 : 3 : 119-122
I
NTRODUCTION
L’ h ypoglycémie représente la complication
métabolique la plus fréquente chez le patient
diabétique et son incidence pourrait encore aug-
menter avec l’insulinothérapie intensive (1). Les
malaises hypoglycémiques, bien ressentis et pas-
sant rapidement au resucrage, sont communs
chez le patient diabétique de type 1 et représen-
tent souvent le prix à payer pour obtenir un bon
contrôle métabolique au long cours (hémoglo-
bine glyquée ou HbA1c < 7,0 %, voire idéale-
ment < 6,5 % pour une valeur normale entre 4 et
6 %). Ils sont plus rares chez le patient diabé-
tique de type 2 caractérisé par une obésité et une
insulinorésistance. L’hypoglycémie sévère est
heureusement plus rare, mais par définition plus
grave. Elle est classiquement définie comme une
hypoglycémie qui nécessite l’intervention d’une
tierce personne pour aider le patient diabétique à
s’en sortir, soit en l’aidant au resucrage oral, soit
en injectant du glucagon par voie sous-cutanée
ou intramusculaire ou encore du glucose par
voie intraveineuse (2). Selon le rapport du
Groupe d’Etude EURODIAB consacré au dia-
bète de type 1, la proportion de patients avec au
moins une hypoglycémie sévère par an est en
moyenne de 32 %, avec une valeur minimale de
12 % dans un centre et une valeur maximale de
48 % dans un autre centre (3). Son incidence est
estimée entre 0,1 et 1,2 épisodes par patient et
par an chez les patients diabétiques traités par
pompe à perfusion continue sous-cutanée d’in-
suline (4).
L’ h ypoglycémie résulte d’un taux circulant
d’insuline anormalement élevé par rapport à la
glycémie ambiante (2). Cette insuline circulante
provient soit d’une injection chez le patient insu-
linotraité (type 1 insulinodépendant ou type 2
insulinorequérant), soit de la stimulation exagérée
de la sécrétion insulinique endogène par un médi-
cament insulinosécrétagogue, le plus souvent un
sulfamide hypoglycémiant (sulfonylurée), plus
rarement le répaglinide. L’analyse de la littérature
et l’expérience clinique révèlent que le risque
d’hypoglycémie est très faible chez les patients
diabétiques traités par metformine, glitazones ou
inhibiteurs des alpha-glucosidases intestinales,
sauf si ces médicaments sont pris en association
avec l’insuline ou un sulfamide (4). Les causes
d’hypoglycémie peuvent être multiples. La plu-
part du temps, cependant, les hypoglycémies
résultent de l’injection d’insuline ou de l’inges-
tion d’une sulfonylurée à la dose habituelle alors
que le patient a pris un repas apportant trop peu
de glucides et/ou a pratiqué un exercice physique
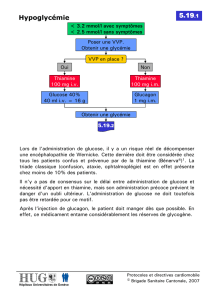
plus important que d’habitude (fig. 1).
L’ h ypoglycémie s’accompagne généralement
de signes d’alarme induits par la stimulation sym-
pathique, à savoir sensation de fringale, suda-
(1) Assistant, (2) Professeur, Université de Liège,
Chef de Service, Service de Diabétologie, Nutrition et
Maladies métaboliques et Service de Médecine interne
générale, Département de Médecine.
COMMENT JE TRAITE …
une hypoglycémie grave chez un patient diabétique
RÉSUMÉ : Les hypoglycémies sévères sont définies par la néces-
sité d’une intervention d’une tierce personne et peuvent aller jus-
qu’au coma profond. Elles peuvent survenir chez le patient traité
par insuline, généralement pour un diabète de type 1,ou chez le
patient traité par sulfamide, pour un diabète de type 2. Le dia-
gnostic est souvent évident, au moins chez le patient insulino-
traité, et doit amener une intervention urgente de la part de
l’entourage. Celle-ci doit comprendre un resucrage oral si l’état
de conscience le permet ou, à défaut, l’injection de glucagon. Si
nécessaire, l’entourage doit faire appel à un médecin qui fera une
injection intraveineuse de glucose hypertonique. Le coma hypo-
glycémique lié à un surdosage absolu ou relatif en insuline
devrait, dans la plupart des cas, pouvoir être traité à domicile. Au
contraire, le coma induit par un surdosage en sulfamide impose
toujours une hospitalisation pour assurer une surveillance adé-
quate et mettre en route une perfusion intraveineuse prolongée
de glucose. Il est indispensable que l’entourage de tout sujet à
risque d’hypoglycémie reçoive l’éducation adéquate pour pou-
voir appliquer promptement et correctement le meilleur traite-
ment susceptible de permettre au patient diabétique de récupérer
rapidement et sans séquelle d’un éventuel coma hypoglycémique.
H
OW
I
TREAT
…
ASEVERE HYPOGLYCAEMIA
IN A DIABETIC PATIENT
SUMMARY : Severe hypoglycaemic episodes are defined as need
of assistance and may progress to profound coma. They can
occur in patients treated with insulin, generally for type 1 dia-
betes, or in patients receiving sulphonylureas, for type 2 dia-
betes. Diagnosis is usually obvious, at least in insulin-treated
patients, and requires an urgent intervention from the entourage.
Such an intervention should comprise the oral administration of
carbohydrates with high-glycaemic index if consciousness allows
it or, if not, the injection of glucagon. When necessary, people
should ask the help of a physician who will inject hypertonic glu-
cose intravenously. Hypoglycaemic coma related to an absolute
or relative excess of insulin should, in most cases, be treated at
home. In contrast, a hypoglycaemic coma due to a too high
dosage of sulphonylurea always requests a hospitalisation in
order to carefully supervise the patient and to provide a prolon-
ged intravenous infusion of glucose. It is mandatory that family
or entourage members of any diabetic patient at risk to develop
severe hyoglycaemia receive a specific education in order to
promptly apply the best treatment capable of a rapid and safe
recovery from hypoglycaemic coma.
K
EYWORDS
: Diabetes mellitus - Glucagon - Hypoglycaemia –
Insulin – Sulphonylurea
R.P. R
ADERMECKER
(1), J.C. P
HILIPS
(1), A.J. S
CHEEN
(2)
119

tions, palpitations, tremblement, … (2). Ces
signes peuvent cependant être absents chez cer-
tains patients diabétiques, ou passer inaperçus, ou
encore être trop fugaces pour permettre une
réponse appropriée de la part du patient. Des
signes de neuroglucopénie peuvent alors appa-
raître (lenteur d’idéation, diplopie, troubles de la
conscience, …), qui peuvent conduire le patient
au coma. Contrairement au coma hyperglycé-
mique qui survient lentement, en quelques
heures, le coma hypoglycémique survient brutale-
ment, en quelques minutes. Outre cette cinétique
d’installation différente, les deux comas se diffé-
rencient aussi par quelques signes cliniques assez
caractéristiques : respiration de Kussmaul, dou-
leurs abdominales et vomissements dans le coma
acidocétosique, agitation, contractures muscu-
laires, parfois crises convulsives dans le coma
hypoglycémique. Le coma hypoglycémique est
rarement mortel et le patient finit généralement
par récupérer, suite à l’élimination progressive de
l’insuline ou du sufamide et suite à l’action des
divers processus de contre-régulation. Néan-
moins, il est important de le diagnostiquer aussi
rapidement que possible pour mettre en route le
traitement approprié et limiter le risque de
séquelles, neurologiques notamment.
Le but du traitement est de rétablir aussi rapi-
dement que possible un état de conscience normal
(traitement d’urgence), d’éviter une rechute
rapide de l’hypoglycémie (traitement de consoli-
dation) et de prévenir une récidive de l’accident
(traitement de prévention). Les moyens de pré-
vention des accidents hypoglycémiques chez le
patient diabétique de type 1, de loin le plus
exposé, seront explicités dans un prochain article
(5). La présente mise au point rappelle les moda-
lités de prise en charge d’une hypoglycémie
grave, non pas par le patient diabétique qui est
incapable de réagir à ce moment, mais bien par
l’entourage, qu’il soit médical ou non. Par souci
de clarté, nous envisagerons séparément le traite-
ment d’un patient diabétique traité par insuline et
celui d’un patient traité par sulfamide.
H
YPOGLYCÉMIE CHEZ UN PATIENT TRAITÉ
PAR INSULINE
Le traitement d’un coma hypoglycémique lié
à un surdosage absolu ou relatif en insuline
repose sur trois modalités qui ont chacune leur
spécificité : le resucrage oral, l’injection de glu-
cagon et l’administration de glucose par voie
intraveineuse. Dans toute la mesure du possible,
le traitement sera fait à domicile, sans hospitali-
ser le patient, sauf circonstances particulières
aggravantes.
Si le patient est encore suffisamment
conscient pour ingurgiter une boisson ou des ali-
ments sans risque de fausse route, il convient de
privilégier le resucrage par voie orale. Il est
généralement conseillé d’administrer l’équiva-
lent de 10 à 20 g de glucose. L’administration
peut se faire sous forme solide, généralement 2
à 4 morceaux de saccharose ou mieux de “Dex-
troenergen”, plus facile à administrer et fondant
rapidement au contact de la muqueuse buccale.
Généralement, cependant, la forme “solution”
sera préférée, avec administration de boisson
sucrée (100 à 200 ml, par exemple de limonade
ou de “coca cola”). Le retour a la conscience
sera consolidé par la prise d’un aliment conte-
nant des sucres à résorption plus lente. La diffi-
culté consiste souvent à ne pas tomber dans le
piège d’un resucrage excessif qui conduira à une
hyperglycémie importante et prolongée. Il faut
cependant savoir que l’hyperglycémie suivant le
resucrage ne résulte pas seulement de celui-ci;
le rebond hyperglycémique post-hypoglycé-
mique (appelé aussi effet Somogyi) s’explique
également par la riposte tardive des hormones de
la contre-régulation. Aussi, même si le resucrage
est raisonnable, une hyperglycémie secondaire
est souvent difficile à éviter et l’entourage ne
doit pas s’en culpabiliser outre mesure.
Si le patient en est coma, le risque de fausse
route est trop important et le resucrage oral forcé
sera évité. Il conviendra alors que l’entourage
recoure à une injection de glucagon par voie sous-
cutanée ou par voie intramusculaire (6). Tous les
patients diabétiques traités par insuline, à tout le
moins tous les sujets avec un diabète de type 1,
devraient recevoir une prescription de glucagon et
l’entourage immédiat devrait recevoir l’éducation
minimale pour pouvoir se servir utilement de ce
médicament aux propriétés salvatrices. Un entraî-
R.P. RADERMECKER ET COLL.
Rev Med Liege; 58 : 3 : 119-122
120
Fig. 1. Représentation schématique de la régulation de la glycémie
avec les principaux mécanismes expliquant la survenue d’une hypo-
glycémie grave (en haut à droite) et les solutions pour assurer une
récupération rapide (en bas à gauche).

nement préalable est d’autant plus important que
le coma hypoglycémique, a fortiori s’il est
accompagné d’agitation et de convulsions, est
une situation particulièrement stressante pour
l’entourage, ce qui risque de faire perdre pas mal
de moyens à la tierce personne susceptible d’ap-
porter l’aide indispensable. Le glucagon est une
hormone qui exerce une puissante stimulation de
la glycogénolyse hépatique et de la gluconéoge-
nèse, deux voies biochimiques qui augmentent la
production de glucose par le foie (fig. 1). Cette
action est extrêmement rapide, permettant une
augmentation de la glycémie de 20-40 mg/dl dans
les 10-20 minutes suivant l’injection de 1 mg de
glucagon, ce qui permet généralement le retour à
un état de conscience quasi normal. Néanmoins,
cette action est relativement fugace (maximum 1
- 1,5 heures) de telle sorte qu’il convient de
consolider l’effet du glucagon par un resucrage
oral de consolidation (20 g de glucides dès que
l’état de conscience le permet). Cette charge per-
mettra de rétablir un stock suffisant de glycogène
hépatique et évitera de voir le patient récidiver
son hypoglycémie 1 à 2 heures plus tard. Le glu-
cagon est maintenant fabriqué par génie géné-
tique, tout comme l’insuline, et présenté sous une
forme quasi prête à l’emploi (Glucagen®Hypokit,
Novo Nordisk, 1 mg) (fig. 2). Il faut savoir que
l’injection de glucagon peut donner lieu, chez
certains patients, à des vomissements importants
(le glucagon est connu pour donner une sidération
du transit gastro-intestinal, raison pour laquelle
cette hormone est d’ailleurs parfois utilisée en
imagerie digestive). Chez les sujets qui tolèrent
mal le glucagon sur le plan digestif, il peut être
conseillé d’injecter une demi-ampoule et de n’in-
jecter l’autre moitié que si la première est insuffi-
sante et ne permet pas de récupérer un état de
conscience suffisant pour permettre un resucrage
oral de consolidation.
Enfin, si on ne dispose pas de glucagon ou si le
glucagon ne permet pas une restauration suffi-
sante de l’état de conscience, la seule solution sera
de recourir à l’administration de glucose par voie
intraveineuse. En pratique, ce traitement ne
pourra être administré que par un médecin, soit le
médecin traitant appelé d’urgence à domicile, soit
le médecin urgentiste du SMUR ou au service
d’urgences. Le médecin sollicité utilisera du glu-
cose hypertonique et injectera environ 20 à 50 ml
à 30-50 %, de façon à administrer de l’ordre de 10
à 25 g de glucose en bolus intraveineux (la dose
recommandée chez l’enfant est d’environ 0,5 g de
glucose par kilo de poids). Si nécessaire, un relais
sera pris par la mise en place d’une perfusion de
glucosé à 5 ou 10 % durant quelques heures. La
récupération est rapide dans l’immense majorité
des cas. Dans le cas contraire, une hospitalisation
devra être envisagée. Si le patient reste en coma,
il faut suspecter une lésion secondaire cérébrale
(notamment chez le patient âgé) et un scanner
cérébral devra être programmé dès que possible. Il
pourra s’avérer utile d’administrer des corticoïdes
de façon à limiter l’œdème cérébral : par exemple,
injection intraveineuse de fortes doses d’hydro-
cortisone (100 mg toutes les 4 heures) ou de
méthylprednisolone (40 mg toutes les 6 heures). Il
est évident que le pronostic est alors réservé.
H
YPOGLYCÉMIE CHEZ UN PATIENT TRAITÉ
PAR SULFAMIDE
Les sulfamides hypoglycémiants stimulent la
sécrétion d’insuline par les cellules B des îlots de
Langerhans de façon pharmacologique et non
physiologique. En fermant directement les
canaux potassiques, ils favorisent l’exocytose de
l’insuline alors même que la concentration plas-
matique de glucose est déjà basse. Les hypogly-
cémies qui en résultent sont généralement
prolongées en raison de la demi-vie souvent de
plusieurs heures de ces médicaments dont cer-
tains ont, par ailleurs, des métabolites actifs et/ou
pénètrent à l’intérieur de la cellule B. Ainsi,
contrairement à ce que l’on pourrait penser de
premier abord, les comas hypoglycémiques
induits par des sulfamides sont plus graves que
ceux induits par l’insuline et requièrent toujours
une hospitalisation pour optimaliser la prise en
charge sur une durée suffisante. Ils surviennent,
en général, chez des sujets plus âgés, fragiles sur
le plan cardiologique et surtout neurologique, de
telle sorte que les séquelles sont souvent plus
importantes. Les hypoglycémies induites par les
sulfamides peuvent être favorisées, comme pour
celles sous insuline, par le saut d’un repas ou par
la pratique d’une activité physique intense.
COMMENT JE TRAITE...
Rev Med Liege; 58 : 3 : 119-122 121
Fig. 2. Illustration du Glucagen®Hypokit, à utiliser par l’entourage
en cas de coma hypoglycémique ne permettant plus le resucrage oral.

D’autres causes sont plus spécifiquement d’ordre
pharmacocinétique, comme une insuffisance
rénale retardant l’élimination de la sulfonylurée
ou de son métabolite actif ou encore une interac-
tion médicamenteuse par une molécule à forte
liaison aux protéines susceptible de déplacer la
sulfonylurée et d’augmenter sa fraction libre
active (7). Les hypoglycémies induites par les sul-
famides sont d’autant plus dangereuses qu’elles
concernent des molécules avec longue demi-vie
(chlorpropamide) ou avec métabolites actifs (gli-
benclamide) ou qu’elles surviennent chez des
patients âgés, souffrant d’autres pathologies
notamment vasculaires (patients coronariens ou
avec ischémie cérébrale) (8). Un des avantages
des nouveaux insulinosécrétagogues de la famille
des glinides (répaglinide, le seul commercialisé
en Belgique) consiste en un moindre risque d’hy-
poglycémie grave en raison d’une demi-vie extrê-
mement courte (environ 1 heure) et d’une
influence négligeable de l’insuffisance rénale sur
la pharmacocinétique du produit (9).
L’ h ypoglycémie induite par un sulfamide ne
sera pas traitée par l’administration de glucagon,
contrairement à celle provoquée par l’insuline
(4, 6). En effet, l’effet du glucagon sera trop
fugace par comparaison à la durée d’action de la
sulfonylurée. De plus, le glucagon risquerait de
stimuler la sécrétion endogène d’insuline dès
que la glycémie remonte. En cas de coma empê-
chant le resucrage oral, la seule solution consis-
tera donc en l’injection intraveineuse de glucose.
Une autre différence essentielle réside, en
effet, dans le fait que le coma, suite à un surdo-
sage absolu ou relatif en sulfamide, est habituel-
lement beaucoup plus prolongé que le coma
secondaire à l’injection d’insuline. L’insuline a
une demi-vie relativement courte (sauf pour les
préparations retard) alors que le sulfamide a une
demi-vie plasmatique qui peut atteindre 6-12
heures et une demi-vie biologique encore plus
importante. Ainsi, alors que le coma hypoglycé-
mique insulinique est, dans la plupart des cas,
rapidement réversible, le coma sur sulfamide
peut être caractérisé par des épisodes de résur-
gence durant les premières 24 à 48 heures. Dès
lors, il est habituellement conseillé de maintenir
le patient hospitalisé sous une perfusion intra-
veineuse d’une solution de glucosé à 5 ou 10 %
après la phase initiale de resucrage avec du glu-
cosé hypertonique en bolus intraveineux et de
n’autoriser la sortie de l’hôpital qu’après 48
heures de surveillance.
C
ONCLUSION
L’ h ypoglycémie sévère chez un patient diabé-
tique insulinotraité n’est pas rare et demande
l’instauration d’un traitement d’urgence. Celui-
ci doit être administré, si possible par l’entou-
rage immédiat qui doit avoir reçu l’éducation
minimale indispensable. Cette dernière vise à
reconnaître l’accident hypoglycémique et à
appliquer le traitement le plus approprié, soit
l’administration orale d’une solution riche en
glucides à index glycémique élevé, soit l’injec-
tion de glucagon. Si nécessaire, il sera fait appel
à un médecin qui, dans la plupart des cas, fera
une injection intraveineuse d’une solution de
glucosé hypertonique. Rapidement diagnosti-
quée, l’hypoglycémie, même apparemment
grave, est toujours rapidement réversible, habi-
tuellement en quelques minutes, et sans
séquelle. Les hypoglycémies secondaires à la
prise de sulfamide nécessitent une prise en
charge spécifique et, en cas de coma, une sur-
veillance plus prolongée à l’hôpital, avec une
perfusion de glucose pendant environ 48 heures.
Enfin, tout accident hypoglycémique doit faire
l’objet d’une enquêt minutieuse à la recherche
de la cause puis, si nécessaire, d’un ajustement
thérapeutique pour prévenir toute récidive.
R
ÉFÉRENCES
1. Selam J.L.— Réévaluation du risque hypoglycémique au
cours de l’insulinothérapie intensive. In : Journées de
Diabétologie de l’Hôtel-Dieu, Flammarion, Médecine-
Sciences, Paris, 1998.
2. Cryer PE, Fisher JN, Shamoon H.— Hypoglycemia
(Technical Review). Diabetes Care, 1994, 17, 734-755.
3. The EURODIAB IDDM Complications Study Group.—
Microvascular and acute complications in IDDM
patients: the EURODIAB IDDM complications study.
Diabetologia, 1994, 37, 278-285.
4. Lefèbvre PJ, Scheen AJ.— Hypoglycemia. In : Ellenberg
and Rifkin's Diabetes mellitus : Theory and Practice.
(Fifth Ed.) (H. Rifkin, D. Porte Jr., eds), Elsevier, New
York-Amsterdam-London, 1997, 1307-1327.
5. Radermecker RP, Jandrain B, Paquot N, Scheen AJ.—
Prévention des hypoglycémies chez le patient diabétique
de type 1. Rev Med Liège, 2003, 58, sous presse.
6. Pollack CV Jr.— Utility of glucagon in the emergency
department. J Emerg Med, 1993, 11, 195-205.
7. Scheen AJ, Lefèbvre PJ.— Antihyperglycaemic agents.
Drug interactions of clinical importance. Drug Safety,
1995, 12, 32-45.
8. Stahl M, Berger W.— Sulfonylurées : pharmacologie et
risque hypoglycémique. In : Journées de Diabétologie de
l’Hôtel-Dieu, Flammarion, Médecine-Sciences, Paris,
1995, 107-119.
9. Scheen AJ.— Le répaglinide (NovoNorm®). Rev Med
Liège, 2001, 56, 456-459.
R.P. RADERMECKER ET COLL.
Rev Med Liege; 58 : 3 : 119-122
122
Les demandes de tirés à part sont à adresser au Pr.
A.J. Scheen, Service de Diabétologie, CHU Sart Til-
man, 4000 Liège.
1
/
4
100%