Lire l'article complet

134 | La Lettre de l’Hépato-gastroentérologue • Vol. XIV - n° 3 - mai-juin 2011
PROCTOLOGIE
Traitement
des condylomes anaux
Agnès Senéjoux*
* Institut de proctologie Léopold-
Bellan, groupe hospitalier Paris
Saint-Joseph.
L
es condylomes ano-génitaux sont liés à l’infec-
tion par les virus des papillomes humains (HPV).
Plus de 120 génotypes viraux ont été identifi és.
Parmi ces génotypes, VPH 6 et VPH 11 sont à l’ori-
gine de 90 % des condylomes ano-génitaux et d’une
partie des dysplasies de bas grade. Les génotypes 16
et 18 sont oncogènes et à l’origine de 80 à 90 % (1)
des cancers de l’anus et de 70 % des cancers du col
utérin. L’infection à HPV est la maladie sexuellement
transmissible ayant l’incidence la plus élevée. Le plus
souvent asymptomatique elle survient précocement
au cours de la vie sexuelle : 60 % des femmes sont
ainsi contaminées par les HPV 5 ans après leurs
premiers rapports (2) et 10 % de la population sera
atteinte de condylomes au cours de sa vie sexuelle
(3). Un travail utilisant un modèle mathématique
a estimé que 80 % des femmes de plus de 50 ans
ayant une vie sexuelle active ont été infectées par
HPV (4). L’histoire naturelle de l’infection à HPV a été
mieux étudiée au niveau du tractus génital féminin
qu’au niveau du canal anal : au bout de 18 mois, le
génome viral est indétectable chez 80 % des femmes
infectées (5). La clairance de HPV 16 est plus lente
que celle des autres génotypes (6). La persistance de
l’infection à un HPV oncogène est le facteur de risque
le plus important de progression vers des lésions
malignes. Vingt pour cent des hommes et 25 à 40 %
des femmes âgées de moins de 25 ans sont porteurs
sains du virus (7, 8). La prévalence des manifestations
cliniques liées à HPV est moindre, estimée à 1 % de la
population sexuellement active (9). Chez l’homme,
dans une étude brésilienne, l’incidence mensuelle de
l’infection génitale à HPV était de 38/1 000, la clai-
rance des génotypes oncogènes était moins rapide
en cas de partenaires multiples et inversement liée
à l’âge du malade (10).
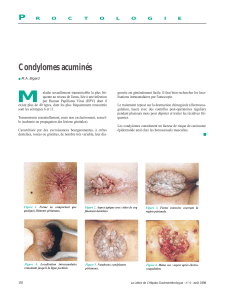
Le diagnostic des condylomes est en règle clinique
(fi gure 1). Le traitement des condylomes de l’anus
est parfois diffi cile et désespérant compte tenu de
la fréquence des récidives qui varie, selon les trai-
tements et les séries, de 30 à 70 %. La découverte
de condylomes de la marge implique la réalisation
systématique d’une anuscopie : la méconnaissance
de lésions endocanalaires est source de récidive. Un
bilan sérologique recherchera une infection sexuel-
lement transmissible associée. Il faut en particulier
déterminer le statut immunitaire concernant le VIH :
l’immunosuppression favorisant les récidives, les
réactivations virales et la survenue d’une dysplasie.
Chez les malades VIH+, le rôle bénéfi que des théra-
pies antirétrovirales demeure néanmoins contro-
versé. Chez les patients sous immunosuppresseurs
une diminution du traitement est parfois à envisager.
Chez les malades VIH+ ayant des condylomes, les
prélèvements histologiques sont systématiques dès
le diagnostic à la recherche d’une néoplasie intra-
épithéliale, le risque variant, selon les travaux, de
40 à 60 %. Ces prélèvements peuvent être orientés
par l’aspect des lésions, les zones suspectes étant
des zones blanchâtres, érythémateuses ou pigmen-
tées, discrètement en relief, voire érosives (fi gure 2).
Cependant, aucun aspect clinique n’est vraiment
spécifi que et le diagnostic peut n’être qu’histolo-
gique. L’application locale d’acide acétique à 3 %
Figure 1. Condylomes anaux.

La Lettre de l’Hépato-gastroentérologue • Vol. XIV - n° 3 - mai-juin 2011 | 135
PROCTOLOGIE
ou de lugol couplée à la colposcopie anale (ou
anuscopie haute résolution) permet de cibler les
prélèvements, mais cette méthode n’est que peu
diffusée en France. Certains proposent la réalisation
d’une cytologie anale par analogie au dépistage du
cancer du col utérin.
Chez les femmes, la réalisation d’un examen gynéco-
logique avec frottis cervico-vaginal doit être systé-
matique. Il a deux buts distincts : celui de rechercher
des lésions condylomateuses synchrones du tractus
génital d’une part, et celui d’analyser le degré de
dysplasie au niveau du col utérin, d’autre part. En
raison du nombre important de faux négatifs des
frottis cervico-vaginaux chez la patiente VIH+ et du
risque accru de dysplasie du col dans cette popula-
tion, certains auteurs conseillent la pratique systé-
matique d’une colposcopie.
Traitement préventif
L’incidence élevée des lésions dysplasiques et cancé-
reuses du col utérin a été initialement le principal
moteur des recherches sur la vaccination HPV.
Il est en effet montré qu’en vaccinant les jeunes
fi lles contre les HPV 16 et 18, l’incidence des lésions
dysplasiques précancéreuses diminue dans la popu-
lation vaccinée (11). Il existe actuellement 2 vaccins
commercialisés : un vaccin bivalent protégeant
contre les HPV oncogènes 16 et 18 et un vaccin
quadrivalent actif également sur HPV 6 et 11, les
2 génotypes les plus fréquemment à l’origine des
condylomes ano-génitaux. La recommandation
actuelle est de vacciner à l’âge de 14 ans, ou entre
15 et 26 ans pour les fi lles qui n’auraient pas eu de
rapports sexuels et au plus tard dans la première
année suivant les premiers rapports. En dépit de
ces recommandations la couverture vaccinale reste
insuffi sante : en 2008, seules 37 % des jeunes fi lles
éligibles étaient vaccinées aux États-Unis.
Chez les garçons, une récente publication a montré
que le vaccin quadrivalent prévient aussi 90 % des
condylomes ano-génitaux (12).
Traitement curatif
Idéalement, le traitement des condylomes devrait
éradiquer l’infection virale, en supprimer les symp-
tômes, en prévenir les conséquences à long terme
et enrayer la transmission du virus. Malheureuse-
ment, les traitements actuels n’ont pas d’action sur
la guérison de l’infection virale elle-même, leur seul
but étant la disparition des lésions macroscopiques.
Traitement physique
Le traitement habituel des condylomatoses exo- et
endocanalaires reste le plus souvent un traitement
physique. L’électrocoagulation au bistouri élec-
trique est largement utilisée. Selon l’importance
des lésions, elle peut être réalisée en consultation
sous anesthésie locale ou nécessiter une anesthésie
générale ou locorégionale. L’effi cacité de ce traite-
ment était évaluée dans des séries anciennes entre
61 et 94 % (9) avec des taux de récidive variant
beaucoup dans la littérature (de 9 à 66 %) [13, 14].
Deux essais randomisés ont montré une meilleure
effi cacité de ce type de traitement à court terme par
comparaison avec l’application locale d’azote liquide
ou avec la cryothérapie (15, 16). Ce dernier traite-
ment, qui consiste à appliquer de l’azote liquide à
– 196° au niveau des lésions, ne nécessite pas d’anes-
thésie, mais il est diffi cilement utilisable en pratique
lorsqu’il existe de nombreuses lésions canalaires.
La vaporisation laser (CO
2
ou YAG) n’est pas plus
Figure 2. Condylomes avec dysplasie de haut grade.

136 | La Lettre de l’Hépato-gastroentérologue • Vol. XIV - n° 3 - mai-juin 2011
PROCTOLOGIE
effi cace que l’électrocoagulation (17-19) : les taux
de récidives varient entre 60 à 77 % (9). Il s’agit, en
revanche, d’une technique plus coûteuse. Elle peut
enfi n imposer de travailler avec des systèmes d’aspi-
ration équipés de fi ltres ou, au mieux, de travailler
sous hotte aspirante afi n de limiter d’éventuelles
contaminations de l’opérateur par des particules
virales en suspension dans les fumées émises.
Quelle que soit la technique physique employée,
les douleurs anales peuvent être importantes en
postopératoire lorsque les lésions à traiter sont
extensives et endocanalaires.
Traitement chimique
L’imiquimod est un immunomodulateur utilisé en
application topique modulant l’activité des macro-
phages et des cellules dendritiques et augmentant la
production locale d’interféron et de cytokines pro-
infl ammatoires. La réponse clinique à l’imiquimod
s’accompagne d’une diminution quantitative des
ADN de HPV et des ARN messagers codant pour
les protéines virales. En application locale triheb-
domadaire de crème à 5 % pendant 16 semaines,
ce produit a une effi cacité estimée à 50 % dans une
méta-analyse avec des récidives dans 20 % des cas
(20). La tolérance locale est médiocre chez 20 % des
malades avec l’apparition d’un érythème modéré à
sévère avec sensations de brûlures, voire d’érosions,
conduisant à espacer les applications (fi gure 3).
Actuellement commercialisé en France sous forme
de crème, ce produit n’a pas d’AMM pour les lésions
muqueuses mais certains ont testé des suppositoires
contenant ce produit, voire la crème elle-même, pour
diminuer les récidives des condylomes après exci-
sion chirurgicale : de bons résultats et une tolérance
correcte ont ainsi été obtenus. L’application d’imi-
quimod après traitement physique initial pourrait
réduire les récidives (21).
La podophylline est un agent cytotoxique extrait,
détruisant les cellules au contact après applica-
tion. La podophyllotoxine en est la forme purifi ée.
Comparativement à l’excision aux ciseaux, ce trai-
tement était moins effi cace dans 2 essais rando-
misés (22, 23). Les effets indésirables locaux pouvant
être sévères (ulcérations douloureuses), ce produit
est inutilisable au niveau du canal anal. Une étude
récente a néanmoins montré que l’effi cacité et la
tolérance de ce traitement étaient comparables à
celles de l’imiquimod (24).
L’acide trichloracétique en solution (60 à 90 %) est
un agent caustique proposé pour le traitement des
condylomes ano-génitaux. Une effi cacité variant de
70 à 81 % après 6 applications et un taux de récidive
de 36 % sont rapportés dans la littérature (9).
L’interféron (α ou β) a été proposé pour traiter les
condylomes soit par voie générale soit par injection
intralésionnelle. La première voie d’administration
pose le problème de la tolérance générale, avec la
survenue d’un syndrome pseudo-grippal, alors que
la voie locale peut entraîner des douleurs au point
d’injection. Ce type de traitement est en fait très
peu utilisé.
Le cidofovir est un agent antiviral inhibant les poly-
mérases de l’ADN viral. Bien qu’il soit non spéci-
fi que du HPV, un essai randomisé contre placebo
suggère son effi cacité en application topique (49 %
de réponses dans le groupe traité versus 0 % pour
le groupe placebo) [25].
La vaccination thérapeutique contre les virus HPV ne
fait pour l’instant que l’objet de recherches cliniques,
et notamment dans le champ du traitement des
lésions dysplasiques viro-induites.
Figure 3. Dermite caustique liée à l’application d’imiquimod.

La Lettre de l’Hépato-gastroentérologue • Vol. XIV - n° 3 - mai-juin 2011 | 137
PROCTOLOGIE
Surveillance
Globalement, le taux de récidive quelle que soit
la technique utilisée, est important et varie de
30 à 70 %. Il est influencé par le statut immu-
nitaire du malade. Une surveillance clinique
(examen proctologique) est donc nécessaire : le
rythme idéal des consultations n’est cependant
pas défini dans la littérature. Il paraît licite de
proposer des examens proctologiques initia-
lement répétés mensuellement, puis avec une
fréquence adaptée à l’importance des récidives
pendant environ 1 an. Le but de ces contrôles est
de dépister une récidive des condylomes à un
stade précoce, accessible à un traitement sous
anesthésie locale en consultation. Le ou les parte-
naires sexuels doivent être dépistés et traités. Le
patient doit être averti qu’il est potentiellement
contagieux même en l’absence de lésion visible
tant que plusieurs contrôles négatifs n’ont pas
été réalisés. Il faut également l’informer que le
préservatif ne protège qu’à 70 % de cette infection,
le virus étant très résistant dans la nature et la
contamination pouvant être indirecte.
Le dépistage des lésions dysplasiques dans la popula-
tion à risque est également un des objectifs du suivi
des malades. Ses modalités ne sont pas défi nies : il
est parfois proposé un examen proctologique et/ou
un frottis anal annuel pour certains, complété par
un examen au colposcope (anuscopie haute réso-
lution). Ce dépistage doit être poursuivi même si
les condylomes sont éradiqués sur le plan clinique.
Conclusion
En attendant une éventuelle modifi cation de l’épi-
démiologie de l’infection à HPV secondaire à l’in-
troduction de la vaccination (dont les modalités
d’application sont d’ailleurs susceptibles d’évoluer :
vaccination des garçons ?), le traitement des condy-
lomes utilise encore souvent des méthodes physiques,
aidées cependant par l’application d’imiquimod, qui
permet de limiter les récidives en plus de son action
immunomodulatrice. La surveillance des patients
est importante, en particulier chez le malade infecté
par le VIH, compte tenu du risque de survenue d’une
dysplasie, voire d’un cancer anal. ■
1. Daling JR, Madeleine MM, Johnson LG et al. Human papil-
lomavirus, smoking, and sexual practices in the etiology of
anal cancer. Cancer 2004;101(2):270-80.
2. Woodman CB, Collins S, Winter H et al. Natural history of
cervical human papillomavirus infection in young women: a
longitudinal cohort study. Lancet 2001;357(9271):1831-6.
3. Munk C, Svare EI, Poll P, Bock JE, Kjaer SK. History of
genital warts in 10,838 women 20 to 29 years of age
from the general population. Risk factors and associa-
tion with Papanicolaou smear history. Sex Transm Dis
1997;24(10):567-72.
4. Myers ER, McCrory DC, Nanda K, Bastian L, Matchar DB.
Mathematical model for the natural history of human
papillomavirus infection and cervical carcinogenesis. Am
J Epidemiol 2000;151(12):1158-71.
5. Ho GY, Bierman R, Beardsley L, Chang CJ, Burk RD. Natural
history of cervicovaginal papillomavirus infection in young
women. N Engl J Med 1998;338(7):423-8.
6. Liaw KL, Hildesheim A, Burk RD et al. A prospective study
of human papillomavirus (HPV) type 16 DNA detection
by polymerase chain reaction and its association with
acquisition and persistence of other HPV types. J Infect Dis
2001;183(1):8-15.
7. Partridge JM, Koutsky LA. Genital human papillomavirus
infection in men. Lancet Infect Dis 2006;6(1):21-31.
8. Weaver BA, Feng Q, Holmes KK et al. Evaluation of genital
sites and sampling techniques for detection of human papil-
lomavirus DNA in men. J Infect Dis 2004;189(4):677-85.
9. Scheinfeld N, Lehman DS. An evidence-based review of
medical and surgical treatments of genital warts. Dermatol
Online J 2006;12(3):5.
10. Giuliano AR, Lee JH, Fulp W et al. Incidence and clearance
of genital human papillomavirus infection in men (HIM): a
cohort study. Lancet 2011;377(9769):932-40.
11. Lu B, Kumar A, Castellsague X, Giuliano AR. Effi cacy
and safety of prophylactic vaccines against cervical HPV
infection and diseases among women: a systematic review
& meta-analysis. BMC Infect Dis 2011;11:13.
12. Giuliano AR, Palefsky JM, Goldstone S et al. Effi cacy of
quadrivalent HPV vaccine against HPV Infection and disease
in males. N Engl J Med 2011;364(5):401-11.
13. Congilosi SM, Madoff RD. Current therapy for
recurrent and extensive anal warts. Dis Colon Rectum
1995;38(10):1101-7.
14. De la Fuente SG, Ludwig KA, Mantyh CR. Preoperative
immune status determines anal condyloma recurrence after
surgical excision. Dis Colon Rectum 2003;46(3):367-73.
15. Simmons PD, Langlet F, Thin RN. Cryotherapy versus
electrocautery in the treatment of genital warts. Br J Vener
Dis 1981;57(4):273-4.
16. Stone KM, Becker TM, Hadgu A, Kraus SJ. Treatment of
external genital warts: a randomised clinical trial comparing
podophyllin, cryotherapy, and electrodesiccation. Geni-
tourin Med 1990;66(1):16-9.
17. Billingham RP, Lewis FG. Laser versus electrical cautery
in the treatment of condylomata acuminata of the anus.
Surg Gynecol Obstet 1982;155(6):865-7.
18. Duus BR, Philipsen T, Christensen JD, Lundvall F, Sonder-
gaard J. Refractory condylomata acuminata: a controlled
clinical trial of carbon dioxide laser versus conventional
surgical treatment. Genitourin Med 1985;61(1):59-61.
19. Ferenczy A, Behelak Y, Haber G, Wright TC, Jr.,
Richart RM. Treating vaginal and external anogenital condy-
lomas with electrosurgery vs CO
2
laser ablation. J Gynecol
Surg 1995;11(1):41-50.
20. Yan J, Chen SL, Wang HN, Wu TX. Meta-analysis of 5%
imiquimod and 0.5% podophyllotoxin in the treatment of
condylomata acuminata. Dermatology 2006;213(3):218-
23.
21. Hoyme UB, Hagedorn M, Schindler AE et al. Effect of
adjuvant imiquimod 5% cream on sustained clearance of
anogenital warts following laser treatment. Infect Dis Obstet
Gynecol 2002;10(2):79-88.
22. Jensen SL. Comparison of podophyllin application
with simple surgical excision in clearance and recur-
rence of perianal condylomata acuminata. Lancet
1985;2(8465):1146-8.
23. Khawaja HT. Podophyllin versus scissor excision in the
treatment of perianal condylomata acuminata: a prospective
study. Br J Surg 1989;76(10):1067-8.
24. Komericki P, Akkilic-Materna M, Strimitzer T, Aberer W.
Effi cacy and safety of imiquimod versus podophyllotoxin
in the treatment of anogenital warts. Sex Transm Dis
2011;38(3):216-8.
25. Snoeck R, Bossens M, Parent D et al. Phase II double-
blind, placebo-controlled study of the safety and effi cacy of
cidofovir topical gel for the treatment of patients with human
papillomavirus infection. Clin Infect Dis 2001;33(5):597-
602.
Références bibliographiques
1
/
4
100%