Un impubérisme bien partiel… A very partial impuberism Observation

Correspondances en Métabolismes Hormones Diabètes et Nutrition - Vol. XVI - n° 10 - décembre 2012 - Vol. XVII - n° 1 - janvier 2013
304304
Cas clinique
Un impubérisme bien partiel…
A very partial impuberism
Julia Morera, Juliette Hardouin, Yves Reznik*
* Service d’endocrino-
logie-diabétologie, CHU
Côte-de-Nacre, Caen.
Observation
Monsieur L., 20 ans, est vu en consultation le 3 février
2010, à sa demande, pour une surcharge pondérale
d’apparition progressive depuis l’âge de 11 ans.
Il n’a aucun antécédent personnel ni familial et ne
prend aucun traitement. Il n’y a pas de surpoids chez
ses parents, ni chez ses frères et sœurs. L’interrogatoire
ne met pas en évidence d’erreurs alimentaires ni de
conduites compulsives.
À l’examen clinique, son poids est de 92 kg pour 1,82 m,
ce qui correspond à un indice de masse corporelle de
27,7 kg/m2. On note une macroskélie. Monsieur L.
chausse du 45, ses mains sont de taille normale.
Son père mesure 1,80 m pour 75 kg et sa mère 1,75 m
pour 60 kg.
On note une surcharge androïde, avec une circon-
férence abdominale de 106 cm. La tension artérielle
est normale, à 130/74 mmHg. Il n’y pas de signe cli-
nique évocateur d’hypothyroïdie ni d’hypercorticisme.
Le développement pubertaire est quasi normal, avec
un volume testiculaire à 15 ml (normale : 18 à 25 cm), et
des érections que le patient juge satisfaisantes, mais la
verge est de petite taille (4 cm) et la pilosité est incom-
plète, au stade P3. Il n’y a pas d’anosmie ni de syndrome
dysmorphique.
Sur le plan biologique, la numération-formule sanguine,
le ionogramme sanguin, la créatininémie, le bilan hépa-
tique et le bilan lipidique sont normaux. Il n’y a pas
d’anomalie du métabolisme glucidique. La ferritiné-
mie est normale, à 51 ng/ml, ainsi que le coeffi cient
de saturation, à 0,26.
En discordance avec le statut pubertaire clinique,
le taux de testostérone plasmatique totale est bas,
à 0,87 ng/ml (normale : 3-10), et les gonadotrophines ne
sont pas élevées : FSH à 1,38 mU/l et LH à 1,62 U/l. Trente
minutes après 100 μg LHRH en i.v., LH 14,5 mU/l et FSH
3,01 mU/l. L’analyse de la pulsatilité de la LH montre une
diminution de l’amplitude des pics (0,38 U/l chez notre
patient versus 2,4 ± 0,3 U/l chez les témoins étudiés).
Autres dosages : AMH 4,9 ng/ml (< 5,8), inhibine B
147 pg/ml (135-350), TSH 1,46 mU/l, T4 libre 9,5 pmol/l
(8-21), T3 libre 5,5 pmol/l (3,8-6,6), prolactine 7,89 ng/ml
et IGF1 434 ng/ml (175-495). GH sur 6 prélèvements
< 0,3 mU/l. Cortisol à 8 heures : 219 ng/ml (100-250),
15 ng/ml à 0 heure, ACTH 38 ng/ml (10-40). Cortisol
libre urinaire 70 μg/24 heures (< 100), cortisol après
freinage minute (1 mg dexaméthasone) : 10 ng/ml.
Le bilan hormonal conclut à un hypogonadisme hypo-
gonadotrope partiel et isolé. Le spermogramme n’est
pas disponible.
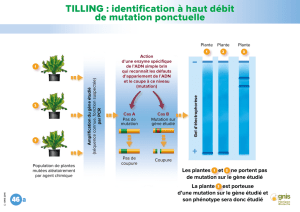
L’IRM hypophysaire met en évidence une hypophyse
bien visible et d’aspect normal. Il n’y a pas de déviation
de la tige pituitaire (fi gure 1).
Malgré le défi cit androgénique profond, la radiographie
du poignet gauche retrouve un âge osseux supérieur
à 13 ans, avec une quasi-soudure des cartilages de
conjugaison.
Devant ce tableau d’hypogonadisme hypogonadotrope
(HH) partiel sans étiologie tumorale ou infi ltrative à
l’IRM hypophysaire et sans anosmie ni syndrome dys-
morphique, une mutation du gène du récepteur de la
GnRH est recherchée. L’étude de ce gène met alors en
Figure 1. IRM hypophysaire : hypophyse de taille et de morphologie normales (séquence T2).

Correspondances en Métabolismes Hormones Diabètes et Nutrition - Vol. XVI - n° 10 - décembre 2012 - Vol. XVII - n° 1 - janvier 2013
305305
Un impubérisme bien partiel…
évidence une hétérozygotie composite pour les muta-
tions c.416G>A (R139H) et c.317A>G (Q106R) situées
sur l’exon 1 du gène du récepteur de la GnRH.
Une supplémentation androgénique est instaurée, et
une analyse génétique est proposée aux parents de
Monsieur L. : la mère du patient s’avère être porteuse
hétérozygote de la mutation c.416G>A (R139H) située
sur l’exon 1 du gène du récepteur de la GnRH, et le père
porteur hétérozygote de la mutation c.317A>G (Q106R)
située sur le même exon.
Discussion
Ce tableau de défi cit gonadotrope partiel induit par une
mutation du gène du récepteur de la GnRH illustre la
grande variabilité phénotypique de cette pathologie.
Ce patient présente un tableau inhabituel d’HH partiel
avec maturation osseuse quasi adulte et volume testi-
culaire normal malgré un défi cit gonadotrope profond.
L’HH congénital (HHC) est une cause rare d’hypo-
gonadisme (1/10 000).
La majorité des HH isolés s’intègre dans une pathologie
génétique liée à l’X, le syndrome de Kallmann, qui asso-
cie un hypogonadisme et une anosmie. Plusieurs gènes
impliqués ont été identifi és comme étant responsables :
les gènes KAL-1, KAL-2, de la prokinéticine et FGFR-1.
En l’absence d’anosmie, la recherche d’une mutation
du gène du récepteur de la GnRH est à eff ectuer en
première intention, puis, en deuxième intention, celle
d’une mutation de GPR54 (régulateur de la sécrétion
de GnRH) ou du gène de la GnRH.
Le gène du récepteur à la GnRH est un récepteur couplé
aux protéines G, composé de 3 exons localisés sur le
chromosome 4.
Jusqu’à 22 mutations ont été décrites, la plus fréquente
étant la mutation Q106R, située sur la première boucle
extracellulaire. Cette mutation, transmise sur le mode
autosomique récessif, concerne 5 % des HHC sans anos-
mie. Cette prévalence s’élève à 40 % en cas de forme
familiale.
Le diagnostic d’HH isolé est classiquement évoqué
devant un impubérisme à l’âge de 18 ans, une hypotes-
tostéronémie et des concentrations faibles de gonado-
trophine. Néanmoins, la présentation phénotypique
est très variable, et tous les stades pubertaires peuvent
être retrouvés à l’âge adulte. Une relation génotype-
phénotype a ainsi pu être établie (fi gure 2) [1], même
si certaines études ont publié des cas familiaux d’HH
isolé chez des patients porteurs de la même mutation
Figure 2. Corrélations génotype-phénotype des mutations du gène du récepteur de la GnRH (d’après [1]).
* et ** : membres de la même famille.
Tyr108Cys/Thr104Ile*
Arg139His/Arg139His
Arg139Cys/Arg139Cys
Arg262Glm/Tyr284Cys
Gln106Arg/L314X
Ala129Asp/Arg262Gln
Splice site mutation, skipping exon 2
Asn10Lys/Gln106Arg
Glu90Lys/Glu90Lys
Arg262Gln/Ala129Asp
Ser168Arg/Ser168Arg
Ala171Thr/Gln106Arg
Arg139His/Arg139His
Cryptorchidie
et/ou micropénis
Aménorrhée primaire
Absence de développement mammaire
Aménorrhée primaire
et développement mammaire partiel
Développement mammaire de partiel à complet,
oligoménorrhée, grossesse spontanée ou induite
par administration de GnRH
Réponse partielle à l’administration de GnRH pulsatile
HHC totale :
sans micropénis ou
cryptorchidie
TV > 6 ml
eunuque fertile
Puberté retardée
Oligospermie
Thr32Ile/Cys200Tyr
Gln106Arg+Ser217Arg/Arg262Gln**
Leu266Arg/Leu266Arg
Ala129Asp/Arg262Gln
Gln106Arg/Arg262Gln
Gln106Arg/Gln106Arg
Tyr108Cys/Thr104Ile*
Arg262Gln/Arg262Gln
Gln106Arg+Ser217Arg/Arg262Gln**
Asn10Lys+Gln11Lys/Pro320Leu
Gln106Arg/Arg262Gln
Gln206Arg/Leu266Arg
Gln106Arg/Gln106Arg
Gln106Arg/Arg262Gln
Gln106Arg/Leu265Arg
Asn10Lys/Gln106Arg
Sévère Moyenne

Correspondances en Métabolismes Hormones Diabètes et Nutrition - Vol. XVI - n° 10 - décembre 2012 - Vol. XVII - n° 1 - janvier 2013
306306
Cas clinique
mais présentant des défi cits gonadotropes de profon-
deurs variables (2).
Le degré d’inhibition du signal de transduction du
récepteur de la GnRH induite par la mutation infl uence
le caractère partiel ou complet de l’hypogonadisme.
La mutation Q106R est une mutation perte de fonc-
tion responsable d’une diminution de la liaison de la
GnRH à son récepteur et de la transduction du signal
(3), souvent présente à l’état hétérozygote et associée
à d’autres mutations.
Les cas décrits dans la littérature d’hétérozygotie com-
posite avec Q106R ont une présentation phénotypique
très variable allant d’un tableau d’HH complet à un
tableau d’hypogonadisme partiel (simple retard puber-
taire, oligospermie isolée, voire syndrome de l’eunuque
fertile) [1, 4, 5] (fi gure 2), en rapport avec le second allèle
muté. Un cas d’homozygotie pour cette mutation a
été décrit, et le tableau était celui d’un syndrome de
l’eunuque fertile (1).
La mutation Q106R est donc une mutation perte de
fonction partielle pouvant expliquer une faible activité
du récepteur.
La mutation R139H entraîne une interruption de la
transduction du signal et de la liaison du récepteur à la
protéine G (3). À notre connaissance, la mutation R139H
n’a été décrite qu’à l’état homozygote, et la présentation
phénotypique univoque est celle d’un HH complet (1).
À l’état homozygote, cette mutation est responsable
d’une perte complète de fonction du récepteur.
L’hétérozygotie Q106R/R139H du patient peut ainsi
expliquer la diminution d’activité du récepteur et le
tableau d’hypogonadisme partiel.
Le volume testiculaire normal traduit probablement
une sécrétion suffi sante de FSH pour le développe-
ment des tubes séminifères, réalisant ainsi le tableau
de l’eunuque fertile.
Le déficit androgénique profond contraste avec le
développement subnormal du statut pubertaire cli-
nique et la maturation osseuse. Il pourrait s’agir d’une
interruption prématurée de l’activité gonadotrope après
démarrage pubertaire.
Les mutations du récepteur de la GnRH dans les cas
d’HH sévère et complet sont responsables d’une résis-
tance hypophysaire à l’administration pulsatile de la
GnRH, elle-même responsable d’une perte de la pul-
satilité de LH (2).
Dans les HH partiels, la sécrétion de LH reste pulsatile,
mais avec une diminution de l’amplitude des pulses
(2, 4).
En conclusion, la présentation clinique des patients
atteints d’HH isolé peut être très variable. Il faut, dans
ce contexte clinique, rechercher une anomalie géné-
tique, et ce même en cas de phénotype partiel et de
découverte post-pubertaire de l’HH.
■
1. Brioude F, Bouligand J, Trabado S et al. Non-syndromic
congenital hypogonadotropic hypogonadism: clinical presen-
tation and genotype-phenotype relationships. Eur J Endocrinol
2010;162:835-51.
2.
De Roux N , Young J, Brailly-Tabard S, Misrahi M, Milgrom E,
Schaison G. The same molecular defects of the gonadotropin-
releasing hormone receptor determine a variable degree of
hypogonadism in aff ected kindred. J Clin Endocrinol Metab
1999;84:567-72.
3. Karges B, Karges W, de Roux N. Clinical and molecular
genetics of the human GnRH receptor. Hum Reprod Update
2003;9:523-30.
4. De Roux N, Young J, Misrahi M et al. A family with hypogona-
dotropic hypogonadism and mutations in the gonadotropin-
releasing hormone receptor. N Engl J Med 1997;337:1597-602.
5. Chevrier L, Guimiot F, de Roux N. GnRH receptor mutations
in isolated gonadotropic deficiency. Mol Cell Endocrinol
2011;346:21-8.
Références
Les articles publiés dans “Correspondances en Métabolismes Hormones Diabètes et Nutrition” le sont sous la seule responsabilité de leurs auteurs.
Tous droits de reproduction, d’adaptation et de traduction par tous procédés réservés pour tous pays.
© octobre 1997 - Edimark SAS
Imprimé en France – Axiom Graphic SAS - 95830 Cormeilles-en-Vexin – Dépôt légal : à parution
1
/
3
100%