Cas clinique L Puberté différée ou hypogonadisme ? Retarded puberty or hypogonadism?

Métabolismes Hormones Diabètes et Nutrition (X), n° 1, janvier/février 2006
Puberté différée ou hypogonadisme?
Retarded puberty or hypogonadism?
J.M. Kuhn*
L
e jeune D.P., adolescent de 16 ans, est accompa-
gné en consultation par ses parents, qui s’inquiè-
tent d’un retard statural. Le jeune homme mesure
en effet 149 cm, ce qui le situe à – 3,5 DS de la
moyenne pour l’âge. Il n’a aucun antécédent médical
ou chirurgical et ne suit aucun traitement. Il est en
première S après avoir suivi un cursus scolaire normal.
Son père, sa mère et son jeune frère de 12,5 ans, tous
en parfaite santé, mesurent respectivement 176, 164 et
150 cm. Lors de la consultation initiale, D.P. pèse
44 kg. La courbe de croissance établie à partir des don-
nées recueillies dans le carnet de santé s’inscrit dans la
moyenne jusqu’à l’âge de 12 ans, puis s’en écarte pro-
gressivement. D.P. ne présente aucun signe de déve-
loppement pubertaire. Il n’a ni gynécomastie ni déve-
loppement pilaire (celui-ci est coté A1-P1). L’examen
des organes génitaux externes ne révèle aucune ambi-
guïté périnéale. Il n’y a pas de micropénis, mais deux
testicules intrascrotaux de 3 ml. L’odorat est normal.
D.P. est en euthyroïdie et en eucortisolisme cliniques.
Sa pression artérielle est mesurée à 115/60 mmHg. Le
reste de l’examen clinique ne révèle aucune anomalie.
La LH et la FSH, mesurées à l’issue de la consultation,
sont respectivement à 2,5 et 3 mU/ml. Le taux de testo-
stérone plasmatique est à 0,5 ng/ml et l’estradiolémie
est inférieure à 10 pg/ml. La TSH plasmatique est à
3,66 mU/l (N : 0,1-4,5) et l’IGF-1, mesurée à
121 ng/ml, s’inscrit dans la norme des enfants prépu-
bères. Les données de l’examen clinique jointes aux
premiers résultats biologiques amènent à réaliser, en
hôpital de jour, un bilan plus complet. Après adminis-
tration i.v. de 100 µg de GnRH, la LH et la FSH attei-
gnent respectivement 7 et 5 mU/ml. La testostéronémie
matinale est à 0,55 ng/ml. En réponse au chlorhydrate
d’ornithine, le taux plasmatique d’hormone de crois-
sance s’élève de 4 à 39 ng/ml (N > 10). Le taux de pro-
lactine plasmatique est à 8 ng/ml. L’âge osseux, en
retard par rapport à l’âge chronologique, est en adéqua-
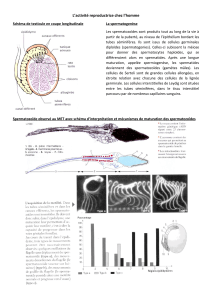
tion avec l’âge statural. L’olfactométrie, le champ visuel
et l’examen par IRM de la région hypophysaire
(figure 1) se révèlent normaux.
À ce stade, les résultats du bilan sont compatibles soit
avec un hypogonadisme hypogonadotrope, dont l’étiolo-
gie serait alors à préciser, soit avec un retard pubertaire
simple. L’harmonieux développement jusqu’à 12 ans,
l’absence d’obésité, d’hypotonie et la normalité du
cursus scolaire suffisent à écarter l’hypothèse d’un hypo-
gonadisme s’inscrivant dans le cadre d’un syndrome de
Willi-Prader. La perception adéquate des odeurs permet
d’écarter un syndrome de Kallmann-de Morsier lié à l’X.
La présence de deux testicules intrascrotaux et les résul-
tats de l’IRM, sans être des arguments de certitude, ne
sont pas en faveur des autres causes de déficit congénital
en GnRH, qu’ils soient sous-tendus par une mutation du
gène du récepteur de type 1 du FGF ou du GPR54. Une
anomalie du récepteur de la GnRH demeure plausible,
mais la faible ascension des gonadotrophines après injec-
tion i.v. de GnRH peut s’observer aussi bien dans ce
cadre que dans celui du retard pubertaire simple. C’est
donc à la bonne vieille méthode du test à l’hCG que la
suite de l’enquête étiologique a recours. Soixante-
douze heures après injection de 5 000 unités d’hCG par
voie i.m., la testostéronémie atteint le chiffre de
* Service d’endocrinologie et maladies métaboliques, CHU de Rouen.
35
Cas clinique
Cas clinique
Figure 1. Examen par IRM de la région hypothalamo-hypophysaire
ne révélant aucune anomalie morphologique.

Testostérone ng/ml
(heures)
24Base 48 72
0
5
10
15
hCG 5 000 U
Témoins
DP
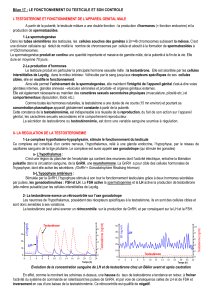
Figure 2. Évolution du taux de testostérone après injection i.m. de
5 000 unités de hCG.
36
Métabolismes Hormones Diabètes et Nutrition (X), n° 1, janvier/février 2006
3,2 ng/ml (figure 2). Le seuil de 2,5 ng/ml étant dépassé
(ce qui témoigne d’un démarrage du processus puber-
taire), le diagnostic retenu est celui de retard pubertaire
simple, même s’il n’y a aucun antécédent identifiable de
ce type dans la famille. Élément confirmatif supplémen-
taire, la recherche d’une mutation inactivatrice du gène
codant le récepteur de la GnRH se révèle négative.
L’évolution ultérieure confirme l’hypothèse de retard
pubertaire simple, puisque, à 18,5 ans, le taux de testo-
stérone plasmatique de D.P. est, en dehors de tout traite-
ment, de 4,9 ng/ml et s’accompagne d’une augmentation
notable du volume testiculaire. Néanmoins, à l’issue du
bilan réalisé initialement, une substitution androgénique
est instaurée à l’âge de 16 ans 3 mois pour accélérer
le développement pubertaire, pour atténuer le retentis-
sement psychologique du retard staturopondéral et
pubertaire et pour préserver le capital osseux. Si les deux
premiers objectifs sont atteints, il n’en est pas de même
en ce qui concerne l’os. Alors qu’il est traité par une
injection de 100 mg d’heptylate de testostérone toutes les
trois semaines depuis plus d’un an, D.P., âgé de 17,5 ans,
chute de sa hauteur et se brise le col fémoral droit.
L’ostéodensitométrie révèlera un risque ostéoporotique
élevé pour la tranche d’âge. L’androgénothérapie est
intensifiée, puis, une fois démontrée, à 18,5 ans, la nor-
malisation de la sécrétion endogène de testostérone, le
relais est pris par une supplémentation en calcium et en
vitamine D.
Cette observation, qui illustre les nuances sémiologiques
séparant un authentique hypogonadisme hypogonado-
trope congénital d’un retard pubertaire simple, permet de
souligner les répercussions squelettiques précoces d’une
imprégnation différée en androgènes au cours de la
puberté masculine. Il est donc important d’identifier
celle-ci afin d’adopter une attitude préventive, qui, dans
un tel contexte, devrait reposer sur un apport transitoire
en androgènes dès l’âge de 16 ans.
■
■
Cas clinique
Cas clinique
1
/
2
100%