La voie moléculaire dans la formation des carcinomes basocellulaires Mise au point

Images en Dermatologie • Vol. VII • n
o
1 • janvier-février 2014
20
PTCH
Absence de signal
GLI
Inhibition de la croissance tumorale
SMO
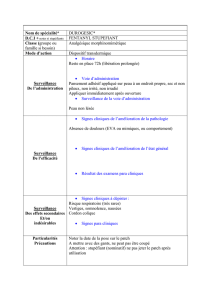
Figure 1. Voie de signalisation hedgehog inactive.
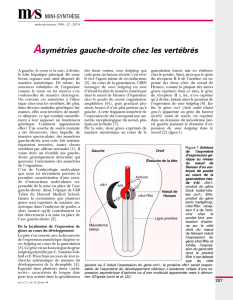
Figure 2. Voie patch activée.
s
ig
na
ti
on
de
la
c
ro
i
▶Points forts
•
Patch/sonic/hedegehog : une voie essentielle dans le
développement des CBC
•
Des inhibiteurs de SMO ont été developpés pour le trai-
tement des CBC localement avancés ou métastatiques
▶
Highlights
•
Patch/sonic/hedgehog: a driver pathway in the deve-
lopment of BCC
•
SMO inhibitors have been developped for the treatment
of locally advanced or metastatic BCC
Mise au point
La voie moléculaire dans la formation des carcinomes
basocellulaires
Molecular pathway implicated in BCC development
N. Basset-Seguin (Polyclinique de dermatologie, hôpital Saint-Louis, AP-HP, Paris ; université Paris-7)
D
epuis 1996, grâce aux travaux réalisés chez les patients
atteints du syndrome de Gorlin, la voie moléculaire
impliquée dans la formation des carcinomes baso-
cellulaires (CBC) a été identifi ée: il s’agit de la voie patch/
sonic/hedgehog
(1, 2)
.
Ces patients ont une mutation constitutive du gène patch, ce
qui explique que, dans toutes leurs cellules, un seul allèle de
patch soit normal. Il est donc beaucoup plus facile d’inactiver
l'allèle restant, et la double inactivation est responsable de la
formation de tumeur chez ces patients. Dans les carcinomes
basocellulaires sporadiques, les deux allèles de patch doivent
être inactives, ce qui explique que ce phénomène soit plus
tardif.
Voie patch/sonic/hedgehog et carcinomes
basocellulaires
La voie patch/sonic/hedgehog contrôle la prolifération et la
différenciation cellulaire au cours de l’embryogenèse
(3)
. Elle
est composée de 2récepteurs transmembranaires, PTCH et
SMO. En l’absence de son ligand hedgehog (HH), PTCH inhibe
l’activation de SMO
(fi gure1)
. Lorsque le ligand HH se lie à
PTCH, il y a levée de l’inhibition de SMO par PTCH et activation
de la voie moléculaire d’aval, entraînant l’activation, via divers
protéines interactives, des membres de la famille Gli (Gli1, Gli2,
Gli3), qui sont des activateurs transcriptionnels, et qui induisent
la transcription de divers gènes impliqués dans le contrôle de
la prolifération et la différenciation cellulaires
[fi gure2]
.
Au cours des CBC, il y a activation de la voie surtout par muta-
tions inactivatrices de patch (décrites plus haut) mais aussi
par mutations activatrices de SMO ou plus rarement de HH
(fi gure2, étoiles)
.
Molécules anti-SMO disponibles et résultats
des essais cliniques
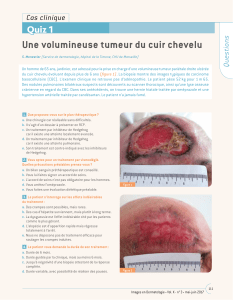
Il existe actuellement 2molécules anti-SMO à l’essai dans le
traitement des CBC avancés ou métastatiques: GDC-0449,
ou vismodégib (laboratoires Roche)
[fi gure3]
et le LDE225
(laboratoires Novartis). Les études cliniques sont plus avancées
avec le vismodégib, qui a été approuvé par la Food and Drug

Images en Dermatologie • Vol. VII • n
o
1 • janvier-février 2014
21
Figure 3. Vismodégib (GDC-0449) inhibe SMO. Un médiateur central
de la voie de signalisation Hedgehog.
PT
CH
Absence de signal
G
LI
Inhibition de la croissance tumorale
SM
O
V
ismo
d
égi
b
G
DC-0449
Inhi
b
iti
o
n
N
HN
O
O
O
Cl
C
l
S
4
ig
n
i
ti
on de la cro
is
sa
nc
Mise au point
Administration (FDA) aux États-Unis en janvier 2012 dans l’indi-
cation: traitement des carcinomes basocellulaires avancés
ou métastatiques. Plus récemment, une autorisation de mise
sur le marché (AMM) conditionnelle a été obtenue en Europe.
Les résultats d’une phaseI ayant pour objectif la tolérance,
l’étude pharmacocinétique et l’évaluation de l’effi cacité du vis-
modégib dans les CBC localement avancés (CBCLa) ou méta-
statiques (CBCm) ont été publiés en 2009
(4)
. Dans ce travail,
33patients avec un CBCLa ou m ont pris du vismodégib à1
des 3doses étudiées (150 mg [n=17], 250 mg [n=15], 450mg
[n=1]). Parmi eux, 18 (54%) patients ont eu une réponse objec-
tive clinique (n=10), sur l’ imagerie (n=7) ou sur les2 (n=1).
Parmi les autres patients, 11 sont restés stables (33%) et 4ont
vu leur maladie progresser (12%).
Parmi les patients ayant un CBCLa (n=15) et qui avaient été
suivis entre 2,1 et 19 mois au moment de la publication, 2(13%)
étaient en rémission complète, 7 (46%) en rémission partielle
et 4 (26%) étaient stables. Enfi n 2 (13%) patients CBCLa étaient
en progression. La réponse globale pour les CBCLa était de
60% (IC95: 33-83).
Parmi les patients CBCm, la réponse globale observée était
de 50% (IC95: 29-71)
Ces résultats sont remarquables étant donné l’absence de
traitement de référence pour ce type de patients qui n’avaient
auparavant aucune solution.
Il n’y a pas eu, pendant l’étude, d’effet indésirable dose limitant
ou de grade 5. Parmi les effets indésirables de grade3 les plus
fréquemment observés, on notait: une hyponatrémie asymptoma-
tique de grade 3 ou 4, une fatigue, une perte de poids, une dyspnée,
des crampes musculaires et une fi brillation auriculaire. Seul
1patient est sorti de cette étude à cause des effets indésirables.
Cette étude de phase I a donc montré la tolérabilité et l’effi cacité
antitumorale du vismodégib dans le traitement des CBCLa et m.
Un essai de phase II international multicentrique a suivi et a
été publié en 2012
(5)
. L’objectif primaire de cette étude était le
taux de réponse objective indépendante du vismodégib dans les
CBCLa et m (la réponse étant évaluée par un panel d’experts
indépendants de l’essai à partir des données photographiques
et d’imagerie). Dans cette étude, 33 patients avaient un CBCm,
et leur taux de réponse indépendante était de 30% (IC
95
: 16-48).
Les patients avec un CBCLa (n=63) avaient un taux de réponse
de 43% (IC95: 31-56), dont 13 réponses complètes (21%). Ces
chiffres sont légèrement plus bas, à la fois pour les CBCm et
les CBCLa, que lors de l’étude de phaseI, mais cela est en
partie lié à la sous-évaluation de l’analyse indépendante qui
n’a raisonné que sur des documents photographiques.
Les effets indésirables étaient observés chez 30% des patients.
Les plus fréquents étaient crampes, alopécie, dysgueusie, perte de
poids et fatigue, et correspondent à ceux reportés dans les études
de phase I et II avec le vismodégib ou avec d’autres inhibiteurs de
hedgehog (LDE225)
[6]
. Au moment de la publication, environ la
moitié des patients avaient arrêté le traitement du fait d’effets
indésirables et le temps moyen de prise du médicament était de
10 mois dans les 2 groupes de patients (CBCLa et m). L’arrêt du
médicament était lié le plus souvent à la progression de la maladie
pour les patients CBCm, et à la décision du patient dans le groupe
des CBCLa. Des effets indésirables sérieux étaient notés chez 25%
des patients. Sept décès ont été rapportés. Dans 3 cas, la cause de
la mort est restée inconnue. Dans les 4 autres cas, le décès était dû
à un choc hypovolémique, une atteinte méningée, un infarctus du
myocarde, un accident vasculaire. Ces effets indésirables graves
sont survenus chez des patients à risque. La responsabilité du
vismodégib dans ces effets graves n’est pas connue.
Ce travail a donc confi rmé l’effi cacité antitumorale du vismodégib
dans la prise en charge des patients atteints de CBCLa oum.
Le problème de la tolérance à long terme du vismodégib a été
posé et a justifi é la mise en place de l’essai STEVIE, qui prévoit
a inclus 1 200patients dans le monde. Cet essai est toujours
en cours. Son objectif principal est l’évaluation de la tolérance
du traitement. Son objectif secondaire, celle de son effi cacité.
Conclusion
La découverte de l’importance de la voie hedgehog dans cer-
tains cancers, et en particulier dans les CBC, et le développe-
ment d’inhibiteurs de cette voie ont permis de transformer la
prise en charge des formes avancées ou métastatiques pour
lesquels nous nous trouvions dans une impasse thérapeutique.
Les taux de réponse observés sont très encourageants. ❙❙
L’auteur déclare avoir des liens d’intérêts avec Roche.
Références bibliographiques
1.
Hahn H, Wicking C, Zaphiropoulous PG et al. Mutations of the human
homolog of Drosophila patched in the nevoid basal cell carcinoma syndrome.
Cell 1996;85(6):841-51.
2.
Johnson RL, Rothman AL, Xie J et al. Human homolog of patched, a candi-
date gene for the basal cell nevus syndrome. Science 1996;272(5268):1668-71.
3.
Ingham PW. Hedgehog signaling. Cold Spring Harb Perspect Biol 2012;4(6).
pii:a011221.
4.
Von Hoff DD, LoRusso PM, Rudin CM et al. Inhibition of the hedgehog
pathway in advanced basal-cell carcinoma. N Engl J Med 2009;361(12):1164-72.
5.
Sekulic A, Migden MR, Oro AE et al. Effi cacy and safety of vismodegib in
advanced basal-cell carcinoma. N Engl J Med 2012;366(23):2171-9.
1
/
2
100%