L’échographie transœsophagienne (ETO) : un outil indispensable pour traiter l’arythmie complète

La Lettre du Cardiologue - n° 341 - janvier 2001
21
ACFA est le plus courant des troubles du rythme. Sa
prévalence de 0,5 % dans une population globale (soit
300 000 cas en France) est directement fonction de
l’âge : 0,1 % de 16 à 59 ans ; 1,7 % de 60 à 64 ans ; 17 % ≥85 ans
(étude de Framingham). Il en va de même de l’incidence annuelle
qui, dans la même étude, est de 0,1 % et un peu plus élevée chez
l’homme que chez la femme (1 % vs 0,8 ‰), soit 60 000 nou-
veaux cas par an en France. Elle expose à deux types de compli-
cations graves : accidents thromboemboliques (dont les trois
quarts sont cérébraux) et insuffisance cardiaque, elle multiplie
par deux la mortalité (1).
L’échographie cardiaque transthoracique apparaît aujourd’hui
comme un outil indispensable à la recherche de la cause et du
retentissement d’amont (oreillettes - petite circulation) de la fibril-
lation auriculaire.
Qu’en est-il de la place de l’ETO ?
PLACE DE L’ETO DANS L’ACFA VALVULAIRE
La survenue d’une ACFAdans une valvulopathie mitrale marque
un tournant évolutif et conduit habituellement à s’interroger sur
l’opportunité d’une prise en charge chirurgicale.
En cas de fuite mitrale
L’échographie transthoracique (ETT) reste l’étape fondamentale
fournissant à la fois le mécanisme précis, l’étiologie et la sévé-
rité de la régurgitation (étape incontournable de la détermination
de la surface de l’orifice régurgitant par la mesure du rayon du
flux de convergence).
L’ETO apparaissait récemment encore comme indispensable
pour :
– une bonne compréhension du mécanisme de la fuite et des pos-
sibilités de réparation conservatrice (localisation et nombre de
festons touchés par le prolapsus ou les ruptures de cordages...) ;
– l’appréciation de l’importance de la régurgitation sur les cri-
tères du diamètre du jet à l’origine et de morphologie du flux vei-
neux pulmonaire (recherche de l’inversion du flux systolique dans
les quatre veines pulmonaires).
L’avènement d’échographes de haute résolution permet aujour-
d’hui une analyse complète par la seule voie transthoracique chez
les trois quarts des patients.
DOSSIER
L’échographie transœsophagienne (ETO) :
un outil indispensable pour traiter l’arythmie complète
par fibrillation auriculaire (ACFA) ?
●
J.P. Lesbre, A. Mirode, J. Boulanger, S. Gharbi*
■
L’ETT est un examen indispensable pour toute fibril-
lation auriculaire :
❏elle éclaire largement son étiologie,
❏elle précise son retentissement sur les cavités auricu-
laires et la petite circulation,
❏elle permet de rationaliser les indications et les contre-
indications du choc électrique.
■
L’ETO ne fait pas encore l’unanimité quant à son
rôle et ses indications dans la prise en charge de
l’ACFA :
❏elle s’impose dans l’ACFA compliquée d’AVC pour
en comprendre la pathogénie, souvent complexe, et
guider son traitement ;
❏elle s’impose également pour l’évaluation rigoureuse
du risque thromboembolique d’une ACFAchronique
non valvulaire, car elle seule peut guider le choix dif-
ficile entre AVK et aspirine : les critères cliniques sont
trop imprécis pour fonder un choix thérapeutique de
cette importance ;
❏elle s’impose dans l’ACFA valvulaire de la sténose
mitrale et autorisera la dilatation percutanée en l’ab-
sence de thrombus ;
❏elle ne s’impose pas, en revanche, avant réduction de
l’ACFArécente, puisque l’étude ACUTE renvoie dos
à dos les deux stratégies de prise en charge possibles.
Points forts
* CHU Amiens.
L
‘

L’ETO est utile lorsque l’ETT n’a pu fournir tous les renseigne-
ments voulus pour des raisons d’échogénicité, ou lorsqu’on soup-
çonne une endocardite ou une thrombose intra-auriculaire, très
rare dans le cadre des IM pures sévères.
En cas d’ACFA sur sténose mitrale
L’ETO est indispensable car le risque de thrombus intra-auricu-
laire est très élevé dans ce cas : le chirurgien comme le cardio-
logue interventionnel ont besoin d’y recourir pour réduire les
risques potentiels de leur geste. L’ETO s’impose donc, car elle
constitue aujourd’hui la meilleure méthode diagnostique du
thrombus, de l’oreillette et de l’auricule gauche.
ACFA NON VALVULAIRE
ACFA récente : ETO et choc électrique
Devant toute ACFArécente non compliquée se pose le problème
de la réduction : elle mérite d’être tentée chaque fois que pos-
sible, car elle met à l’abri des complications éventuelles thrombo-
emboliques ou de l’insuffisance cardiaque.
Sous l’angle théorique, l’ETO apparaît comme hautement sou-
haitable avant réduction, puisque la mise en évidence d’un throm-
bus contre-indique la réduction pharmacologique aussi bien que
par choc électrique. Or, cette éventualité est loin d’être rare
puisque dans un travail récent (2) portant sur 119 patients sou-
mis à ETO systématique, avant choc, sous héparine, notre groupe
retrouvait 14 % de thrombus (18 dans l’auricule, 1 seul dans
l’oreillette gauche et 2 dans l’oreillette droite).
Il était donc permis de penser que l’ETO systématique avant tout
choc électrique permettrait de réduire et les accidents throm-
boemboliques post-choc, et le pourcentage d’échecs de la conver-
sion, puisque ce pourcentage est proportionnel à la durée de la
fibrillation auriculaire.
L’étude ACUTE (3) apporte dans ce domaine un éclairage nou-
veau ; cette étude prospective randomisée compare deux straté-
gies de prise en charge de la FA chez 1 222 patients :
– stratégie conventionnelle : AVK pendant 3 semaines avant et
4 semaines après le choc,
– stratégie rapide guidée par ETO : anticoagulation brève par
héparine, ETO guidant le choc électrique (pas de choc en cas de
thrombus), AVK 4 semaines suivant le choc.
Les critères de jugements primaires sont les événements throm-
boemboliques à 8 semaines, les critères secondaires étant les évé-
nements hémorragiques, le taux de retour en rythme sinusal, la
mortalité.
Les résultats sont synthétisés dans le tableau I :
Il ressort de la lecture de ce tableau que la stratégie de prise en
charge rapide guidée par l’ETO n’a aucune supériorité par rap-
port à la stratégie conventionnelle, si ce n’est en termes de réduc-
tion du pourcentage d’hémorragies. Pour tous les autres critères,
il n’y a aucune différence.
On peut, dès lors, se demander s’il n’est pas préférable pour le
confort du patient de rester fidèle à la stratégie conventionnelle
d’anticoagulation préalable efficace (INR entre 2 et 3) couplée à
la prescription d’amiodarone (2 comprimés par jour pendant 1 à
3 semaines). On favorisera ainsi le pourcentage de réductions
“spontanées” (# 30 à 40 %) et on évitera une hospitalisation, une
anesthésie et une ETO.
L’ETO ne sera proposée qu’aux 60 % restants, avec le double
mérite : d’éliminer un thrombus, et de guider le traitement au long
cours des patients après échecs du choc.
Rappelons enfin que, quelle que soit la stratégie adoptée, l’anti-
coagulation pendant les quatre semaines suivant le choc est un
impératif thérapeutique absolu ; en effet, le risque thrombo-
embolique est au maximum lors de la phase de sidération auri-
culaire post-choc, sidération d’autant plus prolongée que la fibril-
lation est ancienne, comme l’ont bien montré les travaux de
Manning et Grimm (4-5).
ACFA ancienne “titularisée” : l’appréciation du risque
thromboembolique
Nous entendons par là une fibrillation auriculaire ayant plus d’un
an d’ancienneté. Comme dans la forme récente, se posent les
questions de l’étiologie, de l’opportunité de la réduction et du
traitement au long cours par AVK :
–L’étiologie est résolue par la clinique, l’écho transthoracique et
le bilan thyroïdien.
–L’opportunité de la réduction est également résolue par l’écho
transthoracique. Sont considérées comme contre-indications à la
réduction : une OG ≥60 mm, une dysfonction ventriculaire
gauche sévère (FE ≤30 %), un thrombus OG-VG, une FAde plus
de 3 ans.
– La question du traitement par AVK au long cours recoupe celle
de l’appréciation du risque thromboembolique et impose le
recours à l’ETO. L’appréciation de ce risque peut intervenir à
trois niveaux : clinique, ETT, ETO.
●Au niveau clinique
L’étiologie intervient de façon majeure : il faut mettre à part
l’ACFA d’origine rhumatismale, qui multiplie par 17 le risque
relatif d’AVC, par opposition à l’ACFA non valvulaire (6), qui
multiplie ce risque par 5, et à l’ACFAidiopathique qui, selon les
critères d’inclusion très rigoureux de la Mayo Clinic (âge < 60 ans,
pas d’HTA), ne comporte pas de risque thromboembolique (7),
comme l’a démontré un suivi de 14 ans.
Certains facteurs de risque permettent une stratification du risque
embolique. Dans l’étude SPAF 1 (8), concernant 1 330 FA non
valvulaires et suivies 16 mois, ces risques sont l’hypertension
(TA ≥160/90 à trois reprises), les antécédents d’AVC/AIT, le dia-
bète, l’insuffisance cardiaque, l’âge > 75 ans chez la femme.
En l’absence de facteur de risque, le risque d’AVC est bas : 1,4 %
par an.
La Lettre du Cardiologue - n° 341 - janvier 2001
22
D
OSSIER
Groupe ETO Groupe “conventionnel” p
(%) (%)
AVC + AIT + emboles 0,81 0,50 NS
Hémorragies 3,11 5,50 0,02
Hémorragies majeures 0,81 1,50 NS
Succès du choc 80 80 NS
Patients en rythme sinusal 52,7 50,4 NS
(à 2 mois)
Mortalité cardiovasculaire 1,29 0,66 NS
Tableau I. Résultats de l’étude ACUTE.

La Lettre du Cardiologue - n° 341 - janvier 2001
23
En présence d’un facteur de risque, le risque d’AVC s’élève à
7,2 % par an.
En présence de plus de deux facteurs de risque, le risque d’AVC
s’élève à 17,6 % par an.
●Au niveau échographique
L’étude SPAF 2 (9) a permis de retenir seulement, sur les 14 para-
mètres testés, le rôle de la taille de l’OG et de la fonction VG :
– une OG ≥2,9 cm/m2en TM multiplie par 2,7 le risque relatif
d’AVC ;
– une dysfonction VG multiplie par 2,6 le risque relatif d’AVC ;
– la conjonction des deux multiplie par 3,9 le risque relatif d’AVC,
qui atteint alors 20 % par an.
Il convient de souligner que la stratification échographique
diverge notablement de la stratification clinique et conduit à clas-
ser comme patients à risque (méritant un traitement AVK) 38 %
des patients sans facteur de risque clinique et traités initialement
par aspirine.
●L’ETO constitue le troisième niveau de stratification du
risque thromboembolique
Sa valeur et son apport spécifique ont été remarquablement étu-
diés dans l’étude SPAF 3 (10). Il s’agit d’une étude prospective
randomisée portant sur 382 patients en FAnon valvulaire et consi-
dérés comme patients à haut risque thromboembolique, puisqu’ils
présentaient au moins l’un des cinq critères définis par les études
SPAF 1 et 2 : hypertension ≥160/90, antécédents d’AVC ou
emboles, insuffisance cardiaque, dysfonction VG échographique
(fraction de raccourcissement < 25 %), femme > 75 ans.
Le but de cette étude était de définir les critères ETO prédictifs
d’AVC et de comparer l’efficacité thérapeutique de la warfarine
et de l’aspirine. Tous les patients ont été soumis à une ETO à l’en-
trée de l’étude et suivis pendant 14 mois en moyenne, en parti-
culier sous l’angle des événements thromboemboliques.
Les critères ETO prédictifs d’événements thromboemboliques
sont repris dans le tableau II.
D
OSSIER
Tableau II. Les paramètres ETO prédictifs d’AVC (étude SPAF 3).
Paramètre ETO AVC par an (%) Risque relatif d’AVC
1. Contraste spontané dense 18,2 2,9
(20 % des patients)
2. Thrombus auriculaire gauche
(10 % des patients) 17,9 2,7
3. Vitesse de vidange
AG < 20 cm/s 13,1 2,6
(37 % des patients)
4. Plaque aortique complexe 15,8 12,3
(35 % des patients)
5. Plaque aortique complexe
+ 1, 2 ou 3
(7 % des patients) 20,5 16
6. Aucune anomalie 1,3 0,2
(32 % des patients)
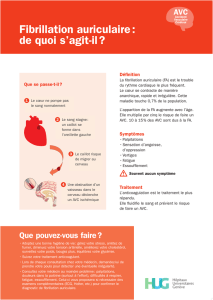
Patiente de 77 ans adressée pour monoplégie régressive et arythmie com-
plète.
L’ETO met en évidence un thrombus grelot, bilobé, dans l’auricule
gauche (A) et une vitesse de vidange de l’auricule inférieure à 25 cm/s
témoignant d’une fibrillation ancienne avec altération sévère de la
contractilité auriculaire (B).
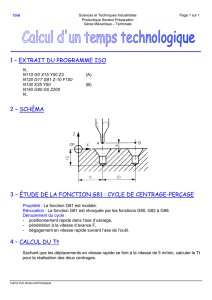
Arythmie complète sur sténose mitrale : aspect typique de contraste
spontané dense et de volumineux thrombus pédiculé barrant le collet
de l’auricule gauche.
A
B

La Lettre du Cardiologue - n° 341 - janvier 2001
24
Il convient de souligner plusieurs acquis fondamentaux de cette
étude :
✔La taille de l’auricule gauche n’intervient pas comme facteur
pronostique, à la différence de sa fonction contractile.
✔Il existe une liaison étroite entre les trois marqueurs de la stase
auriculaire gauche : l’altération sévère de la contractilité auricu-
laire engendre le contraste spontané (traduction échographique
du bas débit local) et favorise la thrombogenèse.
✔Il existe une corrélation entre la densité du contraste spontané
et la thrombogenèse : un thrombus est présent chez 24 % des
patients avec contraste dense, 10 % des patients avec contraste
faible, et chez 3 % des patients sans contraste.
✔La prévalence du contraste spontané dense est identique dans
les cinq catégories cliniques de patients (chez l’hypertendu aussi
bien que chez l’insuffisant cardiaque).
✔Si le pourcentage global de thrombus apparaît relativement
bas (10 %) dans cette étude, cela tient à la date du contrôle ETO,
intervenant 23 jours en moyenne après le début du traitement,
et à l’effet favorable de la warfarine : ce taux est de 6 % chez les
patients soumis à warfarine avec INR entre 2 et 3 versus 14 %
chez les patients du groupe 2 soumis à un traitement combiné
avec INR < 1,5.
L’absence de thrombus constitue un élément pronostique émi-
nemment favorable puisque le taux d’AVC y est de 2,3 % par an
(versus 17,9 % par an en présence de thrombus).
✔Cette étude souligne pour la première fois le rôle des plaques
aortiques complexes dans la genèse des AVC dans une popula-
tion de FA non valvulaire : les patients avec plaques complexes
ont un risque relatif d’AVC quadruple par rapport à ceux qui en
sont dépourvus.
✔La plaque aortique complexe et le contraste spontané dense
apparaissent comme les deux facteurs indépendants d’accident
thromboembolique en analyse multivariée. Leur conjonction
expose au risque d’AVC le plus fort (20,5 % par an), leur absence
au risque le plus faible (1,3 % par an).
✔La warfarine réduit de 75 % le risque thromboembolique des
plaques aortiques complexes et des thrombus intra-auriculaires
gauches. Elle agit donc favorablement sur les deux mécanismes
d’AVC retrouvés dans cette étude.
✔Point sans doute le plus important : l’ETO apparaît dans cette
étude comme l’outil le plus discriminant de stratification du risque
thromboembolique du patient en FA :
– elle permet une évaluation du risque propre à chaque patient
sur des critères précis et quantifiés ;
– comme l’ETT, et plus encore que lui, elle corrige les approxi-
mations de l’évaluation clinique : c’est ainsi que 32 % des
patients de cette étude par définition dits à haut risque (et justi-
fiant a priori un traitement anticoagulant) se situent en fait après
ETO dans la catégorie à bas risque (car sans signe de stase auri-
culaire ni plaque aortique complexe) et ne relèvent que de l’as-
pirine.
C’est là, à n’en pas douter, la principale justification de l’ETO
dans la prise en charge de toute ACFA au long cours.
Le tableau III résume les trois étapes de l’appréciation du risque
thromboembolique de la FA.
L’ACFA compliquée d’AVC
Rappelons que la FA représente à elle seule 45 % des causes
d’AVC d’origine cardioembolique.
a. Le rôle de la thrombose auriculaire dans la physiopatho-
logie des accidents thromboemboliques des patients en ACFA
a bien été mis en lumière par les travaux de Manning (11) : 45 %
des patients avec FA récente compliquée d’un accident throm-
boembolique ont un thrombus auriculaire gauche résiduel démon-
tré à l’ETO. De même, elle est retrouvée dans le travail de Stod-
dard (12) sur une population de 317 patients en FA compliquée
d’un événement thromboembolique récent :
– dans le groupe à FA récente (n = 143) de moins de 3 jours, on
retrouve 14 % de thrombus auriculaire gauche ;
– dans le groupe à FA chronique (n = 174), on retrouve 27 % de
thrombus ;
– dans les deux groupes, 50 % de ces thrombus sont mobiles.
L’ETO est incontournable pour visualiser ces thrombus.
La thrombose auriculaire gauche ne résume cependant pas le
mécanisme de l’AVC dans la FA.
b. Dans le registre lausannois des AVC (13) concernant
159 patients avec infarctus cérébral et FA :
– 13 % avaient une HTAet un petit infarctus profond au scanner,
– 11 % avaient une sténose ou une occlusion carotidienne ipsi-
latérale,
– 56 % avaient des lésions carotidiennes mineures ipsilatérales,
– 14 % avaient une autre source cardiaque d’embolie.
Dans 18% des cas seulement, la FA était la seule cause d’AVC.
c. Depuis cette étude datant de 1990 (13), est apparu un nou-
veau responsable de l’AVC : l’athérome aortique.
Les travaux anatomiques d’Amarenco, en 1992 (14), ont été les
premiers à démontrer le rôle des plaques aortiques ulcérées dans
la genèse des AVC. Depuis lors, de nombreuses études basées sur
l’ETO (15, 16, 17) ont confirmé pleinement ce rôle, les plaques
aortiques complexes étant retrouvées trois fois plus souvent chez
D
OSSIER
Tableau III. Appréciation du risque thromboembolique de la FA.
Haut risque : AVK Bas risque : aspirine
Clinique
●RM - prothèse mitrale
●Antécédents thromboemboliques ●Pas de facteur de risque clinique
●Insuffisance cardiaque =
IDM - CMD
●Cardiopathie hypertensive
●Diabète - Cardiothyréose
●Femme > 75 ans
ETT
●Dysfonction VG Normal
●Dilatation OG
ETO
●Thrombus OG/AG
●Contraste spontané Normal
●Vitesse de vidange < 25 cm/s
●Plaques aortiques ≥4 mm
VG : ventricule gauche ; AG : auricule gauche ; OG : oreillette gauche.

La Lettre du Cardiologue - n° 341 - janvier 2001
25
les patients ayant souffert d’AVC que chez les témoins sans AVC
(27 % versus 9 % dans le travail de Tunick).
La localisation de la plaque ainsi que ses caractéristiques propres
(épaisseur supérieure à 4 mm, ulcération, présence d’un throm-
bus ou d’un débris mobile) conditionnent son potentiel throm-
boembolique (18).
On le voit, la pathogénie de l’AVC dans la FAn’est pas univoque
et ne se résume pas au thrombus auriculaire. C’est pourquoi un
bilan complet s’impose comportant, outre le scanner, l’ETO au
même titre que l’écho doppler carotidien et transcrânien. C’est à
ce prix que l’on ne passera pas à côté de lésions potentiellement
accessibles à un geste chirurgical et que l’on ne conclura pas trop
vite à la responsabilité exclusive de la FA.
CONCLUSION
L’ETT est un examen indispensable pour toute FA :
– elle éclaire largement son étiologie,
– elle précise son retentissement sur les cavités auriculaires et la
petite circulation,
– elle permet de rationaliser les indications et les contre-indica-
tions du choc électrique.
L’ETO ne fait pas encore l’unanimité quant à son rôle et ses indi-
cations dans la prise en charge de l’ACFA.
Elle s’impose dans l’ACFA compliquée d’AVC pour en com-
prendre la pathogénie, souvent complexe, et en guider le traite-
ment.
Elle s’impose également pour l’évaluation rigoureuse du risque
thromboembolique d’une ACFA chronique non valvulaire, car
elle seule peut guider le choix difficile entre AVK et aspirine : les
critères cliniques sont trop imprécis pour fonder un choix théra-
peutique de cette importance.
Elle s’impose dans l’ACFA valvulaire de la sténose mitrale et
autorisera la dilatation percutanée en l’absence de thrombus.
Elle ne s’impose pas, en revanche, avant réduction de l’ACFA
récente, puisque l’étude ACUTE renvoie dos à dos les deux stra-
tégies de prise en charge possibles. ■
RÉFÉRENCES BIBLIOGRAPHIQUES
1. Kannel W, Abbott R, Savage D, MC Namara P. Epidemiologic features of chro-
nic atrial fibrillation. The Framingham study. N Engl J Med 1982 ; 306 : 1018-
22.
2. Tribouilloy C, Lucas G, Rey JL et al. Échocardiographie transœsophagienne
avant cardioversion électrique pour trouble du rythme supra-ventriculaire. La
Presse médicale 1998 ; 27, 3 : 106-9.
3. Elderly patients do not have an excessive risk for complications or recurrence
following transesophageal echocardiography-guided cardioversion of atrial
arrhythmias : results from the ACUTE registry. J Am Coll Cardiol 2000 ; 35 :
2 (suppl. A), 119A.
4. Manning WJ, Leeman DE, Gotch PJ, Come PC. Pulsed Doppler evaluation of
atrial mechanical function after electrical cardioversion of atrial fibrillation.
J Am Coll Cardiol 1989 ; 13 : 617-23.
5. Grimm RA, Stewart WJ, Maloney JD et al. Impact of electrical cardioversion
for atrial fibrillation on left atrial appendage function and spontaneous echo
contrast : characterization by simultaneous transesophageal echocardiography.
J Am Coll Cardiol 1993 ; 22 : 1359-66.
6. Wolf PA, Abbott RD, Kannel WB. Atrial fibrillation as an independent risk fac-
tor : The Framingham study. Stroke 1991 ; 22 : 983-8.
7. Kopecky SL, Gersh BJ, Phil CBD et al. The natural history of lone atrial fibril-
lation. A population based study over three decades. N Engl J Med 1987 ; 317 :
669-74.
8. Stroke Prevention in Atrial Fibrillation investigators, Stroke Prevention in
Atrial Fibrillation study. Final results. Circulation 1991 : 84 : 527-39.
9. Predictors of thromboembolism in atrial fibrillation : II. Echocardiographic
features of patients at risk. The Stroke Prevention in Atrial Fibrillation
Investigators. Ann Intern Med 1992 ; 116 : 6-12.
10. Transesophageal echocardiographic correlates of thromboembolism in high-
risk patients with nonvalvular atrial fibrillation. The Stroke Prevention in Atrial
Fibrillation investigators committee on echocardiography. Ann Intern Med 1998 ;
128 : 639-47.
11. Manning WJ, Silverman DI, Keighley KS et al. Prevalence of residual left
atrial thrombi among patients with acute thromboembolism and newly recognized
atrial fibrillation. Arch Intern Med 1995 ; 155 : 2193-7.
12. Stoddard M. Left atrial appendage thrombus is not uncommun in patients
with acute fibrillation and a recent embolic event. JACC 1995 ; 25 : 452.
13. Bogousslavsky J, Vanmelle G, Regli F et al. Pathogenesis of anterior circu-
lation stroke in patients with non valvular atrial fibrillation : The Lausanne
Stroke registry. Neurology 1990 ; 40 : 1046-50.
14. Amarenco P, Duyckaerts C, Tzourio C et al. The prevalence of ulcerated
plaques in the aortic arch in patients with stroke. N Engl J Med 1992 ; 332 : 221-5.
15. Di Tullio MR, Sacco RL, Gersony D et al. Aortic atheromas and acute ische-
mic stroke : a transesophageal echocardiographic study in an ethnically mixed
population. Neurology 1996 ; 46 : 1560-6.
16. Tunick PA, Perez JL, Kronzon I. Protruding atheromas in the thoracic aorta
and systemic embolization. Ann Intern Med 1991 ; 115 : 423-7.
17. Nihoyannopoulos P, Joshi J, Athanasopoulos G et al. Detection of athero-
sclerotic lesions in the aorta by transesophageal echocardiography. Am J Cardiol
1993 ; 71 : 1208-12.
18. Cohen A, Tzourio C, Bertrand B et al. Aortic plaque morphology and vascu-
lar events : a follow-up study in patients with ischemic stroke. Circulation 1997 ;
96 : 3838-41.
D
OSSIER
Autoquestionnaire FMC
voir page 26
☛
 6
6
1
/
6
100%