Lire l'article complet

MISE AU POINT
100
La Lettre du Pneumologue - Volume IX - no3 - mai-juin 2006
L
es amyloses représentent un groupe hétérogène de
pathologies associées à un dépôt protéique sous
forme fibrillaire anormale. Elles sont héréditaires ou
acquises, localisées ou systémiques, potentiellement létales ou
asymptomatiques. L’incidence est estimée à 12 cas par million
par an (1). Les étiologies varient selon le type d’amylose. Les
plus connues sont le myélome multiple (2) et les infections res-
piratoires chroniques : bronchectasies et tuberculose chronique
(3), mais aussi toutes les pathologies inflammatoires chroniques
(4) ou, plus rarement, cancéreuses (1). La fréquence respective
des étiologies varie selon les pays : les dysglobulinémies pré-
dominent dans les pays occidentaux alors que les causes inflam-
matoires sont encore au premier plan en Turquie ou en Inde (3).
Le diagnostic est histologique par la démonstration de la pré-
sence dans le tissu atteint de dépôts amyloïdes : dépôts
amorphes, protéiques, éosinophiles, caractérisés par une biré-
fringence jaune vert en lumière polarisée (dichroïsme) quand
ils sont colorés au rouge Congo (1). En microscopie électro-
nique, quelle que soit la nature du précurseur protéique, l’ultra-
structure observée est identique : des feuillets fibrillaires régu-
liers de 100 Å, sans embranchement, avec un croisement bêta.
Cette structure explique leurs propriétés physicochimiques :
résistance relative à la protéolyse, liaison selon une organisa-
tion spatiale au rouge Congo et liaison au composant sérique
amyloïde P (SAP) [2].
Amyloses thoraciques
Thoracic amyloidosis
●
A. Hamzaoui*, H. Ghrairi*
* Pavillon B, hôpital Abderrahmen-Mami de pneumologie, Ariana, Tunisie.
Résumé : Les amyloses sont dues à des dépôts de protéines sous forme fibrillaire. Leur diagnostic est histologique. Elles consti-
tuent un groupe hétérogène par la multiplicité de leurs étiologies et la diversité des manifestations cliniques. Elles sont clas-
sées selon la nature du précurseur protéique. Les manifestations respiratoires sont associées aux amyloses AL. Les localisa-
tions laryngées et trachéobronchiques représentent essentiellement des amyloses localisées et sont constituées de nodules,
de plaques sous-muqueuses ou d’épaississement diffus d’aspect très évocateur en tomodensitométrie. Deux types d’atteintes
parenchymateuses sont possibles : nodulaires dans les amyloses localisées, et interstitielles diffuses dans les amyloses sys-
témiques. Des dépôts amyloïdes ganglionnaires et pleuraux sont souvent associés aux atteintes pulmonaires. Les biopsies
transbronchiques et transpariétales sont utiles à la confirmation histologique. L’identification de la protéine anormale est indis-
pensable au choix thérapeutique. Le traitement des amyloses systémiques AL associe chimiothérapie agressive et greffe de cel-
lules souches. Les atteintes trachéobronchiques symptomatiques requièrent un traitement endoscopique. Les localisations
parenchymateuses isolées ne nécessitent pas de résection chirurgicale.
Mots-clés : Amylose - Nodules - Trachée - Poumon - Plèvre - Diagnostic - Traitement.
Summary: Amyloidosis is a heterogeneous group of disorders associated with deposition of protein in an abnormal fibrillar form.
A pathological confirmation is required. Classification is based on the nature of the precursor protein. Localised AL amyloido-
sis involves upper and lower respiratory tracts in various ways: isolated nodules, multifocal submucosal plaques or diffuse infil-
tration. CT findings are highly suggestive. Lung parenchymal deposits constitute either nodules (multiple or solitary) in locali-
sed amyloidosis or diffuse infiltrative lesions often associated with systemic amyloidosis. Lymph nodes and pleura are also
amyloidosis sites. Transbronchial and transcutaneous biopsies are helpful. Identification of amyloid type is necessary before
treatment decision. Management of primary systemic amyloidosis relays on high dose chemotherapy and autologous stem-cell
transplantation with a median survival of 4.6 years. Symptomatic airways amyloidosis requires endoscopic treatment. Pulmo-
nary nodules deserve no treatment.
Keywords: Amyloidosis - Nodular - Trachea - Lung - Pleura - Diagnosis - Treatment.

101
LA COMPOSITION DES DÉPÔTS AMYLOÏDES
EST DÉTERMINANTE, LE TYPAGE DE L’AMYLOSE
EST INDISPENSABLE
La composition des dépôts amyloïdes associe des protéines par-
ticulières à l’étiologie, formées de molécules entières ou de frac-
tions protéiques et des composants constants dont l’importance
a été démontrée chez l’animal : le facteur amyloid enhancing, des
glycosaminoglycanes (GAG) et le SAP. L’injection parentérale
de concentrations minimes d’extraits de tissus amyloïdes favo-
rise chez la souris le développement explosif d’une amylose AA.
Les GAGS, héparane sulfate et dermatane sulfate, augmentent
l’amylogenèse. Le SAP glycoprotéine sérique forme jusqu’à 15%
des dépôts, contribuant à leur stabilité. Ces molécules constantes
sont la cible d’essais thérapeutiques, et le SAP est utilisé comme
marqueur scintigraphique. Les dépôts amyloïdes se renouvellent
continuellement par l’apport de nouveaux substrats. Il est donc indis-
pensable d’identifier la molécule précurseur pour envisager l’inhi-
bition de sa production : l’arrêt de l’apport des précurseurs pro-
téiques provoque la régression des dépôts amyloïdes (1, 2, 5, 7).
Les formes héréditaires, bien que rares, telles que celles liées à
une mutation du lysozyme, ont permis de décrire la pathogénie
des dépôts amyloïdes : les protéines mutées moins stables que
les protéines originelles forment in vitro des fibrilles amyloïdes
après chauffage ou refroidissement. Ces fibrilles forment spon-
tanément des agrégats en réseau parfaitement ordonné sur lequel
vont s’accrocher les autres constituants. Ce processus est com-
plètement réversible (2).
Les dépôts s’accumulent dans les espaces extracellulaires. La
toxicité des dépôts amyloïdes est en partie mécanique par enva-
hissement et destruction de l’architecture tissulaire, mais aussi
secondaire à un effet cytotoxique par induction d’apoptose (2, 5).
La classification actuelle est fondée sur les précurseurs pepti-
diques. L’amylose AA est liée au dépôt de protéine SAA au cours
des inflammations chroniques, et l’amylose AL à des fragments
de chaînes légères d’immunoglobulines G (k ou l) associés dans les
formes diffuses à une gammapathie bénigne ou à un myélome (5).
Les amyloses ATTR, familiale et sénile, sont dues à une accu-
mulation de transthyrétine (tableau I).
L’amylose AA secondaire à une inflammation chronique était
classiquement une complication des dilatations de bronches et
des tuberculoses chroniques. C’est encore le cas dans les séries
turques. Elle est désormais plus souvent associée aux patholo-
gies rhumatismales, particulièrement la polyarthrite rhumatoïde.
Elle provoque un syndrome néphrotique, un orthostatisme et une
hépatosplénomégalie. Les atteintes pulmonaires sont très rares (2).
L’amylose AL peut être localisée, liée à une prolifération lym-
phoplasmocytaire locale à proximité des dépôts amyloïdes. Les
formes localisées touchent les voies aériennes, les tractus géni-
tal ou digestif, la peau et les orbites. Les formes diffuses sont pro-
voquées par des chaînes légères monoclonales circulantes pro-
duites par une dyscrasie plasmocytaire médullaire clonale de bas
grade. Dans 20 % des cas, un myélome multiple est présent. Les
dépôts sont disséminés, l’atteinte des différents organes est très
hétérogène. Des dépôts occultes, asymptomatiques, se manifes-
tent cliniquement sous l’effet du stress secondaire à des inter-
ventions chirurgicales, des infections ou des défaillances orga-
niques. Les atteintes silencieuses de découverte autopsique sont
très fréquentes (1, 2, 5).
LES MANIFESTATIONS CLINIQUES
SONT TRÈS HÉTÉROGÈNES
Les atteintes pulmonaires sont rares : la série de la Mayo Clinic
a regroupé 55 patients en 14 ans (6). Deux types de circonstances
conduisent à la découverte par le pneumologue d’une atteinte
amyloïde : la présence d’anomalies parenchymateuses ou pleu-
rales dans l’évaluation de l’extension d’une amylose systémique
connue, et le diagnostic d’une atteinte trachéobronchique ou
parenchymateuse isolée correspondant à une amylose localisée.
Les tableaux cliniques évocateurs d’amyloses systémiques sont
très variés. Les symptômes les plus évocateurs au cours de ces
amyloses sont l’hématome périorbitaire en lunette, typique par
l’absence de tuméfaction et par la discrétion du traumatisme
déclenchant, la macroglossie avec des empreintes dentaires
(19 %), le syndrome du canal carpien (25 %), et la neuropathie
du système nerveux autonome responsable d’une hypotension
orthostatique (18 %) et de satiété précoce. De même, un amai-
grissement (49 %), un syndrome néphrotique (34-55 %), mais
aussi une neuropathie sensitive (18 %), des éruptions cutanées
ou une hépatosplénomégalie (34 %) peuvent constituer des
signes d’appel (1, 2, 5, 7-9). Parmi les atteintes thoraciques,
l’amylose cardiaque représente la localisation la plus fréquente au
cours des amyloses systémiques AL et ATTR (47-54 %) [8, 9].
Elle conditionne le pronostic de la maladie. Les dépôts provo-
quent un épaississement important et concentrique du myocarde
ainsi qu’une insuffisance cardiaque rapidement progressive, avec
de bruyantes manifestations droites. Électriquement, un bas vol-
tage diffus est évocateur. L’échographie objective un aspect scin-
tillant des dépôts au sein du myocarde (2, 10).
Les atteintes respiratoires sont principalement observées au cours
des amyloses AL (7) [tableau II]. L’atteinte des voies aériennes :
larynx, trachée et bronches ainsi que les dépôts intraparenchy-
mateux nodulaires représentent des formes localisées AL, alors
La Lettre du Pneumologue - Volume IX - no3 - mai-juin 2006
(5).
ApoSAA Réactionnelle :
(composant sérique P) infections, inflammations
chroniques, tumeurs,
maladie périodique,
syndrome de Mückle-et-
Wells
Chaîne légère d’Ig (k, l) Idiopathique, (primitive),
associée au myélome ou à
la maladie de Waldenström
Chaîne lourde d’Ig (g)
Transthyrétine mutée Héréditaire
Transthyrétine normale Sénile

MISE AU POINT
102
La Lettre du Pneumologue - Volume IX - no3 - mai-juin 2006
que les atteintes interstitielles et pleurales s’observent au cours
des amyloses AL systémiques. Les atteintes respiratoires inter-
stitielles diffuses des amyloses héréditaires ATTR et secondaires
AA sont asymptomatiques.
Deux grandes séries font référence : celle de la Mayo Clinic (6)
et celle de Cordier et al. (11). L’étude américaine fondée sur une
étude systématique de tous les cas d’amylose regroupait
55 patients porteurs de dépôts amyloïdes pulmonaires prouvés
histologiquement, dont 35 atteints d’amylose systémique primi-
tive (AL) et d’atteinte pulmonaire interstitielle diffuse (20 cas),
ou d’épanchements pleuraux (isolés dans 10 cas). Parmi les
formes localisées, 4 atteintes trachéobronchiques et 7 atteintes
nodulaires parenchymateuses étaient rapportées. Enfin, parmi les
patients souffrant d’une amylose secondaire, 4 présentaient des
infiltrats interstitiels des bases associés à des adénopathies hilaires
de découverte histologique (5). L’étude française décrivait
21 patients dont 5 atteints d’amylose trachéobronchique symp-
tomatique et multifocale dans 3 cas (sténoses, atélectasie), 2 amy-
loses nodulaires parenchymateuses et 15 atteintes interstitielles
(11). Dans un cas d’amylose familiale, il existait un syndrome
interstitiel asymptomatique (11).
Les atteintes des voies aériennes représentent des formes locali-
sées AL. L’amylose laryngée constitue 0,5 à 1 % des pathologies
laryngées bénignes (7). Sa fréquence augmente avec l’âge. Elle
a aussi été observée chez l’adulte jeune. Les dépôts amyloïdes
affectent le larynx sus-glottique, provoquant un enrouement, un
stridor, une dyspnée dans 75 % des cas avec une sensation de plé-
nitude pharyngée ou d’étouffement. Des hémorragies fatales sont
possibles. Une atteinte trachéobronchique, concomitante ou non,
s’y associe une fois sur deux. Le diagnostic est suggéré à l’endo-
scopie par la visualisation de nodules typiques d’aspect pavi-
menteux (47 %), de plaques sous-muqueuses, d’un épaississement
pariétal circonférentiel (28 %), ou d’un aspect pseudo-tumoral
(7, 12).
L’amylose trachéobronchique est rare. Jusqu’en 1983, 67 cas
avaient été décrits : 57 patients souffraient d’une atteinte infil-
trative diffuse par de multiples plaques sous-muqueuses ; dans
les autres cas, il s’agissait de nodules suggérant une néoplasie
dans les formes isolées. Cette pathologie se manifeste plus fré-
quemment au-delà de 50 ans, directement par une dyspnée, une
toux ou des hémoptysies, ou indirectement par les conséquences
de l’obstruction bronchique : atélectasie, pneumonies récidi-
vantes. Le pronostic varie selon les séries : bon dans celle de Cor-
dier, avec une survie au-delà de 8 ans de 3 patients sur 4 (11), et
mauvais dans celle de Hui : 3 décès (sur 7 patients) par insuffi-
sance respiratoire ou pneumonie (13), ainsi que celle de la Mayo
Clinic : décès de 75 % des patients à 79 mois (5). En tomoden-
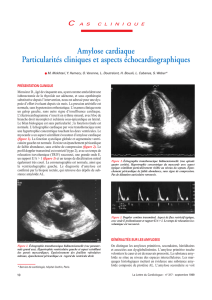
sitométrie, les images sont très suggestives : épaississement
concentrique régulier ou nodulaire de la paroi trachéale sous-
muqueuse, calcifications concentriques (incluant la paroi posté-
rieure) ou en foyers, indépendantes du cartilage, sans malacie
(14, 15) [figure 1].
Les atteintes parenchymateuses
sont les plus fréquemment rap-
portées sous deux formes :
nodulaires pseudo-tumorales et
infiltratives (16).
Les formes nodulaires sont le
plus souvent multiples, asymp-
tomatiques (17) et correspon-
dent à une amylose AL locali-
sée bien que quelques
observations aient été rappor-
tées au cours d’amyloses systé-
miques AL (18). Ce sont en
général des nodules périphé-
riques à contours lisses ou lobu-
lés, sous-pleuraux, prédomi-
nant aux bases, à croissance
lente, pouvant s’excaver ou se
calcifier (19). Leur taille varie
de quelques millimètres à plusieurs centimètres. Les opacités ont
une vitesse de croissance similaire. Le développement asynchrone
d’un nodule nécessite une vérification histologique pour élimi-
ner un cancer (20).
Les tumeurs amyloïdes solitaires (amyloïdomes) sont rares. Elles
représentent des amyloses primitives localisées (21). Elles ont aussi
été associées au syndrome de Sjögren et à des lymphomes pulmo-
naires B de bas grade (22). Le diagnostic est anatomopathologique.
Les atteintes parenchymateuses interstitielles diffuses, nodulaires
ou réticulonodulaires, relativement fréquentes au cours des amy-
loses systémiques (28 %), sont le plus souvent asymptomatiques
[7]
Nodulaire ou infiltrative diffuse, généralement localisée
Nodulaire ou infiltrative diffuse, généralement localisée
– nodulaire Nodules solitaires ou multiples/amyloïdome, souvent limitée
– diffuse Pneumopathie infiltrative diffuse
Adénomégalies hilaires ou médiastinales
Découverte le plus souvent histologique
Figure 1. Aspect tomodensitomé-
trique d’une atteinte des gros troncs
bronchiques : calcifications cir-
conférentielles de la trachée (a) et
de la bronche souche gauche (b).
a
b
.../...

MISE AU POINT
104
La Lettre du Pneumologue - Volume IX - no3 - mai-juin 2006
(7, 23). La cardiopathie présente dans la majorité des atteintes
pulmonaires (91 %) domine le pronostic (20). Parmi les
15 atteintes interstitielles rapportées par Cordier et al., seules 2
ont provoqué le décès par insuffisance respiratoire mortelle (11).
Ces lésions parenchymateuses diffuses étaient de découverte
autopsique dans 10 cas, dont 8 présentaient une insuffisance car-
diaque gauche et 3 étaient associées à une néoplasie. La gêne res-
piratoire était corrélée à l’extension des dépôts dans les zones
d’échange (11). Des hémoptysies par dissection des artères pul-
monaires ainsi que des embolies massives ont été rapportées (20).
En tomodensitométrie, les anomalies associent nodules (75 %),
verre dépoli (38 %), opacités linéaires irrégulières, épaississe-
ment des septums interlobulaires (75 %) et rayons de miel (38 %)
(19). Les fibrilles amyloïdes ayant une forte affinité pour le cal-
cium, des calcifications parenchymateuses sont visibles dans 20 %
des cas, particulièrement dans les régions sous-pleurales des zones
moyennes et inférieures (24). Le lavage bronchiolo-alvéolaire
(LBA) serait d’un apport diagnostique intéressant en révélant une
alvéolite lymphocytaire, avec un rapport CD4/CD8 élevé, asso-
ciée à du matériel amorphe éosinophile ; une paraprotéine IgG 1
a été identifiée dans le surnageant (25). Quelques cas d’amylose
localisée avec infiltration interstitielle ont été rapportés, suggé-
rant la recherche systématique d’une amylose au cours des pneu-
mopathies interstitielles diffuses (7). Ces formes localisées pro-
voquent le décès dans 1 cas d’insuffisance respiratoire sur 2 (20).
Dans les formes systémiques AL, les atteintes ganglionnaires
hilaires et médiastinales fréquentes (75 % des cas) sont associées
une fois sur deux aux atteintes interstitielles, mais elles peuvent
être isolées. Le diagnostic peut alors être posé par ponction biop-
sie sous tomodensitométrie (7, 26, 27). Elles ont été exception-
nellement observées au cours des amyloses secondaires à une
fièvre familiale méditerranéenne (20).
Les épanchements pleuraux représentent une manifestation tho-
racique fréquente des amyloses AL. Elles sont souvent associées
à une amylose cardiaque. Transsudatives ou exsudatives, de cel-
lularité panachée, elles ont un impact négatif sur la survie quand
elles résistent aux diurétiques et aux évacuations répétées. Elles
sont dues à l’infiltration amyloïde des feuillets pleuraux, et la biop-
sie pleurale peut être diagnostique. Une pleurodèse est nécessaire
à l’amélioration symptomatique (28, 29).
L’hypertension pulmonaire est une complication rare et tardive des
amyloses : 5 patients identifiés en 20 ans dans la série de la Mayo
Clinic, parmi lesquels 4 souffraient d’une amylose AL et 1 d’une
amylose AA secondaire à une fièvre familiale méditerranéenne.
Elle témoigne d’une amylose très évoluée (découverte en moyenne
deux mois avant le décès), envahissant les artères pulmonaires (30).
Enfin, un cas d’amylose diaphragmatique avec myopathie a été
décrit (31).
LE DIAGNOSTIC EST HISTOLOGIQUE,
LE TYPAGE INDISPENSABLE
Le diagnostic positif d’amylose nécessite une confirmation his-
tologique. Le type d’atteinte pulmonaire suggère l’amylose en
cause. Les pneumopathies interstitielles nécessitent un bilan
poussé d’amylose systémique. Un bilan biologique de base
apporte des arguments évocateurs : une discrète anémie, une
vitesse de sédimentation accélérée malgré une protéine C réac-
tive (CRP) normale, une baisse du rapport normalisé internatio-
nal (INR), du facteur X ou une protéinurie (1). D’autres sites sont
éventuellement à biopsier si l’amylose n’est pas connue : les plus
recommandés, car faciles d’accès, sont la graisse sous-cutanée
périombilicale, prélevée par ponction, les glandes salivaires
accessoires et la muqueuse rectale (1, 6). Les trois prélèvements
peuvent être associés pour augmenter la rentabilité. Les biopsies
hépatiques sont contre-indiquées à cause d’un risque hémorra-
gique important (1, 2). L’évaluation de l’extension systémique
de l’amylose peut s’appuyer sur la scintigraphie au SAP marqué
à l’iode 123, qui se fixe sur les dépôts amyloïdes (1, 32). Cet exa-
men permet aussi de surveiller l’évolution de la maladie. La spé-
cificité de la scintigraphie en ferait selon certains un outil dia-
gnostique positif. Le marquage est très faible dans les poumons,
mais la tomodensitométrie par émission de positons serait alors
intéressante : les dépôts amyloïdes pulmonaires auraient un mar-
quage intense (33). Pour les amyloses respiratoires basses loca-
lisées, trachéobronchiques ou nodulaires parenchymateuses, les
biopsies bronchiques, transbronchiques, avec un risque de sai-
gnement modéré acceptable, et transpariétales guidées par tomo-
densitométrie permettent la confirmation du diagnostic d’amy-
lose (34). Les dosages préalables de l’INR et du facteur X sont
obligatoires.
L’identification de la protéine précurseur est indispensable (35).
Elle se fait à deux niveaux : tissulaire sur les biopsies par immu-
nohistochimie avec des anticorps vis-à-vis des chaînes légères
d’immunoglobulines (AL), de la protéine SAA et de la transthy-
rétine, et systémique sanguin (ou urinaire) par immunoélectro-
phorèse, à la recherche de chaînes légères d’immunoglobulines.
L’élimination d’une amylose AL est suivie d’une étude de l’ADN
des gènes TTR. L’absence de mutation suggère une étiologie
secondaire (AA) [1].
IL EXISTE DE RÉELLES POSSIBILITÉS THÉRAPEUTIQUES
L’intérêt actuel pour les amyloses est secondaire aux possibili-
tés thérapeutiques.
L’arrêt de l’apport des protéines précurseurs permet la régres-
sion des dépôts. Pour cela, dans les formes systémiques AL, une
chimiothérapie agressive est proposée (36), associant du mel-
phalan à fortes doses (100-200 mg/m2) et une greffe autologue
de cellules souches (37). Sur 701 patients, 50 % étaient éligibles
pour ce traitement. À cent jours, la mortalité était élevée (13 %),
mais la médiane de survie était de 4,6 ans, encore meilleure chez
les patients avec réponse hématologique complète (40 % des cas).
Une régression des atteintes organiques évoluées, pulmonaire,
cardiaque et rénale, est possible (37) [figure 2]. Les amyloses
AA sont traitées quand cela est possible par interruption de
l’inflammation : résection des sites infectieux chroniques, chlo-
rambucil pour la polyarthrite rhumatoïde et l’arthrite chronique
juvénile (1, 38), et colchicine pour la fièvre familiale méditerra-
néenne (1, 39). Dans ce cadre, la colchicine empêche la forma-
.../...

105
La Lettre du Pneumologue - Volume IX - no3 - mai-juin 2006
tion de nouveaux dépôts et per-
met la régression de ceux déjà
établis. Les amyloses familiales
ATTR sont “guéries” par des
greffes hépatiques, interrompant
la production de la protéine anor-
male (40).
Le second volet du traitement
est celui des symptômes et des
défaillances organiques. Des
transplantations rénales (6) et
cardiaques (10) ont été réali-
sées, mais avec un risque de
récidive sur l’organe greffé.
Les formes localisées relèvent
d’un traitement symptoma-
tique. Les amyloses laryngées
et trachéobronchiques bénéfi-
cient des techniques d’endo-
scopie interventionnelle : résec-
tion bronchoscopique des formations endoluminales par
pulvérisation au laser (CO2et NdYag) et prothèses (41). Ces
gestes, efficaces, requièrent un anesthésiste préparé aux risques
liés à la nature friable des dépôts obstruant les sondes d’intuba-
tion et les endoscopes, et au saignement (12). Une irradiation
externe est proposée par certains auteurs (42). Les résections chi-
rurgicales sont exceptionnelles. Les nodules amyloïdes paren-
chymateux ne nécessitent pas de résection chirurgicale dans la
plupart des cas.
EN PERSPECTIVE
Les perspectives thérapeutiques futures se fondent sur des agents
qui stabiliseraient les protéines précurseurs dans leur conforma-
tion normale, inhiberaient la formation des fibrilles et leur pro-
pagation, ou augmenteraient la dégradation fibrillaire (43, 44).
Les drogues à l’essai sont des composés GAG polysulfonés for-
tement chargés et les inhibiteurs de la liaison du SAP.
■
Remerciements au Pr H. Houman, service de médecine interne, hôpital
La Rabta, Tunis, pour les photographies de la figure 2 illustrant l’atteinte
pulmonaire et la réponse au traitement.
RÉFÉRENCES BIBLIOGRAPHIQUES
Khan MF, Falk RH. Amyloidosis. Postgrad Med J 2001;77:686-93.
Falk RH, Comenzo RL, Skinner M. The systemic amyloidosis. New Engl J
Med 1997;337:898-909.
Akçay S, Akman B, Ozdemir H, Eyüboglu FO, Karacan O, Ozdemir N. Bron-
chiectasis-related amyloidosis as a cause of chronic renal failure. Ren Fail
2002;24:815-23.
Tuglular S, Yalcinkaya F, Paydas S et al. A retrospective analysis for aetio-
logy and clinical findings of 287 secondary amyloidosis cases in Turkey.
Nephrol Dial Transplant 2002;17:2003-5.
Grateau G. Amyloses. Encycl Méd Chir (Elsevier, Paris) 1998;5-0390.
[Espace expert. Amylose_Infos. http://www.amylose.net/accueil.php]
Utz JP, Swensen SJ, Gertz MA. Pulmonary amyloidosis. The Mayo Clinic
Experience from 1980 to 1993. Ann Intern Med 1996;124:407-13.
Gillmore JD, Hawkins PN. Amyloidosis and the respiratory tract. Thorax
1999;54:444–51.
Kyle RA, Gertz MA, Greipp PR et al. Long-term survival (10 years or more)
in 30 patients with primary amyloidosis. Blood 1999;93:1062-6.
Pardanani A, Witzig TE, Schroeder G et al. Circulating peripheral blood
plasma cells as a pronostic indicator in patients with primary systemic amyloi-
dosis. Blood 2003;101:827-83.
Dubrey SW, Burke MM, Khaghani A, Hawkins PN, Yacoub MH, Banner
NR. Long term results of heart transplantation in patients with amyloid heart
disease. Heart 2001;85:202-7.
Cordier JF, Loire R, Brune J. Amyloidosis of the lower respiratory tract.
Clinical and pathologic features in a series of 21 patients. Chest
1986;90:827-31.
Minogue SC, Morrisson M, Ansermino M. Laryngo-tracheo-bronchial ste-
nosis in a patient with primary pulmonary amyloidosis: a case report and brief
review. Can J Anesthesia 2004;51:842-5.
Hui AN, Koss MN, Hochholzer L et al. Amyloidosis presenting in the
lower respiratory tract: clinicopathologic, radiologic, immunohistochemi-
cal, and histochemical studies on 48 cases. Arch Pathol Lab Med
1986;110:212-8.
Webb EM, Elicker BM, Webb RW. Using CT to diagnose non neoplastic tra-
cheal abnormalities. Appearance of the tracheal wall. AJR 2000; 174:1315-21.
Marom EM, Goodman PC, McAdams HP. Diffuse abnormalities of the tra-
chea and main bronchi. Am J Roentgenol 2001;176:713.
Liaw YS, Kuo SH, Yang PC, Chen CL, Luh KT. Nodular amyloidosis of the
lung and the breast mimicking breast carcinoma with pulmonary metastasis. Eur
Respir J 1995;5:871-3.
Boutemy-Baudouin M, Ribadeau-Dumas S, Aron C. Fortuitously discovered
lung nodules. Rev Pneumol Clin 2003;59:325-7.
Beer TW, Edwards CW. Pulmonary nodules due to reactive systemic amy-
loidosis (AA) in Crohn’s disease. Thorax 1993;48:1287-8.
Pickford HA, Swensen SJ, Utz JP. Thoracic cross-sectional imaging of amy-
loidosis. Am J Roentgenol 1997;168:351-5.
Berk JL, O’Regan A, Skinner M. Pulmonary and tracheobronchial amyloi-
dosis. Semin Respir Crit Care Med 2002;23:155-65.
Leu CY, Lynch DA, Chan ED. The case of the torpid thoracic tumor. Chest
1997;112:535-7.
Ross P, Magro CM. Clonal light chain restricted primary intrapulmonary
nodular amyloidosis. Ann Thor Surg 2005;80:344-7.
Planes C, Kleinknecht D, Brauner M, Battesti JP, Kemeny JL, Valeyre D.
Diffuse interstitial lung disease due to AA amyloidosis. Thorax 1992;47:323-4.
Chan ED, Morales DV, Welsh CH, McDermott MT, Schwarz MI. Calcium
deposition with or without bone formation in the lung. Am J Respir Crit Care
Med 2002;165:1654-69.
Morgan JE, McCaul DS, Rodriguez FH, Abernathy DA, deShazo RD, Banks
DE. Pulmonary immunologic features of alveolar septal amyloidosis associated
with multiple myeloma. Chest 1987;92:704-8.
Conaghan P, Chung D, Vaughan R. Recurrent laryngeal nerve palsy asso-
ciated with mediastinal amyloidosis. Thorax 2000;55:436-7.
Hiller N, Fisher D, Shmesh O, Gottschalk-Sabag S, Dollberg M. Primary
amyloidosis presenting as an isolated mediastinal mass: diagnosis by fine needle
biopsy. Thorax 1995;50:908-9.
Berk JL, Keane J, Seldin DC et al. Persistent pleural effusions in primary
systemic amyloidosis. Etiology and prognosis. Chest 2003;124:969-77.
Kavuru MS, Adamo JP, Ahmad M, Mehta AC, Gephardt GN. Amyloidosis
and pleural disease. Chest 1990;98:20-3.
Dingli D, Utz JP, Gertz MA. Pulmonary hypertension in patients with amy-
loidosis. Chest 2001;120:1735-9.
Streeten EA, de la Monte SM, Kennedy TP. Amyloid infiltration of the dia-
phragm as a cause of respiratory failure. Chest 1986;89:760-2.
Hachulla E, Grateau G. Moyens paracliniques du diagnostic des amyloses.
Rev Rhum 2002;69:1172-80.
Figure 2. Atteinte macronodulaire
parenchymateuse, réponse à la chi-
miothérapie : avant traitement (a),
après traitement (b).
a
b
 6
6
1
/
6
100%