Leucodystrophie consécutive à une hypomyélinisation : pas seulement une pathologie de l’enfant !

CAS CLINIQUE
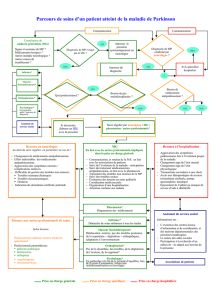
▲ Figure 1.
A. Radiographie du rachis dorsal de profil : cyphose thoracique, dystro-
phies rachidiennes, platyspondylie, irrégularité des plateaux vertébraux.
B. Radiographie du crâne de profil : microcrânie, prognathisme avec
rétromaxillaire discret, épaississement de la diploé.
A B
62 | La Lettre du Neurologue • Vol. XVII - n° 2 - février 2013
Mots-clés
Maladie de Salla – Leucodystrophie – Récessif – Hypomyélination
Keywords
Salla’s disease – Leucodystrophy – Ressive inheritance – Hypomyelination
Leucodystrophie consécutive
à une hypomyélinisation :
pas seulement une pathologie
de l’enfant !
Hypomyelination and leucodystrophy: not only a childhood
medical problem
A. Siri1, N. Menjot de Champfleur2, R. Froissard3, C. Carra-Dallière1, X. Ayrignac1, A. Corlobé1, B. Echenne4, P. Labauge1
1Département de neurologie, CHU de Montpellier. 2Service de neuroradiologie,
CHU de Montpellier. 3Laboratoire de génétique, CHU de Lyon. 4Service de neuro-
pédiatrie, CHU de Montpellier.
Observation
Un patient âgé de 34 ans est pris en charge dans le service de
neurologie pour un syndrome cérébelleux et des troubles du
comportement chroniques.
Alors que la grossesse de sa mère était normale, il a présenté
un retard psychomoteur – ne commençant à marcher que
vers 20 mois et chutant fréquemment –, puis une ataxie
cérébelleuse vers l’âge de 3 ans. Il a été scolarisé dans un
établissement spécialisé.
À l’âge adulte, il présente des hallucinations visuelles et
auditives, des tics moteurs, des troubles compulsifs, notamment
une potomanie. Il n’a pas d’antécédent familial notable,
notamment pas de consanguinité. La famille est originaire
du sud de la France.
L’examen neurologique objective une déficience mentale
sévère, une ataxie cérébelleuse statique, un syndrome
pyramidal et des rétractions tendineuses. On note également
un syndrome autistique avec évitement du regard, des tics
moteurs et une posture dystonique au niveau des mains.
L’examen général retrouve une cyphose thoracique et un
prognathisme.
Les radiographies osseuses mettent en évidence des anomalies
rachidiennes (cyphose thoracique, dystrophies rachidiennes
avec platyspondylie et irrégularité des plateaux vertébraux) et
crâniennes (microcrânie, prognathisme avec rétromaxillaire discret,
épaississement du diploé) [figure 1].
L’IRM cérébrale (figure 2) révèle une atrophie cortico-sous-corticale,
cérébelleuse et du corps calleux. La substance blanche sus-tento-
rielle est raréée avec un aspect d’hypomyélinisation sous-corticale
particulièrement visible sur les séquences en T2 en écho de spin (ES).
Un hypersignal marqué de la substance blanche est retrouvé sur les
séquences FLAIR.
Le bilan enzymatique révèle une augmentation de l’acide sialique libre
urinaire, également retrouvée sur une biopsie cutanée.

CAS CLINIQUE
▲ Figure 2. Une IRM cérébrale identifie un élargissement sulcal diffus ainsi qu’un élargissement du système ventriculaire ( A : séquence T1 ; B : séquence
FLAIR) en rapport avec une atrophie cortico-sous-corticale diffuse, intéressant les étages sus- et sous-tentoriels ( C : acquisition sagittale FLAIR,
atrophie du corps calleux [tête de flèche bleue] et atrophie cérébelleuse avec trop bonne visibilité des folia [flèche bleue]). L’ensemble de la substance
blanche apparaît hyperintense sur les séquences FLAIR ( C ) et T2 ES ( D et E ), en rapport avec une hypomyélinisation touchant les fibres arquées (“en U”)
[ F : séquence axiale T2 ES, tête de flèche orange].
A
D
B
E
C
F
La Lettre du Neurologue • Vol. XVII - n° 2 - février 2013 | 63

CAS CLINIQUE
American Academy of Neurology
SAN DIEGO
CALIFORNIE
16-23
MARS
2013
RETROUVEZ-NOUS À PARTIR DU 18 MARS SUR :
LUNDI MARDI MERCREDI
18 MARS 19 MARS 20 MARS
www.edimark.fr/ejournaux/AAN/2013
Site réservé aux professionnels de santé
Attention : les comptes-rendus de congrès ont pour objectif de fournir des informations sur l’état actuel de la recherche ; ainsi, les données
présentées seront susceptibles de ne pas être validées par les autorités françaises et ne doivent donc pas être mises en pratique. Ces infor-
mations sont sous la seule responsabilité des auteurs et du directeur de la publication qui sont garants de l’objectivité de cette publication.
Sous l’égide de La Lettre du Neurologue - Directeur de la publication : Claudie Damour-Terrasson - Rédacteur en chef : Pr Thibault Moreau
E-journal en direct
du 65th AAN 2013
21 MARS
21 MARS
JEUDI
ENVI-2013-02-092
Avec le soutien
institutionnel de
64 | La Lettre du Neurologue • Vol. XVII - n° 2 - février 2013
La mise en évidence d’une mutation hétérozygote composite
faux-sens − p.R57C (exon 2)/p.S202L (exon 4) − sur le gène de
la sialine SLC17A5, permet d’afrmer le diagnostic de maladie
de Salla.
Discussion
Les maladies de surcharge en acide sialique libre sont des
maladies de surcharge lysosomale, autosomiques récessives,
dues au défaut d’un transporteur de la membrane lysosomale
(la sialine) qui assure l’excrétion de l’acide sialique (ou acide
N-acétylneuraminique) du lysosome. Le spectre clinique est
étendu. Il existe des formes sévères néonatales (Infantile Sialic
acid Storage Disease [ISSD]) avec un tableau d’anasarque fœto-
placentaire in utero, ou congénitales avec une hypotonie, une
hépatosplénomégalie souvent associée à une ascite, un syndrome
dysmorphique (traits un peu grossiers, anomalies osseuses), un
retard mental et des convulsions.
Dans les formes congénitales, le décès survient généralement
avant l'âge de 5 ans (1). La forme modérée de la maladie, ou
maladie de Salla (OMIM 604369), débute dans la première
année de vie et est caractérisée par une hypotonie suivie d’une
spasticité, d’une ataxie, d’un retard psychomoteur et parfois de
traits épais. Ces patients atteignent rarement l’âge de 30 ans.
Une survie prolongée jusqu’à la sixième décennie est toutefois
possible. Une atteinte du système nerveux périphérique est mise
en évidence dans la moitié des cas (2).
Conclusion
Cette pathologie de transmission autosomique récessive est rare
et a été essentiellement décrite en Finlande, où la prévalence du
gène est estimée à 1 personne sur 40 de la population générale.
Le diagnostic biologique repose sur une excrétion urinaire accrue
d’acide sialique libre et une accumulation d’acide sialique libre dans
les broblastes. Le dosage de l’acide sialique peut être cependant
normal, le diagnostic pouvant alors être réalisé sur l’augmen-
tation de l’acide sialique en spectroscopie de masse dans le liquide
céphalorachidien (3). Le diagnostic est conrmé par la mise en
évidence d’une mutation homozygote ou hétérozygote composite
sur le gène de la sialine (SLC17A5), localisé en 6q14-15.
Aucun traitement spécique n’existe actuellement dans cette maladie.
La prise en charge est essentiellement symptomatique. ■
1. Lemyre E, Russo P, Melançon SB et al. Clinical spectrum of infantile free sialic acid
storage disease. Am J Med Genet 1999;82(5):385-91.
2. Varho T, Jääskeläinen S, Tolonen U et al. Central and peripheral nervous system
dysfunction in the clinical variation of Salla disease. Neurology 2000;55(1):99-104.
3. Mochel F, Engelke UF, Barritault J et al. Elevated CSF N-acetylaspartylglutamate
in patients with free sialic acid storage diseases. Neurology 2010;74(4):302-5.
Références bibliographiques
1
/
3
100%