Lire l'article complet

La Lettre du Cardiologue - n° 299 - septembre 1998
7
e 5econgrès d’échocardiographie-doppler de Grenoble
a abordé de très nombreux thèmes. Certains sujets ori-
ginaux ont été toutefois plus particulièrement traités.
Nous rapporterons ici les communications consacrées à la place
de l’échocardiographie dans les urgences cardiologiques, à
l’étude de la fonction auriculaire gauche par quantification acous-
tique, aux nouvelles indications de l’échographie-doppler de
stress, et enfin aux nouvelles techniques écho-doppler.
LES URGENCES EN ÉCHO-DOPPLER CARDIAQUE
Pathologies aiguës de l’aorte
Le Dr B. Bertrand (Grenoble) a rappelé que les dissections aiguës
constituaient une urgence extrême, avec une mortalité proche de
50 % durant les 24 premières heures. L’élément diagnostique clef
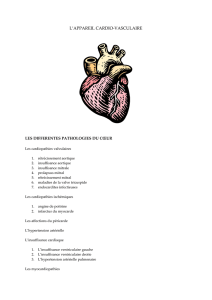
est la présence d’un voile intimal (figure 1), se présentant sous
la forme d’un écho linéaire anormal, noté dans plusieurs inci-
dences.
L’examen doit comporter une étude complète de l’aorte, s’aidant
du doppler couleur et pulsé. Les faux positifs sont constitués par
les artéfacts de réverbération (fréquents en cas de dilatation de
l’aorte), surtout si les parois sont épaissies et calcifiées, proches
du capteur ultrasonore (ETO), et par les artéfacts de réflexion
d’une structure extra-aortique. La présence de plaques d’athé-
rome peut également poser problème. Plus rarement, des abcès
ou des tumeurs, ainsi que la graisse péri-aortique ou un épan-
chement péricardique localisé au sinus de Theile, peuvent abusi-
vement faire conclure à la présence d’une dissection aortique.
Les faux négatifs, devant une scène clinique évocatrice, retrou-
vent souvent une pathologie aortique associée : anévrysme aor-
tique, athérome ulcéré, compression extrinsèque (tumorale), et
surtout hématome pariétal aortique. Ces hématomes pariétaux
sont responsables de tableaux cliniques souvent identiques aux
dissections aiguës. L’échographie ne retrouve pas de voile inti-
mal mais un épaississement pariétal caractéristique, circulaire
ou en croissant de plus de 7 mm, localisé à quelques centimètres,
mais parfois plus étendu. Son échostructure évoque un throm-
bus homogène, mais peut parfois être inhomogène en cas de
zones liquidiennes. Il est limité sur sa paroi interne par l’endo-
thélium aortique. L’évolution habituellement moins rapide que
celle des dissections classiques permet de réaliser des examens
complémentaires : scanner spiralé ou IRM. Dans l’expérience
grenobloise, le scanner est plus performant que l’ETO, et justi-
fie pleinement sa place de recours quand l’échographie n’a pas
abouti à une conclusion formelle, ou qu’elle a conclu à l’absence
de dissection.
Enfin, l’ETO joue un rôle capital dans les ruptures traumatiques
de l’aorte, survenant dans un tout autre contexte, en réanimation,
après traumatisme important avec décélération. L’anomalie siège
dans 95 % des cas au niveau de l’isthme, sous la forme d’un épais-
sissement localisé de la paroi aortique, avec rupture intimale, lan-
guette flottante souvent plus mobile qu’un flap, et flux doppler
de haute vélocité de part et d’autre de cette languette, associé à
un pseudo-anévrysme sur quelques centimètres. Dans un certain
nombre de cas, une collection péri-aortique peut être objectivée.
En pratique, l’ETO est d’un apport décisif dans ces pathologies
I
NFORMATIONS
Compte rendu de congrès
Écho-doppler cardiaque
Théorie et pratique
Grenoble, 4-6 juin 1998
●
Dr G. Vanzetto*
* Clinique cardiologique et Urgences cardiologiques, CHU de Grenoble,
BP 217, 38043 Grenoble Cedex 09.
L
Figure 1. Image caractéristique de voile intimal observé en ETO en cas
de dissection aortique.

La Lettre du Cardiologue - n° 299 - septembre 1998
8
aiguës de l’aorte, surtout pour les dissections aiguës et les rup-
tures traumatiques : elle permet de poser d’emblée l’indication
chirurgicale si le diagnostic est formel. En cas de suspicion d’hé-
matome pariétal ou d’examen incomplet, il est indispensable de
compléter l’investigation par un autre examen, habituellement un
scanner spiralé.
Le Dr E. Borrel (CHU de Grenoble) a ensuite développé les moda-
lités de surveillance des dissections aortiques opérées. Une
insuffisance aortique, un anévrysme de l’aorte résiduelle, un faux
anévrysme périprothétique par désinsertion des anastomoses
proximales, distales, ou coronaires, et enfin une dissection rési-
duelle de l’aorte et de ses branches doivent être tout particulière-
ment recherchés. Les facteurs favorisant l’apparition de
complications tardives sont la présence d’une dystrophie artérielle
(Marfan) ou d’une hypertension artérielle, et sont influencés par
la technique chirurgicale utilisée. Cela explique la nécessité d’être
en possession du compte rendu opératoire précis lors de la réali-
sation des examens de surveillance pour ne pas poser de conclu-
sions erronées sur des images souvent trompeuses. Ces compli-
cations sont souvent longtemps asymptomatiques avant de se
manifester par un événement brutal, parfois létal. Une surveillance
systématique tous les six mois, puis tous les ans pendant cinq ans,
est nécessaire. Le scanner spiralé semble être l’examen de réfé-
rence par sa reproductibilité, son caractère peu invasif et le fait
qu’il explore toute l’aorte. L’ETO permet un examen plus précis
de la valve aortique, du segment O et du segment III. Elle peut
compléter le scanner en cas d’anomalie. L’IRM, si elle est pos-
sible, est réservée aux patients chez qui le scanner est contre-indi-
qué (insuffisance rénale) ou dangereux (allergie à l’iode).
Embolie pulmonaire
Le Dr O. Dubourg (Hôpital Ambroise-Paré, Boulogne) a précisé
que l’embolie pulmonaire est une affection fréquente, de dia-
gnostic souvent méconnu, cause de 5 % des décès observés dans
la récente étude de Göteborg.
L’ETT facilite le diagnostic de cœur pulmonaire aigu en mon-
trant une hypertension artérielle pulmonaire et son retentissement
en amont, c’est-à-dire une dilatation des cavités droites. La dila-
tation du ventricule droit (VD) est directement corrélée à l’im-
portance de l’obstruction artérielle, et un rapport de surfaces
VD/VG - recueillies en vue apicale 4 cavités – de 0,60 corres-
pond à un indice de Miller ≥40 %. La fonction systolique ven-
triculaire droite est nettement diminuée en cas d’embolie pul-
monaire massive, et il existe alors une interdépendance
ventriculaire. La sensibilité et la spécificité de l’ETT pour le dia-
gnostic de ces embolies pulmonaires graves sont respectivement
de 76 et 80 %. L’ETT permet par ailleurs de visualiser les caillots
mobiles dans les cavités droites. Le pronostic de ces caillots est
sévère, avec une mortalité de 5 % chez les patients opérés, contre
35 % en cas de traitement par héparine, et de 46 % dans le groupe
thrombolysé.
L’ETO est la méthode de choix pour visualiser ces thrombus, en
particulier lorsqu’ils sont situés dans le tronc de l’artère pulmo-
naire ou dans une de ses branches. La sensibilité et la spécificité
de l’ETO – en considérant le scanner spiralé comme méthode de
référence – sont de 84 % pour les embolies proximales. En
revanche,la sensibilité baisse à 58 %, si l’on considère l’ensemble
des embolies pulmonaires lobaires et segmentaires. L’examen
ultrasonore ne doit pas se limiter à l’étude cardiaque, et l’écho-
graphie veineuse doit compléter cet examen, puisque sa sensibi-
lité et sa spécificité sont supérieures à 90 %.
En pratique, l’échographie doit être l’examen initial à réaliser
en cas de suspicion d’embolie massive. Chez les patients en état
de choc et intransportables, la découverte d’un VD dilaté au cours
d’une ETT et/ou d’une ETO fait évoquer mais ne confirme pas
le diagnostic d’embolie pulmonaire. Toutefois, on peut éliminer
ainsi une autre affection (tamponade, infarctus inférieur avec
extension VD, syndrome de détresse respiratoire, etc.). La pré-
sence d’un thrombus mobile dans l’artère pulmonaire droite (ou
le tronc de l’artère pulmonaire) affirme une embolie pulmonaire.
En son absence, certains s’attachent à rechercher un thrombus
dans l’artère pulmonaire gauche, et surtout au niveau des membres
inférieurs des veines iliaques et de la veine cave. Enfin, la décou-
verte échocardiographique d’un caillot mobile au niveau de
l’oreillette droite devrait faire envisager une thrombectomie chi-
rurgicale.
ÉTUDE DE LA FONCTION AURICULAIRE GAUCHE PAR QUAN-
TIFICATION ACOUSTIQUE
La détermination automatique des contours endocardiques par
quantification acoustique permet d’obtenir des courbes des varia-
tions de surface et de volume des cavités cardiaques. L’étude pré-
sentée par le Pr B. Denis (CHU de Grenoble) a eu pour but de
préciser la morphologie de ces courbes au niveau de l’oreillette
gauche (OG), de déterminer les valeurs normales des volumes et
des temps de remplissage et de vidange auriculaire, et enfin d’éva-
luer la part de la contraction auriculaire gauche dans ces varia-
tions de volume, chez des sujets normaux et chez des patients
présentant un anomalie de la fonction diastolique VG.
Fonction auriculaire gauche normale
La courbe de variation de volume auriculaire gauche (figures 2
et 3) comporte plusieurs parties :
1. Une partie ascendante “S” correspond à la systole ventricu-
laire, pendant laquelle le volume auriculaire gauche augmente.
Cette augmentation de volume auriculaire permet le stockage du
sang arrivant par les veines pulmonaires et représente la fonction
réservoir de l’oreillette gauche.
2. Une partie descendante puis horizontale “D” correspond au
remplissage rapide initial ventriculaire gauche, passif (contem-
porain de l’onde E mitrale et de la première partie de l’onde D
pulmonaire) et au remplissage lent. C’est la fonction conduitde
l’oreillette gauche.
3. Une deuxième partie descendante “A” correspond à la systole
auriculaire. Cette partie descendante présystolique correspond à
l’onde A du doppler veineux pulmonaire : c’est la fonction pompe
de l’oreillette gauche.
Fonction auriculaire et fonction diastolique ventriculaire
gauche
Selon les différents types de doppler mitral et doppler veineux
pulmonaire, la courbe de variation de volume auriculaire se modi-
fie (figure 4).
I
NFORMATIONS

I
NFORMATIONS
La Lettre du Cardiologue - n° 299 - septembre 1998
9
cm3
Volumes
maximaux
50,9 ± 15,4
Volumes
pré-A
28,9 ± 13,4
Volumes
minimaux
18,56 ± 13,4
Fonction
pompe Fonction
réservoir Fonction
conduit
Remplissage
Vidange
rapide
initiale
Contraction
auriculaire
Relaxation
auriculaire
Contraction
ventriculaire
gauche
S
A
D
369 ± 57 ms 188 ± 53 ms 117 ± 32,2 ms Temps
ms
70
60
50
40
30
20
Doppler mitral
Doppler des
veines pulmonaires
EA
SDSD
A
EEA
D
S
AP
AP AP Pseudo-normalNormal Stade I 55
Figure 2. Image et courbe de variation de volume auriculaire gauche obtenues par quantification acoustique en incidence 4 cavités apicale.
Figure 3.
Courbes de variation
des volumes auriculaires
gauches chez les sujets
avec fonction diastolique VG
normale.
Figure 4.
Évolution des courbes de volume
auriculaire gauche
chez les patients normaux
et avec anomalies
de la fonction diastolique
(voir texte pour commentaires).

I
NFORMATIONS
1. Chez le sujet nor-
mal, l’augmentation
de volume auricu-
laire pendant la sys-
tole et la diminu-
tion de volume en
protodiastole
(fonction réser-
voir et fonction
conduit) sont pré-
dominantes par rapport à la
variation de volume due à la contraction auri-
culaire. Cette dernière est de 32 %, tout à fait en accord avec la
contribution de la systole auriculaire gauche au flux mitral anté-
rograde (25 %). Le flux veineux pulmonaire rétrograde (A
reverse) est alors très faible.
2. Chez les patients avec un doppler mitral de type I, on observe
une augmentation de volume de l’OG et une contribution impor-
tante de la contraction auriculaire gauche aux variations de
volume (> 50 %). La systole auriculaire génère un flux essen-
tiellement antérograde car la compliance ventriculaire gauche est
encore bonne et le flux veineux pulmonaire rétrograde (A reverse)
est faible. À ce stade, l’OG subit une surcharge en volume, alors
que la surcharge en pression est modérée.
3. Chez les patients avec un doppler mitral pseudo-normal, on
observe une augmentation importante du volume de l’OG. La
contribution de la contraction auriculaire est ≥50 %, bien que
l’onde A mitrale ait diminué au profit du remplissage protomé-
sodiastolique. Cela s’explique par l’apparition d’un flux veineux
pulmonaire rétrograde important lors de la systole auriculaire, la
“compliance” pulmonaire étant meilleure que la compliance VG.
L’élément important est que ces patients présentent une baisse
notable de la “fraction d’éjection auriculaire” mesurée par quan-
tification acoustique (18 % pour une normale ≥40 %). À ce stade,
l’OG subit non seulement une surcharge en volume mais aussi
une surcharge en pression, d’où le risque de fibrillation auricu-
laire.
En conclusion, la détermination automatique des contours de
l’endocarde auriculaire gauche par quantification acoustique est
une technique qui permet une approche, jusque-là impossible, de
la fonction auriculaire gauche. La courbe de variation de volume
auriculaire a un intérêt non seulement théorique (pour compléter
la compréhension des troubles de la fonction diastolique VG)
mais aussi pratique (pour diagnostiquer un trouble de la relaxa-
tion et de la compliance ventriculaire gauche, particulièrement
net au stade de doppler mitral pseudo-normal).
Échographie-doppler de stress
L’intérêt de l’échographie de stress (d’effort ou sous dobutamine)
pour l’évaluation des cardiopathies ischémiques est bien démon-
tré. De nouvelles méthodes ou indications de cette technique,
moins connues, ont été développées.
1. Le Dr Brion (Hôpital Desgenettes, Lyon) a fait part de son
expérience du doppler d’effort :
a. L’analyse des flux aortiques à l’effort permet d’évaluer la
réserve myocardique chez l’insuffisant cardiaque. Ainsi, l’inté-
grale temps-vitesse (ITV) aortique à l’effort est corrélée au
volume d’éjection systolique évalué par ventriculographie isoto-
pique et au pic de VO2d’effort. Cette analyse de l’ITV aortique
permet de distinguer trois types de patients : les sujets avec aug-
mentation de l’ITV (sujets les plus performants), ceux chez qui
l’ITV est stable (l’adaptation se faisant uniquement sur la fré-
quence cardiaque), et ceux présentant une diminution de l’ITV
à l’effort. Ce dernier cas est de mauvais pronostic puisque, dans
cette série, tous ces patients sont décédés dans les deux ans.
L’étude de l’ITV aortique à l’effort permet également d’appré-
cier le retentissement d’une ischémie myocardique d’effort. De
nombreuses autres applications de cette technique ont été pro-
posées, comme l’évaluation du profil hémodynamique des pro-
thèses valvulaires aortiques à l’effort, l’étude du gradient intra-
ventriculaire à l’effort des myocardiopathies hypertrophiques,
l’appréciation du retentissement hémodynamique à l’effort des
valvulopathies ou la comparaison de l’efficacité hémodynamique
de modes de stimulation cardiaque pendant l’effort.
b. L’étude du flux transmitral pendant l’effort peut permettre d’ob-
jectiver une anomalie de remplissage ventriculaire gauche à l’ef-
fort (cardiopathie hypertrophique) et d’apprécier les effets des
traitements influençant la qualité du remplissage ventriculaire
gauche. Elle évalue également la réserve de surface mitrale, dif-
férents auteurs ayant mis en évidence chez certains patients por-
teurs d’un rétrécissement mitral une augmentation de la surface
mitrale à l’effort. Enfin, elle peut évaluer le retentissement hémo-
dynamique d’une prothèse valvulaire en position mitrale.
c. L’enregistrement de la régurgitation tricuspidienne permet
enfin d’évaluer la pression de l’artère pulmonaire pendant l’ef-
fort. L’IT est toutefois extrêmement difficile à enregistrer pen-
dant un effort. Plusieurs auteurs ont montré que l’utilisation de
l’échographie de contraste améliorait considérablement la possi-
bilité d’enregistrer un tel reflux. Il a ainsi été démontré que la
réduction de la réserve fonctionnelle de la circulation pulmonaire
à l’effort précédait l’installation d’une hypertension artérielle pul-
monaire permanente quelle qu’en soit la cause, en mettant en évi-
dence, chez certains patients avec pression pulmonaire de repos
normale, une nette augmentation de la PAPS en cours d’effort.
2. Le Dr B. Cormier (Institut hospitalier Jacques-Cartier, Massy)
a pour sa part rappelé l’intérêt de cette technique d’examen dans
les valvulopathies : évaluation de la sévérité des lésions valvu-
laires dans les cas difficiles où l’on n’est pas certain du caractère
significatif de la valvulopathie, de son retentissement hémody-
namique et sur la fonction ventriculaire gauche, enfin détection
d’une éventuelle atteinte coronaire associée.
Ainsi, l’échographie de stress permet, dans les cas difficiles de
rétrécissement aortique (RA) avec faible gradient associé à une
dysfonction myocardique, de déterminer si la dysfonction myo-
cardique est totalement ou partiellement secondaire à la sténose
aortique ou à une myocardiopathie autonome. En pratique, la réa-
lisation d’un stress pharmacologique chez les patients ayant une
surface aortique de 0,6 à 0,8 cm2et un faible gradient permet de
distinguer trois cas de figure :
La Lettre du Cardiologue - n° 299 - septembre 1998
10

La Lettre du Cardiologue - n° 299 - septembre 1998
11
a. une augmentation significative de la surface aortique par équa-
tion de continuité, sans augmentation proportionnelle du gradient
sous dobutamine, plaidant pour une dysfonction myocardique
autonome ;
b. une augmentation significative du gradient sans augmentation
de la surface, en faveur d’une sténose significative ;
c.une absence de réserve contractile sous dobutamine empêchant
donc de conclure quant à la sévérité de la sténose aortique. Ce
groupe semble affecté d’un mauvais pronostic, quelles que soient
les solutions thérapeutiques proposées.
Dans le cadre de la sténose mitrale, l’échographie dynamique a
permis d’améliorer la compréhension du mécanisme par lequel
le volume d’éjection systolique augmente à l’effort, malgré la
diminution du temps de remplissage diastolique. Il s’agit là encore
d’une réserve fonctionnelle de la valve mitrale, dont l’amplitude
est inversement proportionnelle à l’importance des lésions ana-
tomiques.
LES NOUVELLES TECHNIQUES ÉCHO-DOPPLER
Les progrès technologiques
Le Dr C. Scheublé a fait la synthèse des améliorations techniques
et des nouvelles voies de recherche. Ainsi, l’imagerie connaît
déjà, ou connaîtra prochainement, de gros progrès, essentielle-
ment grâce :
1.à l’amélioration de la chaîne de traitement du signal ultra-
sonore (qualité du rapport signal/bruit de fond, conservation de
la dynamique du signal originel) ;
2. au développement de sondes “à large bande passante” (émet-
tant et recevant les ultrasons dans une gamme plus large de fré-
quence) ;
3. aux possibilités de focalisation du faisceau ultrasonore (amé-
liorant considérablement la résolution de l’échographe) ;
4. aux méthodes de recherche automatisée des contours endo-
cardiques (Color Enhanced motion Analysis, de principe com-
parable à celui de l’angiographie numérisée soustractive, et quan-
tification acoustique “color kinesis”, reposant sur l’analyse des
données brutes du signal de radiofréquence) ;
5. au doppler tissulaire (tissue doppler imaging), permettant de
différencier les “échos tissulaires” des “échos hématiques”, d’étu-
dier très précisément la vitesse et les modalités de déplacement de
la région anatomique explorée, et donc autorisant une analyse très
fine de la cinétique pariétale ventriculaire gauche (figure 5) ;
6. enfin à l’imagerie d’harmonique.Son principe est le suivant :
les ondes de pression transmises mettent en vibration les micro-
structures présentes dans le faisceau. Leurs fréquences de réso-
nance sont différentes selon les tissus et possèdent une valeur
optimale qui amplifie le signal de retour. Cette fréquence opti-
male de résonance correspond à la seconde harmonique de la fré-
quence transmise. En choisissant la fréquence de retour au niveau
du capteur, il est possible de réaliser une imagerie optimale adap-
tée à une structure tissulaire spécifique.
Échographie de contraste myocardique (ECM)
Le principe de l’ECM repose sur l’injection de microbulles de
gaz (de 4 à 20 µm de diamètre) créant des interfaces échocardio-
graphiques permettant la visualisation de la microcirculation coro-
naire. Les produits de contraste myocardique de première géné-
ration étaient constitués de bulles de ± 10 µm, et nécessitaient
une injection intracoronaire. Les produits de deuxième généra-
tion, dont les bulles présentent un diamètre de 5 à 7 µm, fran-
chissent la barrière capillaire pulmonaire et peuvent être injectés
par voie veineuse. Une première famille est composée par les
agents de contraste réalisés en absorbant des microbulles d’air
sur différents composés (Albunex®, Échovist®, Levovist®), mais
les concentrations par voie veineuse doivent être élevées pour
permettre une visualisation du myocarde. Leur performance est
toutefois bonne en ce qui concerne le contraste des cavités car-
diaques. La seconde famille consiste en des suspensions colloï-
dales ou des émulsions de gaz non diffusibles de haut poids
moléculaire (décafluoro-pentane : Échogen®), permettant une
meilleure visualisation du temps gauche. Enfin, la troisième
famille, encore expérimentale, associe des lipides et des perfluo-
rocarbones. Le problème majeur est la destruction des bulles par
l’énergie mécanique véhiculée par les ultrasons. Une des solu-
tions apportées est l’acquisition échographique intermittente, qui
permet de prolonger la durée de vie des bulles. Un deuxième pro-
I
NFORMATIONS
Figure 5. Images DTI en mode TM (en haut) et bidimensionnelle (en bas)
permettant l’analyse de la fonction ventriculaire gauche segmentaire.
 6
6
1
/
6
100%