thématique d Infections transmises

dossier
tmiqu
Le Courrier de la Transplantation - Volume VIII - n
o 2 - avril-mai-juin 2008
64
Infections
transmises
par le greon
Coordinateur :
Y. Calmus
Infections transmises par le greffon :
virus herpès humain de type 8 (HHV-8)
Transmission of human herpesvirus 8 by the graft
during solid organ transplantation
C. Francès* ●
* Hôpital Tenon, Paris.
L
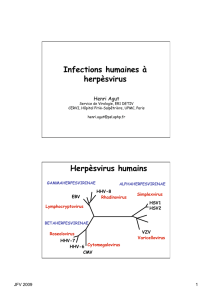
e virus HHV-8 a été découvert en
1994 par Y. Chang (figure 1) [1].
Comme tous les virus herpès, il
présente une phase de latence qui peut
évoluer, après réactivation spontanée ou
induction, vers une phase lytique.
L’expression des protéines, utilisées pour
les tests sérologiques, varie selon l’état
du virus (phase latente, phase lytique
initiale ou phase lytique) [tableau I].
Différentes maladies sont associées à
l’HHV-8 : maladie de Kaposi, maladie
de Castleman multicentrique, lymphome
primitif des séreuses, autres proliféra-
tions lymphoplasmocytaires. Ce virus
peut être responsable d’un syndrome
avec forte virémie associant aplasie,
cytopénie, hémophagocytose, rash, hépa-
tite, épanchement pleural et èvre.
Le risque élevé de transmission de
l’HHV-8 est expliqué par la diversité
de ses cellules cibles : lymphocytes B,
cellules endothéliales ou progénitrices,
monocytes, cellules épithéliales, prin-
cipalement de l’oropharynx, cellules
épithéliales tubulaires.
La détection d’une infection par HHV-8
repose sur différentes méthodes :
détection de séquences du génome
par PCR ;
visualisation d’antigènes d’HHV-8
sur des coupes tissulaires par immuno-
fluorescence/immunohistochimie
(figure 2) ;
détection d’anticorps anti-HHV-8
dans le sérum.
Cependant, aucune de ces techniques
ne permet de préciser la date de conta-
mination. L’absence de standardisation
des méthodes d’immunouorescence
ou des méthodes ELISA (Enzyme-
linked immunosorbent assay) utili-
sées pour les tests sérologiques pose
problème. Toutefois, l’immunouores-
cence sur cellules infectées avec anti-
gène latent a une bonne spécicité, et
celle avec antigène lytique une bonne
sensibilité.
Les tests ELISA sont plus faciles à
utiliser, mais, le plus souvent, ce sont
des tests “maison” qui ne peuvent pas
être comparés d’une étude à l’autre.
Ils utilisent des peptides recombinants
(orf73, orf65, orfK8.1, orfK12, etc.) ou
des extraits cellulaires totaux.
✓
✓
✓
HHV-8 peut être transmis par le greffon. Une étude prospective de cohorte a
été mise en place pour préciser la morbidité de l’infection HHV-8 transmise en
transplantation rénale. Trois événements cliniques (4,7 %) sont apparus chez les
64 transplantés D+/R- (une primo-infection clinique et 2 maladies de Kaposi). À
36 mois, 24,8 % des receveurs sont devenus séropositifs. L’étude a été étendue
à tous les receveurs d’organes D+/R-. Un essai ouvert a étudié la prévention de
l’infection HHV-8 par le rituximab en cas de virémie répétée chez les sujets D+/R-.
Alors que la prévalence d’HHV-8 était élevée chez les donneurs (4 à 11 %), un seul
événement clinique a été observé, après transplantation hépatique.
Actuellement, il est difcile de réaliser une sérologie en urgence chez les donneurs,
car il n’existe pas de technique ELISA able et reproductible. Même si une telle
technique existait, on pourrait discuter de l’intérêt d’éliminer les donneurs positifs
en raison du faible nombre d’événements cliniques apparaissant chez les receveurs
à risque (D+/R-).
RÉsUmÉ
CT N°2 2008.indd 64 30/06/08 18:34:52

Figure 1. Virus HHV-8.
Figure 2. Marquage de la protéine LANA.
Figure 3. Séroprévalence du HHV-8/KSH dans la population générale.
Forte, 40-80 %
Moyenne, 10-30 %
Faible, < 5 %
Foyers de forte séroprévalence (10-60 %) du HHV-8
et KSHV dans la population homosexuelle masculine
dossier
tmiqu
Le Courrier de la Transplantation - Volume VIII - n
o 2 - avril-mai-juin 2008
65
La prévalence de l’infection HHV-8
est indiquée sur la figure 3. On note un
gradient nord-sud, avec une prévalence
parfois très élevée dans certains pays
africains.
Outre la transmission sexuelle (homo- et
hétérosexuelle), une transmission par
contacts proches peut parfois se produire
très tôt dans la vie (baisers de la mère à
son enfant, par exemple) [2]. La trans-
mission par voie sanguine est rare, mais
possible.
En 2000, M. Luppi et son équipe ont
démontré la possibilité d’une trans-
mission de l’HHV-8 par le greffon
(3, 4), grâce à l’identication génique
de la partie variable du virus chez les
deux receveurs de greffons rénaux et le
donneur des reins. Plusieurs études rétro-
spectives de transmission de l’HHV-8
par le greffon ont fait état des résultats
variables.
Du fait de l’absence de données ables
sur la morbidité de l’infection HHV-8
post-greffe, une étude nationale a été
mise en place.
Dans cette étude prospective de cohorte,
tous les receveurs et donneurs de reins
ont été inclus de 2001 à 2004, et suivis
pendant 3 ans. La sérologie HHV-8
(immunofluorescence LANA) a été
effectuée chez tous les donneurs et
Tableau I. HHV-8.
Phase
latente
Phase initiale
lytique
Phase
lytique
LANA Rta (orf50) Protéines
structurales (K8)
vFLIP Z (orfK8) ADN polymérase,
protéase, etc.
v-cycline vIRF
LAMP VGPCR
vIL6
vMIP
K1, K5
MTA (orf57)
Vbcl2
CT N°2 2008.indd 65 30/06/08 18:34:54

Figure 4. Évolution de la virémie.
1 300
18 millions
11 millions
1 million
< 50---------< 50
< 50---------< 50
Copies/106 cellules mononuclées
20/03/2001 18/06/2001 17/09/2001 13/12/2001 2/01/2002 9/01/2002 16/01/2002 17/01/2002 24/01/2002 18/09/2003
6
3 907
1 631
¦Ac anti-CD20 (525 mg/j)
dossier
tmiqu
Le Courrier de la Transplantation - Volume VIII - n
o 2 - avril-mai-juin 2008
66
receveurs de reins. Trois cohortes ont
été constituées, la première regroupant
des donneurs positifs ou négatifs et des
receveurs positifs (cohorte A), la seconde
des donneurs positifs et des receveurs
négatifs (cohorte B), et la troisième
des donneurs et des receveurs négatifs
(cohorte C). Une recherche de virémie
cellulaire HHV-8 a été effectuée tous
les 3 mois pour les cohortes A et B (à
l’hôpital Saint-Louis) ; trois tests sérolo-
giques ont été réalisés pour la cohorte B
(immunouorescence latente et immu-
nouorescence lytique, ELISA orfK8.1).
Les résultats de la séroprévalence HHV-8
par la technique d’immunouorescence
latente ont été classés en fonction des
régions (tableau II).
Le tableau III montre la répartition des
résultats sérologiques des donneurs selon
les deux techniques.
Des événements cliniques sont apparus
chez 4,7 % des 64 transplantés de la
cohorte B : un cas de primo-infection
clinique (1,6 %), avec fièvre élevée,
bicytopénie, syndrome d’activation
macrophagique, détection d’une virémie
dès 6 mois après la greffe, et guérison
sous rituximab ; deux cas de maladie de
Kaposi cutanéo-viscérale (3,1 %), avec
absence de primo-infection clinique,
les virémies étant toujours négatives
dans l’un des cas, et une virémie faible,
13 mois après l’apparition du Kaposi
(figure 4), ayant été constatée dans
l’autre cas.
Aujourd’hui, la maladie de Kaposi est
bien prise en charge, ce qui explique
que, dans cette étude avec suivi de 3 ans,
aucune différence en termes de survie
n’ait été observée entre les cohortes
(figure 5). Il en est de même pour
l’estimation des incidences cumulées
de perte du greffon et de décès sans perte
de greffe (figure 6).
Dans la cohorte B, un transplanté était
considéré séropositif lorsque au moins
deux des trois types de tests utilisés
(immunouorescence latente, lytique
et ELISA) étaient positifs. À 36 mois, le
taux d’incidence cumulée de sérologie
positive ainsi dénie était de 24,8 %.
Un certain nombre de patients ont eu
une séroconversion sans événement
clinique.
Pour évaluer la morbidité de la transmis-
sion du virus HHV-8, une étude rétro-
spective de la cohorte B a été étendue
à tous les receveurs d’organes. Il en
ressort une morbidité très élevée entre
4 et 12 mois après la greffe.
Un essai de phase II non contrôlé multi-
centrique ouvert a étudié la prévention
de la primo-infection clinique HHV-8
et du sarcome de Kaposi transmise
par le greffon par traitement avec le
rituximab de la primo-infection HHV-8.
Les sujets à risque D+/R- ont été inclus
pendant 2 ans, et suivis pendant 2 ans.
Les sérologies HHV-8 de tous les
Tableau II. Séroprévalence HHV-8 par la technique d’immunouorescence latente.
Inter-régions
françaises
Nombre
de donneurs
Donneurs
positifs (%)
Nombre
de receveurs
Receveurs
positifs (%)
IR1 (Nord) 423 0 557 2,7
IR2 (Est) 492 1 531 2,3
IR3 (Centre) 556 1,3 766 2,5
IR4 (Sud) 177 0,6 165 6,1
IR5 (Sud-Ouest) 464 0,9 550 1,8
IR6 (Ouest) 929 1 1 211 1,2
IR7 (Île-de-France) 652 2,1 1 189 6,7
Total 3 693 1,08 4 969 3,24
Cohorte A : 161 transplantés ; cohorte B : 64 transplantés ; cohorte C : 4 744 transplantés.
Tableau III. Répartition des résultats
sérologiques.
Immunouorescence latente
ELISA
orfK8.1
Positif Négatif Total
Positif 13 32 47
Négatif 20 1 818 1 838
Total 33 1 852 1 885
CT N°2 2008.indd 66 30/06/08 18:34:55

0
1,00
0,95
0,90
0,85
0,80
Survie
5
Cohorte A
Cohorte B
Cohorte C
10 15 20 25 30 35
Figure 5. Estimation du taux de survie.
0
0,20
0,15
0,10
0,05
0,00
Incidence cumulée (%)
5
Perte greon cohorte A
Perte greon cohorte B
Perte greon cohorte C
Décès avec greon fonctionnel cohorte A
Décès avec greon fonctionnel cohorte B
Décès avec greon fonctionnel cohorte C
10 15 20
Mois
25 30 35
Figure 6. Estimation des incidences cumulées de perte du greffon et de décès sans perte
de greffe.
dossier
tmiqu
Le Courrier de la Transplantation - Volume VIII - n
o 2 - avril-mai-juin 2008
67
donneurs d’organes ont été déterminées
par deux tests : immunofluorescence
latente et immunouorescence lytique.
Les virémies HHV-8 ont été recherchées
tous les 15 jours, et, si la virémie était
positive à deux reprises, un traitement
de 4 cures de rituximab était entrepris.
Fait surprenant, alors que la prévalence
d’HHV-8 était élevée chez les donneurs
(immunouorescence latente 4,27 %,
immunofluorescence lytique 8,62 %,
immunouorescence latente ou lytique
10,79 %), un seul événement clinique
a été observé, après transplantation
hépatique.
faut-il dépister
et éliminer les donneurs HHv-8 +
de la transplantation ?
Actuellement, il est difcile de réaliser
ces tests en urgence, car il n’existe pas
de technique de sérologie HHV-8 ELISA
commercialisée, able et reproductible.
Même s’il existait une technique facile
et able, on pourrait discuter de l’in-
térêt d’éliminer les donneurs positifs
du fait du faible nombre d’événements
cliniques (4,7 %), sans décès ni perte du
greffon. ■
RéféRences
bibliogRaphiques
1. Chang Y et al. Science 1994;266(5192):1865-9.
2. Hladik W et al. N Engl J Med 2006;355(13):
1331-8.
3. Luppi M et al. N Engl J Med 2000;343(19):
1378-85.
4. Luppi M et al. Blood 2000;96(9):3279-81.
CT N°2 2008.indd 67 30/06/08 18:34:55
1
/
4
100%