Chimioprévention des lésions prémalignes des VADS M

7
La Lettre du Cancérologue - volume XI - n° 1 - janvier-février 2002
es cancers des voies aériennes restent un problème
majeur de santé publique de par leur fréquence
et la morbi-mortalité qu’ils entraînent. Malgré
d’immenses efforts, la mortalité globale liée à ces cancers
épithéliaux n’a pas diminué depuis 25 ans (1). Il est admis
que le tabac est le principal facteur de risque pour l’apparition
d’un cancer des VADS. Par conséquent, la lutte contre le taba-
gisme reste une priorité de santé publique. Toutefois, force est
de constater l’augmentation de la consommation tabagique
à l’échelle mondiale et le problème spécifique que soulèvent
les anciens fumeurs. En effet, le risque relatif de cancer des voies
aériennes décline chez les anciens fumeurs en fonction du temps
passé depuis l’arrêt du tabagisme, mais ce risque reste supérieur
à celui des non-fumeurs (2).
Dans un tel contexte, la prévention et la détection précoce
des lésions précancéreuses et cancéreuses des voies aériennes
présentent un intérêt tout particulier (3). La chimioprévention,
qui correspond à l’utilisation d’agents naturels ou synthéthiques
dans le but de prévenir, de supprimer ou d’inverser la progression
carcinogénique vers le cancer invasif, est un domaine en pleine
expansion, et constitue un des axes de travail pour essayer
de diminuer la morbi-mortalité des cancers des VADS. Les
principales données concernant les essais de chimioprévention
dévéloppés dans le domaine des VADS sont présentées dans
ce document. Les orientations les plus récentes dans le domaine
de la chimioprévention sont également discutées. Il s’agit
de l’individualisation des facteurs de risque afin de réduire
le champ de la chimioprévention primaire aux seuls sujets
à haut risque, de la mise en place de critères intermédiaires
de réponse, nécessaires compte tenu de la lourdeur des essais
cliniques et utiles car permettant de valider l’atteinte de la cible
visée, et, enfin, du développement de nouvelles cibles
de chimioprévention basées sur l’étude des interactions
cellules cancéreuses-cellules de l’hôte.
DÉFINITION DE LA CHIMIOPRÉVENTION
La chimioprévention correspond à l’utilisation d’agents naturels
ou synthéthiques dans le but de prévenir, de supprimer
ou d’inverser la progression carcinogénique vers le stade invasif
du cancer (4). Il s’agit d’un domaine en pleine expansion
qui associe la recherche fondamentale, la recherche appliquée
et la recherche clinique afin de développer des agents chimiques
capables d’arrêter ou de prévenir le processus oncogénique.
Les concepts de base en chimioprévention sont la carcinogenèse
de champ, la carcinogenèse multi-étapes, la réversibilité
de certaines lésions précancéreuses, et l’importance des relations
entre les cellules cancéreuses et leur environnement (notion
de gènes “ modificateurs ” du processus carcinogénique).
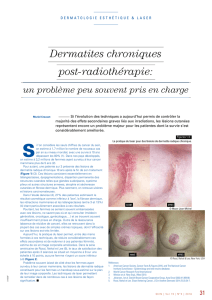
Le concept de carcinogenèse de champ (figure 1) traduit le fait
que l’exposition à un agent carcinogène, au niveau de toute
une région ou de tout un épithélium, comme celui des voies
aériennes, conduit à l’apparition de multiples lésions
sur l’ensemble de cette région ou de cet épithélium. Ainsi,
la présence de lésions prémalignes ou malignes dans une partie
du champ constitue un indicateur de risque élevé de lésions
cancéreuses dans d’autres parties du même champ (figure 2).
Le traitement ou le contrôle des lésions précancéreuses constitue
MISE AU POINT
Chimioprévention des lésions
prémalignes des VADS
J.C. Soria*
L
* Département de médecine, Institut Gustave-Roussy
94805 Villejuif, France.
Figure 1. L
e concept de carcinogènese de champ
.
Figure 2.
Lésions précancéreuses de la cavité buccale.
Lésions
clonales
Épithelium
des VADS

donc un moyen potentiel pour éviter le développement de lésions
invasives. De fait, si le traitement standard des lésions précan-
céreuses des VADS correspond à la chirurgie, il est clair toute-
fois que cette approche reste insatisfaisante (récidives, apparition
de nouvelles lésions), d’où le développement des traitements
médicaux qui cherchent à traiter l’ensemble de l’épithélium,
et à prévenir les rechutes.
CHIMIOPRÉVENTION DES VADS
Le rôle des rétinoïdes comme agents pharmacologiques chimio-
préventifs a été évalué aussi bien en termes de chimioprévention
secondaire (patients avec des lésions précancereuses) que
de chimioprévention tertiaire (patients avec une histoire
de cancer ORL). De nombreux essais cliniques développés
dans ce domaine sont positifs et ont permis de valider
l’approche de chimioprévention. Ils sont résumés dans
le tableau I (5-13). Le premier essai positif, publié par Hong
et al. en 1986 (5) mettait en évidence une efficacité de l’acide
13 cis rétinoïque dans les leucoplasies orales (67 % de régression
majeures contre 10 % dans le groupe placebo). Toutefois,
cet essai pivot présentait deux problèmes : le taux très élevé
de rechutes à distance du traitement et l’importance des effets
secondaires liés aux rétinoïdes. L’essai conduit par Lippman et al.
en 1993 (6) a permis de démontrer l’efficacité de faibles doses
d’isotrétinoïne dans les leucoplasies orales avec une nette
diminution des effets secondaires. Cependant, après l’arrêt
du traitement, et avec un suivi médian de 66 mois, il a été mis
en évidence une perte du bénéfice initial lié au traitement avec
survenue de cancers ORL dans les deux groupes de l’étude.
Cela souligne l’importance d’une intervention prolongée
(plusieurs années) pour pouvoir réellement supprimer
les lésions précancéreuses. D’autres essais ont confirmé l’intérêt
des rétinoïdes dans le traitement des lésions précancéreuses.
Parmi eux, l’essai italien utilisant le fenrétinide (4HPR) après
traitement laser des leucoplasies orales a montré une diminution
nette du risque de récidive (6 % de récurrences contre 30 %
dans le groupe placebo) (7). L’essai publié par Papadimitrako-
poulou et al. en 1999 (8) a démontré l’efficacité des rétinoïdes
en association avec l’interféron
α
et l’
α
-tocophérol, dans
les dysplasies modérées et sévères du larynx (50 % de rémissions
complètes à 12 mois). Cependant, ce traitement s’est avéré
insuffisant dans les dysplasies avancées de la cavité orale (9 %
de rémissions complètes à 6 mois), soulignant la nécessité d’une
autre approche pour ce type de lésions orales à très haut risque.
Les patients traités pour un cancer ORL ont un risque très élevé
de développer un second cancer (4-6 % par an). Ils constituent
donc une population intéressante pour la mise en place de pro-
tocoles de chimioprévention. Dans notre expérience, il s’agit
de patients plus motivés par ces essais et plus enclins à en
accepter les contraintes (effets secondaires, suivi à long terme)
que des patients sans aucun antécédent néoplasique. Toutefois,
une sélection appropriée et un suivi rapproché des patients
ORL (confirmation de l’arrêt complet et définitif du tabac,
compliance, etc.) doivent être assurés si ces patients sont
inclus dans des essais de chimioprévention. La première étude
de chimioprévention tertiaire fut celle publiée par Hong
en 1990 (9). Elle concernait 103 patients traités et guéris
d’un cancer ORL et qui avaient reçu de l’isotrétinoïne ou
un placebo sur une durée de 12 mois. L’incidence des seconds
cancers était de 4 % contre 24 % à 32 mois, et de 14 % versus
31 % à 54 mois, pour le bras rétinoïde et le bras placebo
respectivement. La toxicité liée au traitement était considérable
avec, comme conséquence, 33 % des patients dans le bras
isotrétinoïne incapables de maintenir sur 12 mois leur traite-
ment. L’essai coopératif français publié en 1994 (10) ayant
testé l’emploi de l’étrétinate (50 mg/j 1 mois puis 25 mg/j 24
mois) a confirmé la forte incidence des seconds cancers dans
une population de 322 patients préalablement traités pour
un cancer de la cavité orale ou de l’orophraynx (T1-2 N0-1),
mais n’a pas démontré d’efficacité pour le traitement chimio-
préventif (24 % de seconds cancers dans le groupe placebo
contre 38 % dans le groupe étrétinate à 41 mois). La publica-
tion récente des résultats négatifs de l’essai EUROSCAN (11)
ayant porté sur 1 550 patients avec un cancer de la cavité orale
(T1-2 et N0-1), ou du larynx (Tis, T1-3 et N0-1) traités avec
une intention curatrice, et secondairement randomisés placebo
versus rétinyl palmitate et/ou N-acétylcystéine, vient obscurcir
les résultats initialement très prometteurs de l’équipe du M.D.
Anderson Cancer Center quant à l’efficacité de la chimiopré-
vention tertiaire. C’est donc avec impatience que sont attendus
les résultats de l’essai mené conjointement par le Radiation
Therapy Oncology Group (RTOG) avec le Community Clinical
Oncology Program (CCOP-M.D. Anderson), et qui compare
un placebo à 3 ans de faibles doses d’étrétinate chez des patients
traités pour un cancer ORL T1-2, N0.
8
MISE AU POINT
La Lettre du Cancérologue - volume XI - n° 1 - janvier-février 2002
Essai Population étudiée (n) Médicament (dose) Résultat
Chimioprévention secondaire (lésions précancéreuses)
Hong et al. (1986) Leucoplasie orale 44 Isotrétinoïne (2 mg/kg/j) Positif
Stich et al. (1988) Leucoplasie orale 70 Vitamine A Positif
(200 000 UI/semaine)
Han et al. (1990) Lésions orales 61 Rétinamide (40 mg/j) Positif
prémalignes
Lippman et al. (1993) Leucoplasie orale 70 Isotrétinoïne (0,5 mg/kg/j) Positif
Costa et al. (1994) Leucoplasie orale 153 Fenrétinide (200 mg/j) Positif
Papadimitrakopoulou Lésions de dysplasie 36 13 cis acide rétinoïque Positif
et al. (1999) sévère ou modérée (100 mg/m2/j) (larynx)
des VADS α-tocophérol (1 200 UI/j) Négatif
Interféron α(cavité orale)
(3 MU/m2, x 2/semaine)
Chimioprévention tertiaire (antécédent de cancer)
Hong et al. (1990) Antécédent 103 Isotrétinoïne Positif
de cancer ORL (50-100 mg/m2/j)
Bolla et al. (1994) Antécédent de cancer 316 Etrétinate (20-50 mg/j) Négatif
de la cavité orale
ou de l’oropharynx
EUROSCAN (2000) Cancer de la cavité 1550 Rétinyl palmitate seul Négatif
orale (T1-2 et N0-1), (300 000 UI/j 1ère année,
ou du larynx 150 000 UI/J 2eannée)
(Tis, T1-3 et N0-1) N-acétylcystéine seule
traité avec (600 mg/j 2 ans)
une intention curatrice Association des deux
Tableau I.
Essais de chimioprévention des VADS utilisant
notamment les rétinoïdes.

9
La Lettre du Cancérologue - volume XI - n° 1 - janvier-février 2002
CONCLUSION
L’incidence et la mortalité associées aux cancers des VADS
n’ont pas été significativement modifiées depuis plus de 25 ans,
malgré l’introduction de nouvelles drogues cytotoxiques et le
développement d’approches multidisciplinaires associant chirur-
gie, chimiothérapie et radiothérapie. Ce constat indique à quel
point la mise en place d’approches de chimioprévention, pour
prévenir le processus carcinogénique au niveau des voies
aériennes, est nécessaire. La caractérisation complète des déter-
minants moléculaires de la carcinogenèse des VADS est essen-
tielle pour permettre le développement rationnel et ciblé
d’agents chimiopréventifs. Des progrès considérables ont été
réalisés en ce sens ces dernières années. Les résultats prélimi-
naires, démontrant une efficacité des rétinoïdes dans le cadre
des lésions prémalignes de la cavité orale et du larynx, fournis-
sent un rationnel supplémentaire pour continuer à explorer la
stratégie chimiopréventive avec ces agents ou d’autres molé-
cules présentant un meilleur index thérapeutique. La chimio-
prévention va sans doute s’enrichir de l’utilisation d’agents
pharmacologiques capables de combattre la dépendance vis-à-vis
de la nicotine chez des sujets à risque. Il a été démontré que
l’addiction nicotinique pouvait être associée avec des polymor-
phismes génétiques mettant en jeu le récepteur D2 à la dopamine
et l’enzyme CYP2A6 (14). La lutte contre la dépendance nico-
tinique pourrait faire intervenir des antagonistes du récepteur
dopaminergique D2 et des inhibiteurs de l’enzyme CYP2A6.
Par ailleurs, des molécules ciblant des mécanismes alternatifs
de la carcinogenèse des VADS (inhibiteurs des tyrosines
kinases, de la farnesyl-transférase et des cyclo-oxygénases 2)
sont en train d’être évaluées dans le cadre de la chimiopréven-
tion (15-18). Quoi qu’il en soit, le futur de la chimioprévention
réside sans doute dans la mise en place d’essais fondés sur une
meilleure compréhension des mécanismes carcinogéniques. O
RÉFÉRENCES BIBLIOGRAPHIQUES
1. Greenlee RT, Hill-Harmon BB, Murray T, Thun M. Cancer statistics, 2001.
CA Cancer J Clin 2001 ; 51 : 16-36.
2. Lippman SM, Hong WK. Second malignant tumors in head and neck squamous
cell carcinoma : the overshadowing threat for patients with early stage disease.
Int J Radiat Oncol Biol Phys 1989 ; 17 : 691-4.
3. Hong WK, Sporn MB. Recent advances in chemoprevention of cancer.
Science 1997 ; 278 : 1073-7.
4. Sporn MB, Dunlop NM, Newton DL, Smith JM. Prevention of chemical carcinoge-
nesis by vitamin A and its synthetic analogs (retinoids). Fed Proc 1976 ; 35 : 1332-8.
5. Hong WK, Endicott J, Itri L, Doos W, Batsakis JG, Bell R et al. 13-Cis retinoic
acid in the treatment of oral leukoplakia. N Engl J Med 1986 ; 315 : 1501-5.
6. Lippman SM, Batsakis JG, Toth BB, Weber RS, Lee JJ, Martin JW et al.
Comparison of low-dose isotretinoin with b-carotene to prevent oral carcinoge-
nesis. N Engl J Med 1993 ; 328 : 15-20.
7. Costa A, Formelli F, Chiesa F, Decensi A, De Palo G, Veronesi U. Prospects
of chemoprevention of human cancers with the synthetic retinoid fenretinide.
Cancer Res 1994 ; 54 : 2032s-2037s.
8. Papadimitrakopoulou VA, Clayman GL, Shin DM, Myers JN, Gillenwater
AM, Goepfert H et al. Biochemoprevention for dysplastic lesions of the upper
aerodigestive tract. Arch Otolaryngol Head Neck Surg 1999 ; 125 : 1083-9.
9. Hong WK, Lippman SM, Itri LM, Karp DD, Lee JS, Byers RM et al. Prevention
of second primary tumors with isotretinoin in squamouscell carcinoma
of the head and neck. N Engl J Med 1990 ; 323 : 795-801.
10. Bolla M, Lefur R, Ton Van J, Domenge C, Badet JM, Koskas Y et al.
Prevention of second primary tumours with etretinate in squamous cell carcinoma
of the oral cavity and oropharynx. Results of a multicentric double-blind rando-
mized study. Eur J Cancer 1994 ; 30A : 767-72.
11. Van Zandwijk N, Dalesio O, Pastorino U, de Vries N, van Tinteren H.
EUROSCAN, a randomized trial of vitamin A and N-acetylcysteine in patients
with head and neck cancer or lung cancer. J Nat Cancer Inst 2000 ; 92 : 977-
86.
12. Stich HF, Hornby AP, Mathew B, Sankaranarayanan R, Nair MK.
Response of oral leukoplakias to the administration of vitamin A. Cancer Lett 1988 ;
40 : 93-101.
13. Han J, Jiao L, Lu Y, Sun Z, Gu QM, Scanlon KJ. Evaluation of N-4-
(hydroxycarbophenyl) retinamide as a cancer prevention agent and as a cancer
chemotherapeutic agent. In Vivo 1990 ; 4 : 153-60.
14. Spitz MR, Shi H, Yang F, Hudmon KS, Jiang H, Chamberlain RM et al.
Case-control study of the D2 dopamine receptor gene and smoking status
in lung cancer patients. J Nat Cancer Inst 1998 ; 90 : 358-63.
15. Chan G, Boyle JO, Yang EK, Zhang F, Sacks PG, Shah JP et al. Cyclooxy-
genase-2 expression is up-regulated in squamous cell carcinoma
of the head and neck. Cancer Res 1999 ; 59 : 991-4.
16. Grandis JR, Tweardy DJ. Elevated levels of transforming growth factor
alpha and epidermal growth factor receptor messenger RNA are early markers
of carcinogenesis in head and neck cancer. Cancer Res 1993 ; 53 : 3579-84.
17. Shin DM, Ro JY, Hong WK, Hittelman WN. Dysregulation of epidermal
growth factor receptor expression in premalignant lesions during head and neck
tumorigenesis. Cancer Res 1994 ; 54 : 3153-9.
18. Un essai multicentrique de chimioprévention avec l’Iressa®(inhibiteur
del’EGFr) des patients traités chirurgicalement pour une leucoplasie ou une
érythroplasie buccale ou oro-pharyngée va débuter en France au printemps
2002. Pour plus d’informations, contacter les docteurs Jean-Charles Soria
à [email protected] ou Stéphane Temam à [email protected].
1
/
3
100%