Tumeur carcinoïde du grêle métastatique sur terrain à risque cardio-vasculaire :

Correspondances en Métabolismes Hormones Diabètes et Nutrition - Vol. XIV - n° 4 - avril 2010
114
Cas clinique
M
onsieur M., né en 1950, est pris en charge
pour une tumeur carcinoïde digestive métas-
tatique révélée par un syndrome sécrétoire
en mars 2008. Il a présenté un accident vasculaire céré-
bral ischémique sylvien gauche en 2002 sans anoma-
lie cardiaque, vasculaire ou thrombophilique mise en
évidence. Un accident vasculaire cérébral était égale-
ment survenu chez ses deux parents : à 57 ans chez sa
mère, à 65 ans chez son père. Les autres antécédents
de ce patient sont : une intoxication mixte (tabagisme
à 50 paquets-année), des calcications pancréatiques
sans passé de pancréatite aiguë ni de diabète secon-
daire, une appendicectomie, une cure de hernie
inguinale. Son traitement comporte un antiagrégant
plaquettaire, un hypolipémiant, un anxiolytique et un
antidépresseur.
Son histoire débute en 2003, par la survenue de dou-
leurs abdominales diuses, accompagnées de diarrhées
motrices, le plus souvent aqueuses. Il rapporte l’émis-
sion de 4 à 10 selles par jour, déclenchées par la prise
alimentaire (notamment après ingestion de banane ou
de café). La symptomatologie s’est progressivement
enrichie avec l’apparition de ushs du visage et du
thorax, survenant 3 ou 4 fois par jour, durant approxi-
mativement 5 minutes, plus fréquents la nuit ou au
réveil. L’altération de l’état général est plus marquée
depuis quelques mois : asthénie physique, anorexie et
amaigrissement majeur de 20 kg en 6 mois. Des dou-
leurs dorsales exquises en T5-T6 sont présentes lors de
l’examen clinique sans manifestations neurologiques
particulières.
Les premiers examens digestifs sont non contributifs
(échographie abdominale, coloscopie). Les dosages
biologiques orientent le diagnostic vers une tumeur
carcinoïde devant l’élévation spécifique de l’acide
5 hydroxy-indole-acétique (5HIAA) à 20,4 mg/24 h
(< 7) [diurèse de 200 ml, 0,19 g/24 h de créatininurie],
de la sérotonine sérique à 1 315 µg/l (55-180), de la
chromogranine A 445 ng/ml (< 120). Les analyses biolo-
giques standard sont normales. L’exploration digestive
est alors complétée par une vidéocapsule, là encore
non informative. C’est l’entéroscanner qui permettra
de suspecter un foyer primitif du grêle par l’identi-
cation d’une lésion nodulaire endoluminale iléale de
15 mm, se rehaussant fortement au temps artériel. Une
seconde lésion tissulaire de 15 × 27 mm, de contours
spiculés, calciée et se rehaussant discrètement au
temps artériel, est localisée dans la racine du mésentère.
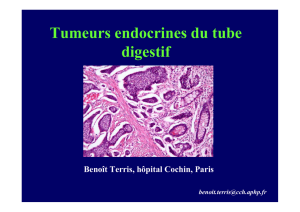
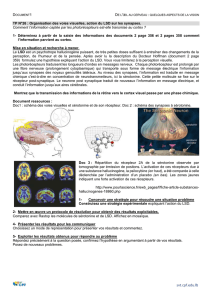
Sont également présents : des adénopathies suspectes
célio-mésentériques, rétropéritonéales, des nodules
de carcinose péritonéale (images 1 et 2), des lésions
hépatiques hypovasculaires infracentimétriques d’al-
lure secondaire.
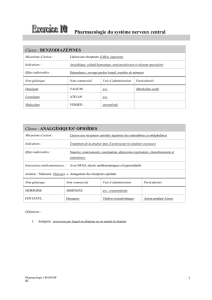
Le bilan d’extension est complété par un Octréoscan
®
qui montre de multiples foyers de xation de la région
abdominale, en intra-hépatique, et à l’étage thoracique
en regard des vertèbres dorsales (images 3 et 4). En
scintigraphie osseuse, il existe plusieurs foyers d’hy-
perxation suspects : le plus intense est situé en regard
de D6-D7 ; un autre foyer, moins intense, latéralisé à
Tumeur carcinoïde du grêle métastatique
sur terrain à risque cardio-vasculaire :
une cardiopathie peu ordinaire
Fanny Mouton, Christine Do Cao*
Images 1 et 2. Entéroscanner – Lésions suspectes de tumeurs neuroendocrines.
1 Coupe coronale. 2 Coupe axiale.
* Services d’endocrinologie,
de diabétologie
et métabolisme,
Marc-Linquette,
hôpital Claude-Huriez, Lille.

Correspondances en Métabolismes Hormones Diabètes et Nutrition - Vol. XIV - n° 4 - avril 2010
115
Tumeur carcinoïde du grêle métastatique sur terrain
à risque cardio-vasculaire : une cardiopathie peu ordinaire
gauche est situé en regard de D10 ; deux derniers foyers
suspects sont visibles au niveau de l’articulation sacro-
iliaque gauche. Les radiographies standard et l’étude du
scanner en fenêtre osseuse centrées sur les segments
osseux hypercaptants ne montrent pas d’image de lyse
corticomédullaire.
Même en l’absence de signes cliniques d’insusance
cardiaque, une évaluation cardiologique systématique
est organisée devant l’importance de la sécrétion
tumorale de sérotonine concordante avec l’atteinte
secondaire hépatique et l’association diarrhée chro-
nique-ushs. L’échocardiographie découvre une fraction
d’éjection réduite à 30 %, un ventricule gauche hypo-
kinétique, une insusance tricuspidienne de grade 2
(discret épaississement tricuspide), une insusance
mitrale de grade 1, une oreillette gauche modérément
dilatée. L’ imagerie par résonance magnétique (IRM)
cardiaque vient confirmer ces données : la fraction
d’éjection est abaissée à 23 % et on constate une aki-
nésie apicale, associée à une prise de contraste tardive
dans le territoire de la marginale correspondant en
coronarographie à une artère marginale thrombosée.
Monsieur M. présente une tumeur carcinoïde du grêle
multimétastatique, compliquée d’une cardiopathie
carcinoïde, mais surtout ischémique. L’attitude théra-
peutique a consisté en une prise en charge cardiolo-
gique en urgence devant l’identication du problème
ischémique. L’introduction des analogues retards de la
somatostatine, destinée à réduire la sécrétion tumorale
de sérotonine et à améliorer la symptomatologie diges-
tive et vasomotrice, a permis au patient de reprendre
une dizaine de kilos. Pour la maladie osseuse ont été
proposées une irradiation externe antalgique et la per-
fusion de biphosphonates intraveineux. L’état général
précaire du patient et surtout l’atteinte cardiaque mixte
n’ont pas permis d’envisager l’exérèse de la lésion pri-
mitive ni la mise en route de traitements systémiques
(cardiotoxicité des chimiothérapies). La chimioemboli-
sation hépatique a été réfutée du fait du caractère peu
vascularisé des lésions.
Discussion
Les carcinomes endocrines bien diérenciés se déve-
loppent à partir de cellules du système neuroendocrine
et correspondent à des tumeurs malignes de croissance
lente. Leur incidence est de l’ordre de 1 à 4 nouveaux
cas/100 000 habitants. Leur pic de fréquence concerne
la 6e-7e décennie (1). Ces tumeurs se rencontrent prin-
cipalement dans le thymus, dans le système broncho-
pulmonaire, dans le pancréas endocrine, dans le tractus
gastro-intestinal, au niveau des gonades, etc. Près
de 42 % des tumeurs endocrines se développent au
niveau de l’intestin grêle ; ces carcinomes endocrines,
en général bien diérenciés et capables de produire
de la sérotonine, répondent également à la dénomi-
nation historique de “tumeurs carcinoïdes”. Deux tiers
des patients atteints de carcinomes endocrines du grêle
présentent une maladie métastatique ganglionnaire
et/ou hépatique au moment du diagnostic.
Les cellules neuroendocrines du tractus digestif peuvent
sécréter de nombreux peptides, dont la sérotonine,
principale hormone incriminée dans les manifestations
cliniques du syndrome carcinoïde. Cette molécule est
synthétisée à partir du tryptophane, elle est cataboli-
sée en 5-hydroxy-indole-acétaldéhyde, puis en acide
5HIAA (métabolite inactif) dans le foie, les poumons
et le rein. On lui connaît le rôle de neurotransmetteur
mais elle possède également des eets systémiques :
vasoconstriction et vasodilatation (via son action sur
le système nerveux autonome), action prothrombo-
gène, accélération du péristaltisme intestinal, donc du
transit intestinal… La sérotonine mais aussi les autres
substances produites par le système endocrine dius
(bradykinine, prostaglandines, kallicréine, substance P,
histamine, etc.) sont habituellement métabolisées et
inactivées par le foie. Ainsi, un syndrome carcinoïde
en provenance d’une lésion intestinale drainée par
les vaisseaux portes n’apparaît qu’en présence de taux
circulants élevés de sérotonine, et d’envahissement
tumoral hépatique ou de masse tumorale fonctionnelle
importante dépassant les capacités de catabolisme
hépatique.
Images 3 et 4. Scintigraphie à l’octréotide marqué à l’indium 111 – Multiples foyers de xations abdo-
minales, hépatiques et dorsales.
3 Face postérieure. 4 Face antérieure.

Correspondances en Métabolismes Hormones Diabètes et Nutrition - Vol. XIV - n° 4 - avril 2010
116
Cas clinique
Un syndrome tumoral (subocclusion, occlusion, saigne-
ment digestif) peut parfois révéler la maladie intestinale
en l’absence de symptomatologie sécrétoire. Quatre à
10 % des patients avec lésions secondaires hépatiques
présentent un syndrome carcinoïde associant classi-
quement diarrhée, ush, bronchoconstriction et car-
diopathie carcinoïde. La symptomatologie est variable
d’un patient à l’autre, comme au cours du temps. Les
ushs peuvent être spontanés ou provoqués par l’in-
gestion de certaines substances comme pour notre
patient. L’existence d’une diarrhée (motrice et sécré-
toire) chronique peut se compliquer d’un syndrome
de malabsorption (2).
L’évaluation biologique chez ces patients comprend
le dosage de 5HIAA dans les urines de 24 heures, de
chromogranine A plasmatique. Ces deux marqueurs
sont des indicateurs pronostiques et sont également
utiles lors du suivi (2).
Le scanner abdomino-pelvien, l’entéroscanner, la colos-
copie ou l’IRM sont les premiers examens réalisés à la
recherche de la lésion primitive, et pour compléter le
bilan d’extension. Si la tumeur primitive n’est pas mise
en évidence, l’échoendoscopie, la vidéocapsule peu-
vent être utiles pour étudier respectivement la région
duodéno-pancréatique et l’intestin grêle. L’imagerie
fonctionnelle repose sur la scintigraphie des récepteurs
à la somatostatine (Octréoscan
®
), qui est un examen
à la fois spécique des tumeurs endocrines et inté-
ressant pour explorer le corps entier. Les métastases
osseuses peuvent être visualisées sur l’Octréoscan
®
,
ou être recherchées spéciquement par une scintigra-
phie osseuse. L’IRM rachidienne ou le scanner rachidien
précisent mieux le risque fracturaire ou neurologique.
La chirurgie est le traitement de référence des tumeurs
endocrines bien diérenciées et localisées. En pré-
sence de métastases hépatiques, elle reste une option
à discuter : l’exérèse du foyer primitif intestinal peut
éviter une complication occlusive et une chirurgie
de réduction tumorale hépatique peut permettre de
réduire le syndrome fonctionnel. En l’absence d’indi-
cation chirurgicale, des traitements locaux tels que la
chimioembolisation hépatique, l’ablation par radiofré-
quence, la cryothérapie représentent des pistes théra-
peutiques en fonction du nombre et de la distribution
des foyers tumoraux (2). Le bénéce des analogues
de la somatostatine est réél dans le contrôle clinique
du syndrome carcinoïde (ecacité dans 40 à 80 % des
cas, en corrélation avec une baisse de sécrétion des
marqueurs biologiques). Leur action antitumorale n’est
pas armée, néanmoins une stabilisation semble être
obtenue pour 50 % à 60 % des patients présentant des
tumeurs progressives et chez des patients ayant un
faible volume tumoral hépatique (3, 4). Les chimiothé-
rapies systémiques donnent des résultats décevants. La
radiothérapie métabolique par les analogues radiomar-
qués de la somatostatine (177 Lu-Dota-octreotate ou
90-Yttrium-Dota-octreotate) constitue une alternative
thérapeutique intéressante à la fois pour le contrôle
symptomatique et tumoral. Ces traitements dispo-
nibles aux Pays-Bas, en Belgique et en Suisse ne sont
pas encore délivrés en France.
L’évaluation cardiaque des patients porteurs de
tumeurs endocrines fonctionnelles est indispensable
dès le moment où une élévation de 5HIAA urinaire
est mise en évidence. L’examen clinique recherchera
un soue tricuspidien, des signes périphériques d’in-
susance ventriculaire droite. L’électrocardiogramme
est le plus souvent normal. L’échocardiographie est
un temps essentiel, elle évalue la fonction cardiaque
globale, la morphologie et la mobilité des valves. L’IRM
cardiaque permet une étude plus ne de la morpho-
logie cardiaque. En 1993, P.A. Pellikka a évalué la fonc-
tion cardiaque de 74 patients, 56 % étaient porteurs
d’un retentissement cardiaque dont la majorité pré-
sentait un épaississement de la valve tricuspide (plus
ou moins rétractée) responsable d’une insusance
tricuspidienne. L’atteinte de l’endocarde correspond
à des dépôts de tissu breux, localisée préférentiel-
lement au niveau du cœur droit (la sérotonine et les
autres molécules vasoactives sont inactivées lors du
passage pulmonaire). L’atteinte est valvulaire mais
concerne aussi les cordages et les muscles papillaires.
L’épaississement valvulaire tricuspidien ainsi que pulmo-
naire doit être recherché de façon attentive. L’atteinte
valvulaire du cœur gauche est rare (7 % des patients
selon P.A. Pellikka, en raison soit d’un foramen ovale,
soit d’un foyer tumoral pulmonaire). L’atteinte cardiaque
carcinoïde semble bien corrélée à l’exposition à la séro-
tonine. La production de 5HIAA est signicativement
plus importante chez les malades porteurs d’une car-
diopathie carcinoïde. L’atteinte cardiaque est par ailleurs
un facteur indépendant de mauvais pronostic (5-8). Le
taux de survie dépend du stade, de la diérenciation
de la maladie. Il est évalué à 5 ans, à 65 % en l’absence
de métastases, et à 36 % en présence de localisations
secondaires ; il dépend également de l’existence d’une
atteinte cardiaque (taux de survie à 3 ans : 68 % sans
atteinte cardiaque, 31 % avec) [1, 7].
En ce qui concerne la physiopathologie de l’atteinte
cardiaque ischémique, notre patient présente de façon

Correspondances en Métabolismes Hormones Diabètes et Nutrition - Vol. XIV - n° 4 - avril 2010
117
Tumeur carcinoïde du grêle métastatique sur terrain
à risque cardio-vasculaire : une cardiopathie peu ordinaire
indéniable de nombreux facteurs de risque cardio-
vasculaires héréditaires et environnementaux. Au-delà
de ces facteurs vasculaires classiques reconnus, existe-
t-il un impact de la pathologie néoplasique carcinoïde
sur la coronaropathie ? L’atteinte coronaire a pu en eet
être favorisée par la sécrétion tumorale de sérotonine,
par le biais d’eets vasculaires. Celle-ci possède des
actions chimiotactiques, trophiques et mitogènes sur
les cellules endothéliales, un eet prothrombotique
via une vasoconstriction coronaire (action directe
ou médiée via d’autres hormones : noradrénaline,
endothéline, etc.). La sérotonine induit ainsi une
hyperagrégabilité plaquettaire pouvant favoriser le
développement et l’aggravation de lésions d’athé-
rosclérose (9).
Conclusion
Il s’agit d’une observation inhabituelle de cardiopathie
mixte, plurifactorielle, dans un contexte de tumeur car-
cinoïde du grêle métastasée. La sérotonine, produite en
excès par les cellules tumorales digestives, non dégra-
dée par le foie en raison de la dissémination hépatique,
a pu accéder aux cavités et aux vaisseaux cardiaques.
Les actions prothrombotiques, trophiques, brosantes
induites par la sérotonine ont contribué ou favorisé
chez notre patient (en addition aux facteurs vasculaires
existants) une double atteinte cardiaque : carcinoïde
et ischémique. La double atteinte cardiaque ainsi que
l’extension tumorale ont été deux facteurs décisifs dans
la prise en charge et pour le devenir de ce patient.
■
1.
Modlin IM, Lye KD, Kidd M. A 5-decade analysis of 13,715
carcinoid tumors. Cancer 2003;97(4):934-59.
2. Plockinger U, Rindi G, Arnold R et al. Guidelines for the
diagnosis and treatment of neuroendocrine gastrointestinal
tumours. A consensus statement on behalf of the European
Neuroendocrine Tumour Society (ENETS). Neuroendocrinology
2004;80(6):394-424.
3.
Massironi S, Sciola V, Peracchi M, Ciafardini C, Spampatti
MP, Conte D. Neuroendocrine tumors of the gastro-entero-
pancreatic system. World J Gastroenterol 2008;14(35):5377-84.
4. Rinke A, Müller HH, Schade-Brittinger C et al. Placebo-
controlled, double-blind, prospective, randomized study
on the effect of octreotide LAR in the control of tumor
growth in patients with metastatic neuroendocrine midgut
tumors: a report from the PROMID Study Group. J Clin Oncol
2009;27(28):4656-63.
5. Meijer WC, Van Veldhuisen DJ, Kema IP et al. Cardiovascular
abnormalities in patients with a carcinoid syndrome. Neth J
Med 2002;60(1):10-6.
6. Fox DJ, Khattar RS. Carcinoid heart disease: presentation,
diagnosis, and management. Heart 2004;90(10):1224-8.
7. Pellikka PA, Tajik AJ, Khandheria BK et al. Carcinoid heart
disease. Clinical and echocardiographic spectrum in 74
patients. Circulation 1993;87(4):1188-96.
8. Zuetenhorst JM, Bonfrer JM, Korse CM, Bakker R, Van
Tinteren H, Taal BG. Carcinoid heart disease: the role of uri-
nary 5-hydroxyindoleacetic acid excretion and plasma levels
of atrial natriuretic peptide, transforming growth factor-beta
and fibroblast growth factor. Cancer 2003;97(7):1609-15.
9.
Mekontso Dessap A. Sérotonine et pathologie cardiovascu-
laire. Implication dans les valvulopathies cardiaques, la mala-
die coronaire et le remodelage vasculaire. Thèse de doctorat,
école doctorale Sciences de la vie et de la santé, université
Paris-Est, soutenue en 2008.
R é f é r e n c e s
Les articles publiés dans “Correspondances en Métabolismes-Hormones-Diabètes et Nutrition” le sont sous la seule responsabilité de leurs auteurs.
Tout droits de reproduction, d’adaptation et de traduction par tous procédés réservés pour tous pays.
© octobre 1997 - Edimark SAS (éditions DaTeBe)
Imprimé en France – Axiom Graphic SAS - 95830 Cormeilles-en-Vexin – Dépôt légal à parution
1
/
4
100%