Lire l'article complet

ASCO 2007
Nouvelles thérapies
273
1
0,75
Jours depuis la randomisation
Sorafénib + DTIC (n = 36)
Médiane : 21,1 semaines (IC95 : 16,0-28,0)
Placebo + DTIC (n = 40)
Médiane : 11,7 semaines (IC95 : 6,1-17,9)
Hazard-ratio = 0,619 (p = 0,039)
0,50
0,25
0 100 200 300 400 500 600
Temps jusqu'à progression (survie)
0
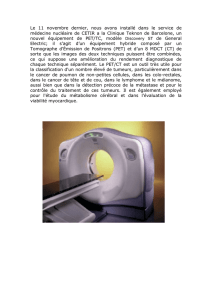
Figure 1.
Survie en temps jusqu’à progression dans l’étude DTIC
± sorafénib.
La Lettre du Cancérologue - Vol. XVI - n° 6-7 - juin-juillet 2007
Nouvelles thérapies – Mélanome métastatique
New drugs – Metastatic melanoma
●● M. Saghatchian d’Assignies*
* Comité de pathologie mammaire, Institut Gustave-Roussy, Villejuif.
L
es nouvelles thérapies étaient les stars de cet ASCO 2007,
et l’on voit enfi n aboutir sur le plan clinique cette stra-
tégie de ciblage thérapeutique en développement depuis
plusieurs années.
L’innovation et le progrès proviennent maintenant du position-
nement stratégique de ces drogues, tant dans les indications
tumorales que dans les associations ou séquences utilisées, et
de l’exploration de nouvelles cibles.
Les diff érentes études présentées dans ce chapitre illustrent
ces tendances :
Positionnement innovant de nouvelles drogues dans le méla-
nome.
Exploration de nouvelles cibles comme les HDAC (histones
désacétylases) et l’IGF-R (insulin-like growth factor receptor).
Positionnement innovant de drogues ayant de nouvelles
cibles, comme les inhibiteurs d’intégrines dans les tumeurs
cérébrales.
MÉLANOME
Le mélanome au stade avancé
est une cible de choix pour les
nouvelles drogues compte tenu des faibles possibilités thérapeu-
tiques et de la physiopathologie propres à ces tumeurs.
L’étude la plus intéressante de cet ASCO 2007 dans cette indi-
cation est l’étude de phase II randomisée comparant la dacar-
bazine (DTIC) associée au sorafénib à la dacarbazine seule chez
des patients présentant un mélanome avancé (McDermott DF,
abstract 8511).
Le sorafénib est un inhibiteur multicible de kinase anti-VEGFR-1,
-2, -3, PDGFR-α, -β et Raf.
Il s’agit d’une étude multicentrique en double aveugle compa-
rant dacarbazine-sorafénib à dacarbazine-placebo en première
ligne métastatique.
Les patients étaient traités par dacarbazine 1 000 mg/m² tous les
21 jours + placebo oral ou sorafénib 400 mg deux fois par jour
tous les jours jusqu’à progression ou intolérance au traitement.
Au total, 101 patients ont été inclus (dont 51 dans le bras avec
sorafénib).
Les données d’effi cacité sont résumées dans le tableau I.
La fi gure 1 montre les courbes de temps jusqu’à progression
dans chaque bras.
L’association avec le sorafénib apporte donc un gain non signi-
fi catif en termes de survie sans progression, mais signifi catif en
termes de temps jusqu’à progression, de 9,4 semaines (3 à 5 mois),
▶
▶
▶
sans bénéfi ce toutefois en termes de survie globale. Les toxicités
(grade 3 ou plus) comprenaient essentiellement, dans le bras avec
sorafénib, des cas de neutropénies (33 %), de thrombopénies
(35 %), d’accidents thromboemboliques (6 %), d’hypertension (8 %),
d’hémorragies cérébrales (8 %, les trois quarts étant survenues chez
des patients présentant de nouvelles métastases cérébrales).
Cette association, dont la tolérance reste acceptable, représente
sans doute une véritable avancée thérapeutique, même si l’étude
n’est pas positive en termes de survie globale. En eff et, avec une
médiane de survie globale de 11,1 mois, l’étude avait une puis-
Tableau I.
Mélanome avancé : étude DTIC ± sorafénib.
DTIC + placebo
n = 50
DTIC + sorafénib
n = 51 p
Réponses objectives
(réponses complètes
+ réponses partielles)
12 24 NS
Béné ce clinique
(RO + stabilisations) 56 71 NS
Progressions 42 29
Taux de progression
à 6 mois 20 % 41 %
Médiane de temps
jusqu’à progression 11,7 semaines 21,1 semaines p = 0,039
Médiane de survie
sans progression 11,7 semaines 21,1 semaines p = 0,068
Médiane de survie
globale (analyse
intermédiaire)
45,6 semaines 51,3 semaines NS

ASCO 2007
Nouvelles thérapies
274
La Lettre du Cancérologue - Vol. XVI - n° 6-7 - juin-juillet 2007
sance de 20 % pour détecter une diff érence de 5 mois de survie,
l’analyse en survie étant encore une analyse intermédiaire.
Il faut cependant noter que l’étude de phase III randomisée
comparant l’association paclitaxel-carboplatine avec ou sans
sorafénib présentée lors de la même session est en revanche
négative (Agarwala SS et al., abstract 8510). Dans cette étude,
il s’agissait toutefois de patients en deuxième ligne métastatique
après une première ligne de traitement par dacarbazine ou
témozolomide.
Cette grande étude de 270 patients randomisés n’a pas permis
de montrer de diff érence en termes de survie sans rechute ou
de taux de réponse objective (11 % versus 12 %).
La question de l’effi cacité de cette association reste cependant
pertinente, et une grande étude de phase III, cette fois-ci menée
en première ligne (à l’instar de l’étude dacarbazine-sorafénib),
est en cours.
Sur le terrain de l’adjuvant
, deux études de phase III sur l’in-
terféron alpha chez des patients atteints de mélanome à haut
risque de rechute rapportent des résultats positifs.
L’étude EORTC 18991, présentée par A.M. Eggermont, est la plus
grande étude adjuvante jamais réalisée dans cette indication. Elle
comparait l’interféron pégylé (PEG-IFN) [induction à 6 μg/ kg/
semaine par voie s.c. pendant 8 semaines suivie d’un traitement
de maintenance à 3 μg/kg/semaine par voie s.c. pendant 5 ans]
à une surveillance sans traitement (standard actuel) chez des
patients atteints de mélanome de stade III. Une stratifi cation
selon diff érents facteurs pronostiques permettant une analyse
en sous-classes était prévue.
L’avantage du PEG-IFN est son profi l de tolérance permettant
des administrations prolongées.
Cette étude a porté sur 1 256 patients avec un suivi médian
de 3,8 ans.
Les résultats sont positifs en termes de survie sans rechute
(locale et métastatique).
En revanche, les données en termes de survie sans rechute
métastatique à distance et de survie globale ne sont pas signi-
fi catives (tableau II).
Tableau II.
Mélanome adjuvant : survie dans l’étude EORTC 18991.
Survie sans rechute Survie sans rechute
métastatique Survie globale
Surveillance PEG-IFN Surveillance PEG-IFN Surveillance PEG-IFN
Taux à 4 ans (%) 39 46 45 48 56 57
Médiane
(années) 2,1 2,9 3,0 3,8 Non
atteinte
Non
atteinte
p 0,01 0,11 0,78
Cependant, les résultats pour le sous-groupe de patients N1
(43 % des patients) sont positifs en termes de survie sans rechute
et de survie sans rechute métastatique.
La compliance au traitement a été médiocre, avec 251 patients
(40 %) qui ont arrêté le PEG-IFN pour toxicité, celle-ci compre-
nant essentiellement l’asthénie (15 %), l’hépatotoxicité (10 %)
et le syndrome dépressif (6 %). Au total, en incluant les arrêts
pour toxicité et/ou progression, 23 % des patients ont reçu le
traitement pendant une durée de 4 à 5 ans.
Ce traitement semble donc surtout bénéfi cier aux patients
présentant un envahissement ganglionnaire microscopique
(ganglion sentinelle positif).
Une autre étude de phase III (Gogas H et al., abstract 8505)
présentée pendant cet ASCO 2007 comparait dans la même
indication le bénéfi ce clinique de 4 semaines d’IFN à haute dose
en traitement d’induction à un an d’IFN à haute dose.
Cette étude montre que les 4 semaines de traitement d’induc-
tion i.v. peuvent être aussi effi caces que le traitement standard
sous-cutané pendant un an, avec une meilleure compliance
au traitement (94 % versus 69 % des patients ont pu recevoir la
totalité de leur traitement).
Cependant, il faut noter que l’IFN dans le bras “un an” était
sous-dosé par rapport au standard habituel.
INHIBITEURS DE HSP
Hsp 90 est la protéine chaperonne nécessaire au remodelage
des protéines en cas de stress cellulaire et à la maturation des
protéines impliquées dans la signalisation intracellulaire. L’in-
hibition de Hsp 90 par le 17-AAG induit la dégradation dans
le protéasome des molécules clientes comme HER2, Raf, Akt
ou les récepteurs stéroïdiens.
La tanespimycine (17-AAG/KOS 953) est un antibiotique inhi-
biteur de Hsp 90 dont le développement se poursuit depuis
plusieurs années et qui compte actuellement parmi les drogues
les plus prometteuses de cette classe. Les premières études en
monothérapie montraient un bon profi l de tolérance, mais une
effi cacité antitumorale limitée.
Plusieurs nouvelles études intéressantes avec cette drogue dans
diverses associations et dans des situations cliniques variées
(tableau III) ont fait l’objet de présentations orales cette
année.
L’étude de phase I en association au sorafénib (Vaisham-
payan UN et al., abstract 3531) dans diverses tumeurs solides
a inclus 19 patients (cette étude du National Cancer Institute est
Tableau III.
Études d’association avec le 17-AAG (tanespimycine).
Schéma 17-AAG Drogue associée Tumeurs Toxicité E cacité
> 300 mg/m
i.v. 3 h
J1, J8, J15
J1 = J28
Sorafénib p.o.
400 mg x 2
Rein
Côlon
Mélanomes
Tolérance bonne
DLT non atteinte
1 RP
6 stabilisations
100-340 mg/m
i.v. 1 h
J4, J8, J11
J1 = J21
Bortézomib
i.v. directe
0,7-1,3 mg/m2
Myélomes
réfractaires
ou en rechute
post-bortézomib
Thrombopénie
G3
(16 %)
Réponses même
chez les patients
réfractaires
i.v. 2 h
J1, J8
J1 = J21
Irinotécan
i.v. 30 mn
100 mg/m
Tumeurs solides
Nausées-
vomissements
Diarrhées
Embolie
pulmonaire
Pancréas
Sein
TNE haut grade

ASCO 2007
Nouvelles thérapies
275
La Lettre du Cancérologue - Vol. XVI - n° 6-7 - juin-juillet 2007
encore ouverte). Le rationnel pour l’association est de combiner
une action anti-VEGF à une action intracellulaire en aval par
l’inhibition de Raf-kinase. Le sorafénib était administré à la dose
conventionnelle de 400 mg deux fois par jour, et le 17-AAG était
ensuite ajouté deux semaines après à doses progressivement
croissantes (à partir de 300 mg/m² i.v. en 3 heures à J1, J8 et J15
tous les 28 jours). Diff érents types de tumeurs ont été traités
(dont 6 cancers du rein à cellules claires, 1 cancer papillaire du
rein, 4 cancers colorectaux et 3 mélanomes). Il y a eu au total
une réponse partielle et 6 stabilisations, l’ensemble du traitement
étant par ailleurs bien toléré et la DLT non atteinte.
L’équipe du Dana Farber Cancer Institute (Richardson PG et al.
abstract 3532) a mené une étude de l’association au bortézomib
(Velcade
®
) dans le myélome. Le bortézomib est un inhibiteur
du protéasome 26S qui est responsable de la dégradation des
protéines sur lesquelles est fi xée l’ubiquitine. La voie ubiqui-
tine-protéasome joue un rôle essentiel dans l’organisation du
renouvellement des protéines spécifi ques. L’inhibition du protéa-
some 26S empêche cette protéolyse ciblée et aff ecte de multi-
ples cascades de signaux à l’intérieur de la cellule, entraînant la
mort de la cellule cancéreuse. Le bortézomib est actuellement
indiqué dans le traitement du myélome en troisième intention.
Les études précliniques suggèrent une synergie potentielle entre
les inhibiteurs de Hsp 90 et les inhibiteurs du protéasome.
Dans cette étude, la tanespimycine (17-AAG) était administrée
en perfusion d’une heure à J1, J4, J8 et J11 tous les 21 jours à
la suite du bortézomib injecté en i.v. directe.
Au total, 49 patients ont été inclus dans 7 cohortes de doses
(tanespimycine 100-340 mg/m² ; bortézomib 0,7-1,3 mg/m²).
Dans la dernière cohorte de traitement (tanespimycine 340/
bortézomib 1,3 mg/m²), les eff ets secondaires les plus fréquents
étaient : diarrhée (42 %), nausées (32 %), vomissements (26 %),
augmentation des enzymes hépatiques AST/ALT/phosphatases
alcalines (26 %/21 %/21 %), myalgies (16 %) et confusion (16 %).
La seule toxicité de grade 3 était la thrombopénie (16 %).
Des réponses ont été observées chez des patients naïfs de trai-
tement par bortézomib ou prétraités ou même réfractaires
au bortézomib (27 % de réponse objective observée pour ces
patients).
Dans l’étude du Memorial Sloan-Kettering Cancer Center
(Tse AN et al., abstract 3533), la molécule a été associée à l’iri-
notécan, inhibiteur de la topo-isomérase I, avec lequel son action
est synergique. Dans cette étude de phase I, les patients rece-
vaient l’irinotécan en perfusion de 30 minutes suivi du 17-AAG
administré en 2 heures une fois par semaine pour 2 semaines
tous les 21 jours. Des biopsies tumorales post-traitement étaient
par ailleurs réalisées. L’étude a inclus 22 patients présentant des
tumeurs variées.
Les toxicités dose-limitantes sont apparues chez 4 patients aux
doses de 100 mg/m² d’irinotécan et de 375 mg/m² de 17-AAG :
nausées, vomissements, diarrhée et embolie pulmonaire. Il
n’y avait pas d’interaction pharmacocinétique entre les deux
molécules.
Il y a eu quelques réponses mineures chez des patients n’ayant
pas reçu préalablement d’irinotécan et présentant des cancers
du pancréas (2), du sein (1), et des tumeurs neuro-endocrines
de haut grade (1).
La dose recommandée en phase II est de 100 mg/m² d’irinotécan
et de 300 mg/m² de 17-AAG.
INHIBITEURS DE HDAC
Les inhibiteurs des histones désacétylases (HDACi) appartien-
nent à une classe thérapeutique à part dont le développement est
particulièrement intéressant en hématologie avec, récemment,
des études prometteuses dans les tumeurs solides. Le vorinostat
est la première de ces molécules à avoir été commercialisée aux
États-Unis dans les lymphomes T cutanés (en octobre 2006).
Ces molécules permettent l’acétylation des histones, la relaxa-
tion de la structure chromatinienne et ainsi la réactivation des
gènes régulateurs du cycle cellulaire (en particulier des gènes
suppresseurs de tumeurs anormalement réprimés dans les
cellules tumorales). On parle dans ce cas de ciblage thérapeu-
tique épigénétique.
Plusieurs molécules sont à l’étude et se distinguent essentiel-
lement par l’inhibition plus ou moins sélective des diff érents
isotypes d’HDAC.
Le MGCD0103 est un inhibiteur sélectif de certains isotypes
(HDAC1, 2, 3 et 11) et fait cette année une apparition remarquée
dans la maladie de Hodgkin (déjà présenté en 2006 en phase I
de tumeurs solides).
Dans l’étude de phase II présentée en session orale (Younes A
et al., abstract 8000), parmi les 20 patients évaluables, tous
préalablement multitraités pour un lymphome hodgkinien en
rechute (et pour certains ayant progressé lors de toutes les lignes
précédentes), le MGCD0103 en monothérapie était administré
par voie orale à 110 mg 3 x/semaine pendant 4 semaines. Le
traitement a permis de contrôler la maladie dans 45 % des cas,
avec 40 % de réponses objectives (réponses complètes et réponses
partielles) ! L’effi cacité a été évaluée chez 22 patients, permettant
d’obtenir deux réponses complètes (10 %), 6 réponses partielles
(30 %), 1 stabilisation de plus de 6 mois (5 %), 8 stabilisations de
moins de 6 mois (40 %) et 3 progressions (15 %).
Le traitement est par ailleurs extrêmement bien toléré, les
nausées et la fatigue étant les eff ets indésirables les plus gênants
(toxicités de grade 3 : asthénie [2 %], thrombopénie [10 %], toxi-
cités de grade 1-2 les plus fréquentes : nausées, vomissements,
diarrhée, dyspnée, asthénie, anorexie, perte de poids).
Il s’agit donc là d’un nouvel espoir, dans une maladie globale-
ment de bon pronostic, mais dont les formes réfractaires ou en
rechute constituent encore un défi thérapeutique.
Le LBH589 est le nouvel inhibiteur d’HDAC qui agit sur les
classes I, II et IV, comme le vorinostat.
Il a été évalué dans une étude de phase I (Prince HM et al.,
abstract 3500) dans les tumeurs solides et les lymphomes non
hodgkiniens, en particulier T cutanés. Le traitement était admi-
nistré trois fois par semaine par voie orale, et des lymphocytes
périphériques étaient prélevés afi n d’évaluer l’état d’acétylation
des histones après traitement (par Western-Blot).

ASCO 2007
Nouvelles thérapies
276
Hypothalamus
Foie
IGF-I
Hormone de croissance (GH)
GHRH
IGFBP-3
Cellules cibles
Autocrine
IGF-I, IGF-II
Paracrine
IGF-I, IGF-II
Endocrine
IGF-II
Récepteur GH
Somatostatine
Hypophyse
Figure 2.
Régulation de la sécrétion des IGF.
Métabolisme
Insuline IGF-II
IGF-I
Prolifération Métastases Survie
InsR-B InsR-A InsR-A/
IGF-IR InsR-B/
IGF-IR IGF-IR IGF-IIR
Figure 3.
Ligands et récepteurs.
La Lettre du Cancérologue - Vol. XVI - n° 6-7 - juin-juillet 2007
Au total, 32 patients ont été traités, présentant : lymphome T
cutané (10), cancer du rein (6), mélanome (6), cancer de la pros-
tate (4), carcinome hépatocellulaire (1), rhabdomyosarcome (1),
mésothéliome (1), cancer du côlon (1), cancer de la vessie (1)
et cancer de la parotide (1).
Les patients ont reçu des doses de 15 mg (3), 20 mg (19) et
30 mg (10).
Les toxicités correspondaient à celles habituellement retrouvées
avec cette classe pharmaceutique, soit, pour les toxicités dose-
limitantes (30 mg) : thrombopénie, diarrhée ; pour les toxicités
de grade 3-4 : asthénie (5 %), thrombopénie (21 %). Les toxicités
les plus fréquentes étaient : nausées-vomissements, diarrhée,
asthénie, anorexie, œdème.
Au total, 1 057 ECG ont été réalisés, retrouvant un allongement
du QTcF de 503 m/s chez un seul patient, survenant de façon
spontanément résolutive et isolée. L’acétylation des histones a
été mise en évidence à partir de la dose de 20 mg chez plus de
50 % des patients à 72 heures après traitement.
La pharmacocinétique était linéaire entre 15 et 30 mg.
Les réponses ont été notables, en particulier dans les lympho-
mes T cutanés, avec deux réponses complètes, quatre réponses
partielles et deux stabilisations. Des stabilisations ont également
été obtenues dans les tumeurs solides : cancer du rein, 2 patients
(3,5 et 7 mois) ; mélanome, un patient (4 mois) ; mésothéliome,
un patient (2,5 mois) ; parotide, un patient (5 mois).
INHIBITEURS DE L’IGFIR
Le récepteur de l’IGF-I (insulin-like growth factor 1) et ses ligands
ont été impliqués dans de nombreux types de cancers (cancer
du sein, de la prostate, du côlon, du poumon, de la thyroïde,
glioblastomes, etc.).
Ces cancers sont souvent associés à une surexpression et/ou à
une suractivation du récepteur de l’IGF-I, ainsi qu’à une produc-
tion anormale de ses principaux ligands (IGF-I et IGF-II).
IGF- I et IGF-II sont présents dans la circulation sanguine,
mais également exprimés localement dans le tissu tumoral. La
biodisponibilité de ces ligands est régulée par la famille des IGF
binding proteins (IGFBPs1-6).
La fi gure 2 montre le schéma de régulation de la sécrétion de
ces molécules.
Le récepteur de l’IGF-I (IGF-IR) fait partie de la famille du récep-
teur de l’insuline (InsR), avec lequel il présente 60 % d’homologie.
La liaison du ligand à son récepteur induit l’activité tyrosine
kinase du récepteur envers des substrats intracellulaires.
L’InsR et l’IGF-IR partagent plusieurs substrats et plusieurs
voies de signalisation (voie de MAP kinases, voie PI3-kinase/
PKB, etc.).
L’IGF-IR est généralement considéré comme un récepteur
contrôlant la croissance cellulaire, alors que l’InsR est plutôt
considéré comme un récepteur contrôlant le métabolisme
énergétique. Cependant, les eff ets biologiques induits par ces
récepteurs ne sont pas toujours clairement distincts : l’IGF-IR
a des eff ets métaboliques importants, alors que l’InsR a, pour
sa part, des eff ets bien documentés sur la croissance, la proli-
fération et la diff érenciation cellulaire (fi gure 3). Il apparaît en
outre que le récepteur de l’insuline peut lui aussi jouer un rôle
important dans certains processus de cancérogenèse.
Enfi n, dans plusieurs tissus a été mise en évidence la présence
d’hétérodimères IR/IGF-IR qui ont des eff ets biologiques se
rapprochant plutôt de ceux de l’IGF-IR. Ces hétérodimères
semblent jouer un rôle majeur dans la signalisation par l’IGF-I
dans certaines lignées dérivées de cancers du côlon, dans les
cancers de la thyroïde et dans les cancers du sein.
De nombreuses molécules ciblant le récepteur de l’IGF-I sont en
développement : il s’agit soit d’inhibiteurs de tyrosine kinase du
récepteur, soit d’anticorps monoclonaux, le développement de
ces derniers étant plus avancé, avec de nombreuses molécules
actuellement en étude de phases I et II.
Le CP-751871 est un anticorps monoclonal humain IgG2 ciblant
l’IGF-IR, avec une spécifi cité élevée. Lorsque l’anticorps se fi xe,
il induit une internalisation et une dégradation du récepteur.

ASCO 2007
Nouvelles thérapies
277
La Lettre du Cancérologue - Vol. XVI - n° 6-7 - juin-juillet 2007
Plusieurs études de phase I avaient montré son bon profi l de
tolérance.
Il a été présenté cette année dans une étude de phase II (Karp DD
et al., abstract 7506) randomisée, non comparative, en association
au paclitaxel (T) et au carboplatine (C) versus TC seul dans les
cancers du poumon non à petites cellules de stades IIIB, IV ou en
rechute, chez des patients n’ayant jamais reçu de chimiothérapie.
Les patients étaient randomisés selon un ratio 2:1 et recevaient :
T (200 mg/m²), C (ASC 6) et inhibiteur de IGF-1R (I) [10 mg/kg],
ou TC seul toutes les 3 semaines pour 6 cycles. Les patients
répondeurs ou stables après 6 TCI pouvaient continuer à bénéfi -
cier de l’anticorps seul jusqu’à progression. Les patients progres-
sant sous TC seul pouvaient bénéfi cier de l’anticorps seul ou en
association au TC, selon l’appréciation de l’investigateur.
Une analyse intermédiaire a été réalisée après inclusion de
73 patients (48 dans le bras TCI ; 25 dans le bras TC).
Le traitement par TCI était bien toléré, avec comme toxicité
de grade 3/4 : hyperglycémie (20 % TCI, 10 % TC), asthénie
(15 % TCI, 8 % TC), neutropénie (13 % TCI, 20 % TC) et neuro-
pathie (10 % TCI, 4 % TC).
Les taux de réponse étaient élevés (RO) : 22 patients sur 48 dans
le bras TCI (46 %) et 8 patients sur 25 dans le bras TC (32 %).
De plus, dans le bras TCI, 14 des 27 patients (52 %) présentant
des adénocarcinomes ont répondu au traitement.
Par ailleurs, l’un des 4 patients ayant reçu l’anticorps seul après
progression sous TC a répondu au traitement.
Cette classe thérapeutique est donc pleine de promesses et
l’essai va être poursuivi.
SYSTÈME NERVEUX CENTRAL
On n’y croyait plus et, pourtant, c’est dans cette tumeur parti-
culièrement diffi cile à traiter que les nouvelles thérapies sont
en train de changer l’histoire de la maladie.
La piste des antiangiogéniques devient la route de l’espoir avec
plusieurs essais thérapeutiques montrant l’effi cacité de ces trai-
tements dans les gliomes malins.
Les antiangiogéniques semblaient intéressants dans cette indi-
cation compte tenu des fortes concentrations de récepteur au
VEGF retrouvées dans ces tumeurs comme facteur de mauvais
pronostic.
La stratégie étant d’associer ces molécules à la chimiothérapie
pour potentialiser leur effi cacité, le choix de la chimiothérapie
n’était pas simple dans cette indication.
Parmi les drogues existantes, l’irinotécan, inhibiteur de la topo-
isomérase 1, a une faible activité dans les gliomes malins et,
surtout, une excellente pénétration à travers la barrière hémato-
méningée.
Le bévacizumab a donc été testé en association à l’irinotécan
dans un essai de phase II chez des patients atteints de gliome
malin en rechute et préalablement traités par radiothérapie et
témozolomide (Goli KJ et al., abtract 2003). Les patients (au
total 68, dont 35 présentant des tumeurs de grade IV et 33 des
tumeurs de grade III) ont été traités au sein de deux cohortes
testant deux schémas thérapeutiques diff érents.
La première cohorte de 32 patients comportait un schéma d’admi-
nistration tous les 15 jours d’irinotécan associé au bévacizumab.
La seconde cohorte recevait l’irinotécan en hebdomadaire associé
au bévacizumab toutes les 3 semaines.
Le traitement était bien toléré, avec seulement une hémorragie
cérébrale après 10 cycles de traitement. Il y a eu 8 complications
thromboemboliques, dont 2 décès.
Le taux de réponse au traitement a été impressionnant : 59 % de
réponse (38 réponses partielles et 2 réponses complètes !). Ces
taux de réponses se traduisent, dans les tumeurs de grade IV et
de grade III respectivement, par une survie sans progression de
23 semaines et 42 semaines et une survie globale de 40 semaines
et 60 semaines.
Le bras optimal de traitement était le bras de traitement tous
les 15 jours.
Ces données d’effi cacité de la stratégie antiangiogénique dans
cette indication semblent par ailleurs confi rmées par les études
à un stade plus précoce de développement d’une nouvelle molé-
cule, le cilengitide (EMD121974), un inhibiteur des intégrines
αvβ3 et αvβ5.
Ces molécules ont plusieurs modes d’action :
action antiangiogénique ;
action antitumorale ;
synergie avec les agents alkylants ;
action sur les vaisseaux tumoraux qui expriment les intégrines
αvβ3 et αvβ5 ;
action sur les glioblastomes qui expriment les intégrines
αvβ3 ;
action en association à la radiothérapie qui induit l’expression
des intégrines.
La molécule a été testée en association avec le témozolomide et
la radiothérapie concomitante (équipe de R. Stupp à Lausanne,
étude de phase I/IIa), et les taux de survie sans progression
à 6 mois sont encourageants par rapport à ceux des séries
historiques.
Une étude américaine de phase II a également évalué la molécule
en monothérapie après rechute chez des patients préalablement
traités par radiothérapie et témozolomide : des stabilisations
prolongées sous traitement chez certains patients témoignent
de son effi cacité potentielle.
La voie des antiangiogéniques dans cette indication semble
donc bien tracée. ■
▶
▶
▶
▶
▶
▶
1
/
5
100%