Pharmacologie du SRA

PH A R M A C O L O G I E D E S D I U R E T I Q U E S
Objectifs :
- connaître les mécanismes d’action des diurétiques
- savoir classer les diurétiques
- connaître les principaux EI
- connaître les modalités de surveillance
DEFINITION
Diurétiques = qui augmentent le volume des urines et la technique est d’augmenter l’excrétion sodée (et donc l’excrétion d’eau).
Tous sont des natriurétiques (salidiurétiques) :
- en diminuant la réabsorption tubulaire du sodium (le but de la réabsorption du sodium est de garder un capital sodé constant dans
l’organisme)
- entraînent une perte d’eau augmentation de la diurèse (conséquence de l’hypernatriurèse)
CLASSIFICATION
- selon leur mécanisme d’action = lieu d’effet sur le néphron
- selon l’intensité de leur effet diurétique (importance de l’action natriurétique)
- selon leur effet sur la kaliémie (augmente ou diminue)
I. Généralités
Ce sont des médicaments très prescrits. Leurs indications sont multiples en particulier en cardiologie, néphrologie, hépatologie… mais ils sont à
manier avec précautions (source de pathogénies iatrogènes).
La iatrogénie est un pourvoyeur majeur de déshydratation globale chez les PA, avec
pour premiers responsables les diurétiques.
Les principaux diurétiques sont :
- Les thiazidiques
- Les diurétiques de l’anse
- Les inhibiteurs de l’anhydrase carbonique
- Les diurétiques anti-aldostérone
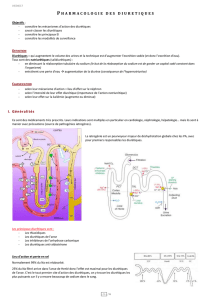
Lieu d’action et perte en sel
Normalement 99% du Na est réabsorbé.
25% du Na filtré arrive dans l’anse de Henlé donc l’effet est maximal pour les diurétiques
de l’anse. C’est le tout premier site d’action des diurétiques, on y trouve les diurétiques les
plus puissants car il y a encore beaucoup de sodium dans le sang.

II. Diurétique de l’anse
Leur site d’action est la partie ascendante de l’anse de Henlé.
Le furosémide est le diurétique de référence parmi les diurétiques de l’anse
inhibition du co-transport Na/K contre 2 Cl.
A. Effets
Action au niveau de la branche ascendante de l’anse de Henlé :
- diminution de la réabsorption du Na (effet sur le transporteur
Na/K/Cl)
- diminution de la réabsorption du K+ (déplétion potassique)
- modification du gradient transépithélial : diminution de la réabsorption de calcium et de magnésium
Action en aval :
- échange K+/H+ : explique l’alcalose métabolique
Ce sont des substances de type dérivés sulfamidés :
- résorption digestive rapide (biodisponibilité moyenne de 66% mais variation si bas débit = problème hémodynamique ; la molécule
peut ne pas arriver à son site d’action)
- faible métabolisme hépatique
- atteignent la lumière du tubule par filtration et sécrétion tubulaire (compétitive avec l’acide urique) une hyperuricémie peut être
induite par les diurétiques de l’anse.
- élimination urinaire (pas de métabolisme)
- effet de courte durée
Lors d’une IR, il faudra augmenter les doses pour maintenir les effets de ces diurétiques.
Chez un sujet normal, 40mg de furosémide (IV) excrétion de 200-250mmol de Na, dans 3 à 4 litres d’urines en 3 à 4 heures.
Effet natriurétique puissant et bref 6 à 8h après la prise orale, 2 à 3h après IV. Intérêt dans les situations d’urgence comme les OAP.
Autres effets :
- vasodilatation veineuse et artériolaire qui peut être intéressante dans le cadre du TTT de l’IC avec diminution du retour veineux.
- Augmentation de l’excrétion du Ca et du Magnésium (TTT des hypercalcémies aigues)
B. Présentation
Furosémide (LASILIX)
- diverses présentations : comprimés sécables 20 ou 40 mg, buvable 10mg/ml seringue graduée, retard 60mg à libération prolongée. La
dose va dépendre de la fonction rénale ; plus la fonction rénale est altérée plus il faudra augmenter les doses pour qu’il y ait une dose
suffisante qui arrive au néphron :
posologie 20 à 80 mg/jour à répartir en 2 prises
effet diurétique dès la 20e minute (action max à 30-60min après prise orale)
forme injectable (20mg IV lente ou IM : effet en 2-3 minutes) pour l’œdème aigue du poumon par exemple
- LASILIX spécial en ampoule IV 250mg, comprimé 500mg réservé à l’utilisation chez l’IR sévère voire terminale sous hémodialyse parce
que la disponibilité des sites est réduite
Autres diurétiques de l’anse :
- Bumétanide (BURINEX) : vo cp 1-5mg, IV lente ou perf 2mg/4ml 1-2mg si OAP
métabolisme hépatique
- Pirétanide (EURÉLIX LP)
Chez l’IR :
- indication du furosémide à dose élevée (250 à 1500 mg/jour, car faible quantité de diurétique arrivant au tubule)
- augmentation du débit urinaire
- IR à diurèse conservée
- Risque d’ototoxicité avec les fortes doses. Ces attaques peuvent être spontanées.
C. Les effets indésirables
D’abord en rapport avec la perde hydrosodée :
- hypovolémie
- hypotension orthostatique
- déshydratation extracellulaire

- IR fonctionnelle
Attention chez les sujets à risque.
Risque d’hypokaliémie liée à l’augmentation de la résorption du Na contre K dans le TCD (échange Na/K-H) avec alcalose métabolique.
Sur un ECG : les ondes T sont plates, onde U s’ajoute.
Risque de troubles du rythme cardiaque : torsade de pointes normalement spontanément résolutive. Elles se manifestent cliniquement par des
syncopes. Allongement de l’intervalle QT sur l’ECG. Elles peuvent être provoquées par l’hypokaliémie ou par des neuroleptiques et d’autres
médicaments.
Autres EI :
- Hyponatrémie (de déplétion, …)
- hypomagnésémie
- hyperuricémie
- élévation de la glycémie
- ototoxicité :
proportionnelle à la dose
en cas d’IR ++
association aux ATB aminosides
- réactions d’hypersensibilité : croisée avec d’autres sulfamides (thiazidiques, ATB …)
D. Les indications
- rétention hydrosodée en cas d’ICC, d’IR, de syndrome néphrotique, de cirrhose hépatique décompensée
- HTA (mécanisme mal connu dépendant de l’effet natriurétique mais qui ne l’explique pas directement. Baisse du DC puis des
résistances périphériques)
- OAP (voie IV)
- Hypercalcémie élevée
- Hyperkaliémie
E. Les interactions
- AINS risque d’IR (vasoC au niveau glomérulaire sans l’effet vasoD au niveau de l’artère efférente -> perte du contrôle du système
glomérulaire)
- Inhibition de l’excrétion du lithium (risque d’augmentation des lithiémies et toxicité)
Le lithium est un ion s’éliminant par le rein. Utilisé dans les maladies psycho-dépressives, troubles bipolaires…
- Autres médicaments hypokaliémants (corticoïdes par exemple), médicaments torsadogènes (neuroleptiques)
- Majoration du risque arrythmogène avec digitaliques + diurétique de l’anse
l’hypokaliémie favorise le risque arrythmogène des
digitaliques.
- Autres substances ototoxiques : aminosides
F. Contre-indication
- hypersensibilité aux sulfamides
- IRA fonctionnelle (hypovolémie, déshydratation)
- Obstacle sur les voies urinaires
- Déconseillé pendant la grossesse (réserver aux OAP de la femme enceinte). L’apport de sang au fœtus passe par le placenta, il sera
extrêmement dépendant de la volémie, si on diminue la volémie, le fœtus va être en hypoperfusion fœtale avec des conséquences sur
son développement.
III. Thiazidiques
A. Action
Son action se situe au niveau du tube contourné distal :
- inhibition du co-transport Na/Cl
- diminution de la réabsorption de K et Mg
- réabsorption Ca augmentée
Son effet maximal : environ 5% car 90% du Na déjà réabsorbé.

B. Présentation
- Résorption digestive rapide (biodisponibilité 60-80%)
- Présentent des métabolismes différents
- Action prolongée d’environ 12h (contrairement aux diurétiques de l’anse) dépend de la fonction rénale.
- Élimination surtout rénale (90% de la clairance totale) avec sécrétion tubulaire compétitive avec l’acide urique
- Hydrochlorothiazide (ESIDREX)
- Chlortalidone (exemple HYGROTON n’est plus utilisé que dans le cadre d’une association à un bêtabloquant)
- Indapamide (FLUDEX) 2 formes 2,5mg et LP 1,5mg
- Ciclétanine (TENSTATEN)
Ils sont indiqués dans l’HTA.
C. EI
- déplétion hydrosodée
- hypokaliémie, alcalose métabolique, hypercalcémie
- hyperglycémie
- hyperuricémie
- hyperlipidémie
- allergie
- anomalies hématologiques (très rares comme thrombopénie… )
D. Indications
- HTA (de choix parmi les diurétiques) seulement en absence d’IR et pas dans l’HTA gravidique.
- ICC pour Esidrex
- Lithiase rénale par hypercalciurie
- Pas d’effets si IR (perte d‘effet complète)
IV. Diurétiques distaux = épargneurs potassiques
A. Action
L’aldostérone stimule la réabsorption de Na et la sécrétion de K+ et H+ :
- anti-aldostérone spironolactone (ALDACTONE) chef de file
Stéroïde empêchant la migration du récepteur à
l’aldostérone (le récepteur devient donc inactif)
Antagonise les effets de l’aldostérone : épargne de
potassium
Si utilisation IV (lente) canrénoate de potassium =
SOLUDACTONE
Eplérénone (indication limitée à l’IC = INSPRA)
- effet direct sur le tube collecteur :
amiloride (MODAMIDE)
triamtérène (TÉRIAM seulement présent maintenant dans
des associations fixes)
B. Indications
- HTA essentielle
- États œdémateux avec hyperaldostéronisme secondaire (ascite cirrhotique, syndrome néphrotique)
- IC de stade III et IV avec IEC, furosémide pour spironolactone 25mg avec surveillance étroite de la kaliémie, éplérénone IC avec
dysfonction VG après infarctus
C. Effets indésirables
- Effet natriurétique peu important (risque faible d’IR fonctionnelle)
- Risque d’hyperkaliémie +++ surtout en cas d’IR, diabète, prise d’AINS, de blocage du SRA même si association à un diurétique
hypokaliémiant.
- Troubles endocriniens : gynécomastie le plus souvent réversible à l’arrêt surtout avec la spironolactone (non anti-minéralocorticoïde
spécifique mais également anti-androgène), exceptionnelle avec l’éplérénone. Impuissance, troubles des règles

D. Interaction
Interaction avec IEC et antagonistes des récepteurs de l’angiotensine (hyperkaliémie) = baisse de la libération d’aldostérone par la CS lors du
blocage du système rénine-angiotensine.
V. Inhibiteurs de l’anhydrase carbonique
- diurétiques les plus anciens
- encore utilisé : acétazolamide (DIAMOX)
- action au niveau du tube contourné proximal
- inhibent l’anhydrase carbonique (H2CO3 -> H2O + CO2)
- diminue la sécrétion de l’ion H+ et favorise le risque d’acidose
métabolique hyperchlorémique
- effets extra-rénaux :
diminution de la pression intra-oculaire (glaucome)
formation de LCR (HTIC)
VI. Diurétiques osmotiques
- administrés par voie IV
- le plus utilisé = mannitol
- éliminé par filtration glomérulaire
- le soluté non résorbable s’oppose à la réabsorption de l’eau (force osmotique)
- augmentation du volume urinaire (natriurèse non obligatoire)
- indiqué dans intoxications, œdème cérébral
VII. Indication des diurétiques en général
- IC (rétention hydrosodée qui est une conséquence du défaut hémodynamique de l’IC qui va augmenter la pression dans la circulation
veineuse, favorise la formation des oedèmes)
- OAP
- HTA
- Ascite sur foie cirrhotique
- Hypercalcémie (anse)
- Lithiase sur hypercalciurie (thiazidiques)
VIII. Surveillance du traitement
- ionogramme avant traitement : kaliémie, uricémie, créatininémie, urée
- ionogramme après le début du traitement puis régulièrement
- mesure du poids
- mesure PA
Éducation :
- prise le matin pour éviter les levers nocturnes et fuites urinaires en cas d’incontinence
- se peser régulièrement (même balance, même heure, vêtement)
- prendre la TA régulièrement (détecter hypotension, efficacité du traitement si employé comme antihypertenseur)
- se lever lentement pour diminuer le risque d’étourdissement et le risque d’hypotension orthostatique
 6
6
 7
7
 8
8
 9
9
 10
10
1
/
10
100%