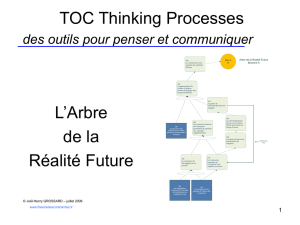
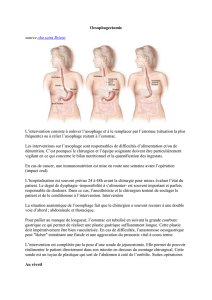
COMPLICATIONS URINAIRES APRES TRAITEMENT PAR

COMPLICATIONS URINAIRES COMPLICATIONS URINAIRES
APRES TRAITEMENT PAR APRES TRAITEMENT PAR
RADIOFREQUENCE DES RADIOFREQUENCE DES
TUMEURS DU REINSTUMEURS DU REINS
A Sadfi A Sadfi 11, JM Correas , JM Correas 11, A Khairoune , A Khairoune 11, MO Timsit , MO Timsit 22, ,
A Méjean A Méjean 22, O Hélénon , O Hélénon 11
Service de Radiologie Adultes (1) et Urologie (2) Service de Radiologie Adultes (1) et Urologie (2)
Groupe Hospitalier Necker EnfantsGroupe Hospitalier Necker Enfants--Malades, Paris, FranceMalades, Paris, France
Université Paris Descartes, Faculté de MédecineUniversité Paris Descartes, Faculté de Médecine

–– Les petites tumeurs rénales doivent bénéficier d’une Les petites tumeurs rénales doivent bénéficier d’une
prise en charge spécifique, en raison de :prise en charge spécifique, en raison de :
-- l’augmentation de leur incidence liée à l’étude des reins sur les l’augmentation de leur incidence liée à l’étude des reins sur les
examens d’imagerie pratiqués pour une autre raison examens d’imagerie pratiqués pour une autre raison
( 11% 1( 11% 1
004004
è dé d 60% f )è dé d 60% f )
INTRODUCTIONINTRODUCTION
(
+
11%
1
993
(
+
11%
1
993--2
004
, surtout
7
2
004
, surtout
7
--9
è
me
dé
ca
d
e;
60%
f
ortuite
)
9
è
me
dé
ca
d
e;
60%
f
ortuite
)
-- l’augmentation de l‘incidence de l’insuffisance rénale chez le sujet âgél’augmentation de l‘incidence de l’insuffisance rénale chez le sujet âgé
-- l’efficacité «l’efficacité « carcinologiquecarcinologique » du traitement conservateur démontrée » du traitement conservateur démontrée
par la prise en charge chirurgicale (tumorectomie….)par la prise en charge chirurgicale (tumorectomie….)
–– Parallèlement les techniques de traitement percutanées Parallèlement les techniques de traitement percutanées
««minimini--invasifsinvasifs »»se sont développées (se sont développées (ablation ablation
radiofréquence ou ARF, cryothérapie, ablation microradiofréquence ou ARF, cryothérapie, ablation micro--onde…)onde…)
Cooperberg J Urol 2008; Ahar Expert Rev Anticancer Ther 2006Cooperberg J Urol 2008; Ahar Expert Rev Anticancer Ther 2006

• Le • Le traitementtraitement de de référenceréférence restereste la la résectionrésection
chirurgicalechirurgicale ((sisi possible par possible par chirurgiechirurgie partiellepartielle))
•• Le Le problèmeproblème du du traitementtraitement des petites masses des petites masses
rénalesrénales restereste
p
osé
p
osé chez le chez le su
j
etsu
j
et â
g
éâ
g
é: :
INTRODUCTIONINTRODUCTION
pp
jj
gg
-- surveillance active avec surveillance active avec examensexamens d’imageried’imagerie répétésrépétés ouou
-- traitementtraitement conservateurconservateur (mini (mini invasifinvasif) ?) ?
=> MAIS, la => MAIS, la llongévitéongévité augmenteaugmente et, et, mêmemême en en cascas de multiples de multiples
facteursfacteurs de de comorbiditécomorbidité, la , la duréedurée de vie de vie estest non non prédictibleprédictible
=> Un => Un autreautre argument argument estest la la fréquencefréquence des des métastasesmétastases, qui, , qui,
mêmemême pour les pour les tumeurstumeurs < 4 cm de < 4 cm de diamètrediamètre, , varievarie de 2de 2--6%6%
Crispen BJU Int 2007; Pahernik J Urol2007; Abouassaly J Urol 2008Crispen BJU Int 2007; Pahernik J Urol2007; Abouassaly J Urol 2008

–– Après validation de l’indication en Après validation de l’indication en
réunion de concertation multidisciplinaire réunion de concertation multidisciplinaire
LES INDICATIONSLES INDICATIONS
–– Les iLes indications de l’ARF sont :ndications de l’ARF sont :
-- une tumeur solide < 4une tumeur solide < 4--5 cm de diamètre5 cm de diamètre
-- de localisation plutôt exode localisation plutôt exo--rénalerénale
-- les tumeurs à caractère familial (VHL…)les tumeurs à caractère familial (VHL…)
-- la présence d’un rein unique ou d’une insuffisance rénalela présence d’un rein unique ou d’une insuffisance rénale
-- la présence de contrela présence de contre--indications opératoiresindications opératoires
Il faut abolir le dogme chirurgical des 3 cm et traiter la Il faut abolir le dogme chirurgical des 3 cm et traiter la
tumeur dès qu’elle apparaît accessible à la ponctiontumeur dès qu’elle apparaît accessible à la ponction

LE PRINCIPE DE L’ARFLE PRINCIPE DE L’ARF
• L’ARF repose sur l’application d’ondes de radiofréquence • L’ARF repose sur l’application d’ondes de radiofréquence
de 300de 300--500 kHz qui vont entraîner un échauffement 500 kHz qui vont entraîner un échauffement
des tissus, qui aboutit à une nécrose de coagulationdes tissus, qui aboutit à une nécrose de coagulation
éééé
àà
• La temp
é
rature l
é
thale des cellules est atteinte au• La temp
é
rature l
é
thale des cellules est atteinte au--del
à
del
à
de 55de 55°°CC
• Il existe de multiples systèmes d’ARF différents :• Il existe de multiples systèmes d’ARF différents :
-- monopolaire, bi et multipolairemonopolaire, bi et multipolaire
-- utilisant une électrode refroidie («utilisant une électrode refroidie (« coolcool--tiptip »), »),
unique, triple (cluster), ou multiples (switch)unique, triple (cluster), ou multiples (switch)
-- ou une électrode qui déploie de multiples baleinesou une électrode qui déploie de multiples baleines
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
1
/
37
100%