Les Enterobacteries (word)

UE8-De l’agent infectieux à l’hôte
Date : 26-02-16 Plage horaire : 14H-16H
Promo : P2 Enseignant : G. Miltgen
Ronéistes :
PERRAULT Geoffroy
GRONDIN-HOAREAU Jean-Christophe
Les Entérobactéries
I.
Les Entérobactéries
1.
Introduction
2.
Identification et caractères bactériologiques
3.
Classification
4.
Habitat
A- Chez l’homme
B- Dans l’environnement
5.
Pouvoir pathogène
6.
Diagnostic
7.
Sensibilité aux antibiotiques
II-
Différents groupes d’entérobactéries
1.
E.Coli
2.
Salmonella sp
A- Caractéristiques
1
Formes digestives
2
Formes septicémiques
3.
Formes extra digestives
B- Diagnostic
1.
Diagnostic direct
2.
Diagnostic indirect
C- Traitement
D- Prévention
3.
Shigella sp.
4.
KES =Klebsiella sp. - Enterobacter sp. – Serratia sp. (autres
entérobactéries)
5.
Proteus sp/ Providencia sp/ Morganella sp
6.
Yersinia sp.
Conclusion
Note: Il ne va pas nous piéger sur les petits détails. Retenir les grandes idées.

I.
Les Entérobactéries
1.
Introduction
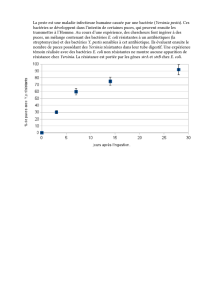
Les entérobactéries sont des bactéries commensales ou pathologiques du tube digestif de l’homme et des
animaux, d’où leur nom (entéro= intestin grêle).
Elles sont très fréquentes en pathologie humaine :
Elles représentent 2/3 à ¾ des bactéries identifiées dans un labo de bactériologies.
Certaines sont des pathogènes obligatoires (ex : shigelles) : Dès leur entrée dans le tube digestif elles
provoquent des maladies.
D’autres présentent un caractère opportuniste. Elles ne sont pathogènes qu’en quantité très
importante sur fond d’immunodépression.
D’autres groupes prolifèrent dans l’environnement et peuvent être une source de contamination notamment
le groupe des serratia.
Ce sont des bactéries GRAM-. Les entérobactéries sont situées au premier rang dans l’infection des
bactéries GRAM-, à la fois en communautaire et à l’hôpital. Il a y a environ 10^12 bactéries par gramme de
selles.
La plupart sont des bactéries anaérobies et parmi les anaérobies, les entérobactéries représentent 10^3
bactéries par gramme de selles. Il y a différentes espèces et toutes n’ont pas la même virulence et les mêmes
applications en termes de pathologies.
Schéma (absent de la ronéo) : sur la gauche on a les pathogènes primaires (fréquent strict) notamment les
Salmonella, les Shigella, les Yersinia (qui sont des entéropathogenes qui donnent de grandes
symptomatologies digestives (diarrhées..). Parfois ils peuvent diffuser de manière exceptionnelle en dehors
du tube digestif et donner des septicémies.
Sur la droite on a les pathogènes opportunistes, les Providencia, les Morganella, les Enterobacter, les
Serratia, que l’on retrouve essentiellement à l’hôpital, souvent sur un terrain fragilisé.
On a des bactéries un peu à la frontière des deux : Escherichia coli, Klebsiella pneumonia, Proteus. Ce sont
des bactéries avec des facteurs de virulence certain, que l’on retrouve très fréquemment en infections,
notamment en communautaire pour E. coli.
2.
Identification et caractères bactériologiques.
La famille des entérobactéries possèdent 7 caractéristiques communes:
Bacille gram négatif (couleur rose)
Mobile (ciliature péritriche) ou immobile
Non exigeants (poussent sur milieux usuels)
Croissance en aéro-anaérobie facultatifs (poussent à la fois avec et sans O2).
Fermentent le glucose
Nitrate oxydase : transformation possible des nitrites en nitrates
Oxydase négative

Entérobactéries en forme de bâtonnets, GRAM négatif donnant cet aspect rosé. Souvent on a une
coloration bipolaire, c.à.d. que l’on a des bacilles un peu plus colorées aux extrémités et clair au milieu.
Cela permet parfois sur un examen direct de nous orienter vers la famille des entérobactéries.
Comment identifie-t-on une entérobactérie (EB) au labo ?
Examen Direct : Réalisé avec la coloration de GRAM ou l’état frais (on met juste un prélèvement liquide
sur une lamelle et on l’observe).
Paramètres observables pour l’entérobactérie : Bacille GRAM-, bipolaire, mobile
Petite parenthèse sur ce qui se passe concrètement dans un labo de bactério :
On a 3 phases :
-
Jour 0 : arrivé du prélèvement
-
Jour 1 : 1er jour de culture
-
Jour 2 : on réalise un antibiogramme si nécessaire.
Comme tout cela dure 48h on a en clinique 2 traitements :
-
Le traitement probabiliste : on connait plus ou moins la bactérie impliquée dans la pathologie mais
on ignore sa sensibilité aux antibiotiques
-
Le traitement ciblé : on a eu un antibiogramme ce qui permet de traiter le patient avec l’antibiotique
auquel la bactérie est sensible.
Caractères culturaux :
Aspect de colonies grasses: lisses, bombées et brillantes
Croissance rapide
Type de milieux : milieux ordinaires et enrichis
Atmosphère : O2 et sans O2.
A gauche : Culture sur gélose au sang.
A droite : Culture en fonction des caractères
biochimiques des bactéries ce qui permet de les
colorer. Milieux dits chromogènes.

Caractères biochimiques :
Grande diversité enzymatique et de fermentation des sucres (galerie d’identification, géloses chromogènes)
Aujourd’hui remplacé par la spectrométrie de masse (MALDI-TOF).
Caractères antigéniques :
des antigènes O pour la paroi
Toujours présents, thermostables, très toxiques (responsables de la toxicité, endotoxine)… choc
septique (fièvre, CIVD, bradycardie, hypotension…)
Permet de classer les EB d’une même espèce en sérotype ou sérovar (agglutination)
Mosaïque d’Ag, certains communs et certains spécifiques de chaque espèce, fréquemment
utilisés pour la détermination des sérotypes ou sérovars, parfois diagnostic indirect (ex : sérologie
Widal et Félix)
antigènes H pour les flagelles
Thermolabiles
Intérêt dans l’identification de certaines espèces comme la salmonella
des antigènes K pour les capsules ou l’enveloppe (ex Vi pour salmonella)
3.
Classification

Il y a 4 grands groupes :
-
les Escherichiae : Les plus fréquentes sont E.Coli, Shigella, Salmonella qui ont beaucoup de
matériel génétique en commun notamment E.Coli et Shigella ce qui fait qu’en MALDI-TOF on a
beaucoup de mal à les séparer.
-
les Klebsiellae : les plus fréquents sont Klebsiella, Entérobacter et Serratia (groupe KES). Groupe
n’ayant pas de tropisme particulier.
-
les Protae : proteus, providencia, morganella
-
les Yersiniae : yersinia qui donne la peste.
Paragraphe en bleu à connaitre absolument !
4.
Habitat
A- Chez l’homme :
Les entérobactéries sont en grande majorité commensales du tube digestif. D’autres sont retrouvés en
majorité dans le milieu extérieur (ex de Serratia).
B- Dans l’environnement :
Leur localisation habituelle sert à tester la potabilité de l’eau et la qualité des produits alimentaires en faisant
des tests de contamination fécale.
Si on trouve des bactéries coliformes dans les eaux on sait qu’elles ont été souillées par des excréments.
5.
Pouvoir pathogène
2 types de pathogènes :
Les pathogènes opportunistes
-
Bactéries présentes au niveau intestinal mais qui peuvent, à des degrés variables, devenir agressives
pour l’homme. Si elles sont présentes en quantité trop importante ou si on est immunodéprimé, elles
deviennent pathogènes.
-
Phénomène renforcé par l’acquisition des résistances (dysmicrobisme)
-
Responsables d’infections diverses :
Digestives : gastroentérites, adénite mésentérite, abcès profonds…
Urinaires : cystites, pyélonéphrites,
Septicémies à point de départ urinaire
Autres : pneumopathie (klebsiella pneumoniae), méningite néonatale (E.Coli, citrobacter koseri),
suppurations diverses.
Les Pathogènes spécifiques :
-
Bactéries non présentes au niveau intestinal qui dès qu’elles sont retrouvées dans l’organisme sont
responsables d’infections plus ou moins graves.
Schéma résumant la classification selon
le pouvoir pathogène :
-
A gauche les bactéries représentant les
pathogènes spécifiques : Shigella
(pathogène à partir de 100 bactéries),
salmonella, yersinia.
-
Au milieu, les bactéries qui peuvent
être à la fois commensales et
pathogènes si elles sont présentes en
trop grande quantité (E.Coli et
klebsiella pneumoniae).
-
A droite, les pathogènes opportunistes.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
1
/
20
100%