Étude de phase III randomisée, réalisée en ouvert, comparant l

1
Étude de
phase
III
randomisée, réalisée
en
ouvert,
comparant
l’irinotécan
avec le
paclitaxel
chez des
patients porteurs d’un
cancer
de
l’estomac avancé
sans
métastase péritonéale sévère
après échec
d’une polychimiothérapie antérieure
à base
de
fluoropyrimidine
et d’un sel de
platine
: essai
WJOG
4007
INTR
ODUCTION
Le
devenir
des
patients présentant un cancer
de l’estomac
non résécable
est
extrêmement mau-
vais ;
une survie
médiane
de 3 à 5
mois
a
é
t
é
rapportée
avec les
meilleurs
soins palliatifs
(M
S
P
)
uniquement
1-3
. Dans
les
études
randomisées
réali
- sées
dans
les
années 1990, une
chimiothérapie
d
e
première ligne pour
le
cancer
de
l’estomac
à
un
stade avancé apportait un bénéfice
en
matière de
survie,
comparé aux
MSP
uniquement.
À
l
’
h
e
u
r
e
actuelle
et
dans
le
monde entier, après avoir
réa
- lisé de
nombreux
essais
cliniques,
il
est
c
o
n
s
i
d
é
r
é
que l’association
chimiothérapeutique
à base
de fluoropyrimidine plus
sel de
platine,
avec ou
sans
épirubicine
ou
docétaxel,
est la
chimiothérapie
de
première ligne standard pour
le
traitement
du
cancer
de
l’estomac
4-9
.

2
Depuis que
le S-1 a
été approuvé au
J
a
p
o
n
pour
le
t
r
a
i
t
e
m
e
nt
du cancer
de
l’estomac
à
un stade avancé, plusieurs études de
phase
III
ont
été
menées, notamment l’étude
JCOG
9912
(
Japan
Clinical Oncology Group
9912
;
fluorouracil
versus S-1 versus
irino
-
técan plus cisplatine)10, l’étude
SPIRITS (S-1
plus cisplatine
versus
S-1
dans
le
cadre
d
’
u
n
essai
contrôlé randomisé dans
le
t
r
a
i
t
e
m
e
nt
du
cancer
de
l’estomac
; S-1 versus S-1
plus cisplatine)
9
,
et les
essais
GC0301/TOP-002
(Gastric Cancer
0301/Topotecin-002
; S-1
versus
S-1
plus irinotécan)
11
.
Sur
la base des
résultats
de ces
études,
il
e
s
t
maintenant accepté
au
Japon que
le S-1
plus cisplatine constitue
la
chimiothérapie
de
première ligne standard pour
le
cancer
de
l’es
-
tomac
à
un stade avancé.
Bien qu’il n’y ait pas de
preuves
robustes
d’un bénéfice
en
matière
de
survie,
> 70 % des
participants ont
reçu
une chimiothérapie
de
seconde ligne dans
ces
études
9-11
.
De
nombreuses études
de
phase
II avec
chimiothérapie
d
e
seconde ligne pour
le
cancer
de
l
’
e
s
t
o
m
a
c
à
un stade avancé o
nt
été
réalisées
12-20
. Dans
les
évaluations
des
taxanes, l’administration
tout
à la fois de
paclitaxel
(210
mg/m
2
)
et de
docétaxel
(60
mg/
m2)
selon un schéma trihebdomadaire
a
donné suite
à des
t
a
u
x
élevés
de
neutropénie
de
grade
3 ou 4 (37 % à 88
%)
12-14
, alors
que
des
taux
de
neutropénie sévère plus faibles
(3 % à 32 %)
o
nt
été observés
lors de
l
’
a
dm
i
n
i
s
t
r
a
t
i
o
n
hebdomadaire
de
p
a
cli
t
ax
el
(80
mg/m
2
)
15-18
. En
ce
qui concerne
les
paramètres
de
l
’
e
ffi
c
a
ci
t
é
,
le
taux
de
réponse
(TR)
et
la
survie sans progression
(SSP)
é
t
a
ie
nt
similaires chez
les
patients recevant
le
paclitaxel selon un schéma
d’administration hebdomadaire
et
chez ceux
le
recevant selon
un
schéma trihebdomadaire. Deux rapports ont évalué
le
p
a
cli
t
ax
el
hebdomadaire
à
titre
de
chimiothérapie
de
seconde ligne,
et ils
ont
indiqué que
la
survie globale
(SG)
médiane était
de 5
et
6,9
m
o
i
s
,
respectivement
15,16
. Dans
d
’
a
u
t
r
e
s
études, une
p
o
lyc
h
i
m
i
o
th
é
r
a
p
ie
incluant l’administration bihebdomadaire d’irinotécan
(150
mg/m
2
)
en
tant que chimiothérapie
de
seconde ligne
a
entraîné une
SG
médiane
de 8 à 10
mois
19,20
, bien que
la
toxicité ait paru plus
s
évè
r
e
que
celle
observée
avec le
paclitaxel hebdomadaire.
C
’
e
s
t
a
i
n
s
i
que
le
paclitaxel hebdomadaire est devenu
la
chimiothérapie
d
e
seconde ligne préférable
au
Japon.
A
c
t
u
elle
m
e
nt
,
les
taxanes et
l
’
i
r
i
n
o
t
éc
a
n
constituent
les
d
e
u
x
principales options thérapeutiques pour
le
cancer
de
l’estomac à
un stade avancé réfractaire
à
l’association fluoropyrimidine
plus
sel de
platine.
Ceci
dit,
à
notre connaissance, aucune étude
ran
-
domisée
n
’
a
encore directement comparé
l
’
e
ffi
c
a
ci
t
é
de ces
d
e
u
x
traitements.
Le
West
Japan Oncology Group
(WJOG)
a
mené un
essai de
phase
III
(
W
J
O
G
4007) qui avait pour but
de
comparer
le
paclitaxel et
l
’
i
ro
n
o
t
éc
a
n
chez
des
patients atteints d
’
u
n
cancer
d
e
l’estomac
à
un stade
avancé.
P
A
TIENT
S
ET
MÉTHODES
Patients
Les
patients admissibles
à
l
’
é
t
u
d
e
avaient entre
20
et
75
ans
e
t
ils
présentaient un adénocarcinome métastatique ou récidivant d
e
l’estomac confirmé
par
histologie.
Les
autres critères
d’inclusion
étaient
:
un indice
de
performance
de l’Eastern Cooperative
Onco
-
logy Group (IP
ECOG) compris entre
0 et 2 ;
une progression
de
la
maladie confirmée
par
scanner
(CT), par
endoscopie ou
par
u
n
e
autre technique d’imagerie quelconque durant
ou
dans
le
mois
suivant
la
dernière dose
de
chimiothérapie
de
première ligne par
fluoropyrimidine plus
sel de
platine
;
aucune chimiothérapie
anté
-
rieure
par
taxanes
ou
irinotécan
; et
l’absence
de
métastases
péri
-
tonéales sévères.
On
entendait
par
métastases péritonéales
sévères
des
métastases définies comme un iléus ou un sous-iléus
év
o
q
u
é
lors
d
’
u
n
examen baryté, et
la
présence
d
’
a
s
ci
t
e
modérée
à
s
évè
r
e
allant au-delà
de la
cavité pelvienne sur un scanner
(CT)
du
r
a
c
h
i
s
,
causée
par des
métastases péritonéales.
En cas de
traitement
par
chimiothérapie adjuvante
ou
néo-adjuvante
à base de
fluoropyri
-
Randomisation
(N = 223)
Randomisés au groupe sous paclitaxel hebdo (n = 111) Randomisés au groupe sous irinotécan hebdo (n = 112)
Ont reçu l’intervention attribuée (n = 108)
N’ont pas reçu l’intervention attribuée (n = 3)
Maladie évolutive
(n = 2)
Non admissibles
(n = 1)
Ont reçu l’intervention attribuée (n = 110)
N’ont pas reçu l’intervention attribuée (n = 2)
Maladie évolutive
(n = 1)
Non admissibles
(n = 1)
Intervention interrompue (n = 108)
Progression de la maladie (n = 93)
Effet indésirable (n = 6)
Retrait (n = 5)
Décès (n = 1)
Autre (n = 1)
Perdus de vue au suivi (n = 2)
Ensemble d’analyses complet (n = 108)
Exclus des patients randomisés (n = 3)
Non admissibles
(n = 3)
Ensemble d’analyses de l’innocuité (n = 108)
N’ont pas reçu l’intervention attribuée (n = 3)
Intervention interrompue (n = 110)
Progression de la maladie (n = 96)
Effet indésirable (n = 10)
Retrait (n = 2)
Décès (n = 1)
Autre (n = 1)
Ensemble d’analyses complet (n = 111)
Exclus des patients randomisés
(n = 1)
Non admissibles (n = 1)
Ensemble d’analyses de l’innocuité (n = 110)
N’ont pas reçu l’intervention attribuée (n = 2)
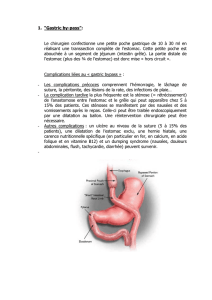
Fig. 1.
Diagramme
CONSORT

3
Tableau 1.
Caractéristiques démographiques et cliniques initiales des patients
Paclitaxel
hebdomadaire
Irinotecan
(n 108) (n
111)
Caractéristique Nbre % Nbre
%
Sexe
Homme 84 77.7 87 78.4
Femme 24 22.2 24 21.6
Age, ans
Médiane 64.5 65
Valeurs
extrêmes 37-75 38-75
IP ECOG
0 à 1 104 96.3 107 96.4
2 4 3.7 4 3.6
Gastrectomie antérieure
Oui 37 34.3 39 35.1
Non 71 65.7 72 64.9
Chimiothérapie antérieure
S-1 plus cisplatine 92 85.2 102 91.9
Capécitabine plus cisplatine 13 12.4 8 7.2
S-1 plus oxaliplatine 3 2.8 1 0.9
Lésion cible
Oui 91 84.3 88 79.3
Non 17 15.7 23 20.7
Histologie
Intestinal 54 50.0 54 48.6
Diffuse 54 50.0 57 51.4
Métastases péritonéales
Oui 28 25.9 28 25.2
Non 80 74.1 83 74.8
Nbre de sites métastasiques
Un 57 52.8 64 57.7
Deux ou plus 51 47.2 47 42.3
Abréviation : IP
ECOG,
indice de performance du Cooperative Oncology
Group.
Survie globale
(
%
)
Survie sans progression
(
%
)
midine plus
sel de
platine,
les
patients présentant une
progression
de la
maladie en cours
de
traitement ou dans
les 6
mois
s
u
iv
a
nt
l’achèvement
du
traitement étaient admissibles
à
l’étude.
De
plus,
il
était nécessaire que leurs fonctions médullaire, hépatique et
r
é
n
a
le
soient adéquates.
Conception de l’étude
W
J
O
G
4007 était un
essai
clinique
de
phase
III
p
ro
s
p
ec
t
i
f
,
multicentrique, randomisé ouvert et
avec
groupes parallèles
q
u
i
s
’
e
s
t
déroulé dans
37
centres au
J
a
p
o
n
.
Le
protocole
a
été
a
pp
ro
u
vé
par le
comité d’éthique indépendant
ou le
comité d’éthique médi
-
cale de
chaque établissement participant
à l’essai.
Cet
essai a
é
t
é
mené conformément
à la
Déclaration d’Helsinki.
Tous les
patients
ont donné
leur
consentement éclairé
par
écrit avant d’être admis
à
l’étude.
L’essai
était enregistré dans
l’University
Hospital
Medical
Information Network (Réseau
d’informations médicales
des
hôpitaux
universitaires).
Après
vérification
de
leur admissibilité
à l’essai, les
patients
o
nt
été
randomisés
en
nombres égaux entre
le
groupe recevant
le
pacli
-
taxel et celui recevant
l
’
i
r
i
n
o
t
éc
a
n
.
La
randomisation était r
é
a
li
s
ée
centralement au centre
des
données au moyen
d
’
u
n
e
méthode d
e
minimisation
qui
utilisait
les
facteurs d’ajustement suivants
:
éta
-
blissement,
IP ECOG (0 à 1 versus 2)
et lésions mesurables
(
p
r
é
s
e
n
ce
versus absence).
Le
traitement attribué était connu
des
investiga
-
teurs tout comme
des
patients.
Traitement
Le
paclitaxel
(80
mg/m
2
) était administré
par voie
intravei
-
neuse aux jours
1, 8
et
15,
toutes
les 4
semaines. Une
d
e
m
i
-
h
e
u
r
e
avant l’administration
du
paclitaxel,
les
patients recevaient
des
inhibiteurs
des
récepteurs
1 et 2 de
l’histamine
et de la
dexamé
-
thasone
à
titre
de
prévention
de
réactions allergiques.
L
’irinotécan
(150
mg/m
2
) était administré
par voie
intraveineuse aux jours
1
e
t
15,
toutes
les 4
semaines.
Il
était permis
de
réduire
la
dose
et/ou
de
retarder
les
cycles
d
’
a
p
r
è
s
des
critères
de
toxicité prédéfinis.
L
e
traitement
se
poursuivait jusqu’à une progression
de la
maladie,
la
survenue
d
’
u
n
e
toxicité grave inacceptable ou
le
refus du patient
d
e
continuer
à
être traité.
A
u
c
u
n
e
spécification
n
’
é
t
a
i
t
donnée q
u
a
nt
à
une chimiothérapie
ultérieure.
Évaluations
Les
signes vitaux, l’indice
de
performance
ECOG
et
les
anal
yses
de
laboratoire étaient évalués
au
cours
des 7
jours précédant
l’ad
-
mission
à
l’étude.
Des
examens physiques
et des
analyses
hémato
-
logiques
et
biochimiques étaient effectués durant
l’administration
du médicament tout au long du traitement.
Les
tumeurs
é
t
a
ie
nt
évaluées
par
scanner
(CT) du
thorax,
de
l’abdomen
et du
bassin
au
cours
des 28
jours précédant l’admission
à
l’étude puis tous
les
2
mois après
la
randomisation
j
u
s
q
u
’
à
l
’
i
nt
e
rr
u
p
t
i
o
n
du
t
r
a
i
t
e
m
e
nt
A 100
80
60
40
20
Paclitaxel hebdomadair
e
Irinotécan
Log-rank P = 0.38
0
Nbre à
risque
6 12 18 24 30 36
Temps (mois)
Paclitaxel hebdo 108 80 36 10 2 0 0
Irinotécan 111 75 29 10 3 1 1
B
100
80
60
40
20
Paclitaxel hebdomadair
e
Irinotécan
Log-rank P = 0.33
0
Nbre à
risque
3 6 9 12 15 18 21 24
Temps (mois)
Paclitaxel hebdo 108 66 16 9 3 2 2 0 0
Irinotécan 111 46 18 8 6 2 1 0 0
Fig. 2.
Courbes
de
Kaplan-Meier
de la
survie
globale (A) et de la
survie sans
pro-
gression
(B)

4
selon
le
protocole.
Les
critères
RECIST
(version
1.0)
ont
servi
à
évaluer
les
réponses
au
traitement
21
.
Les
évaluations
de
l
’
i
nn
o
c
u
i
t
é
étaient renouvelées toutes
les 2
semaines jusqu’à l’instauration
d’une chimiothérapie ultérieure
ou 6
semaines après
le
dernier
traitement administré selon
le
protocole.
Le
degré
de
sévérité des
effets indésirables était déterminé selon
les
National
Cancer
Ins
-
titute
Common Terminology
Criteria for Adverse Events
(Critères
d
e
terminologie courants pour effets indésirables
du
National
Ca
n
ce
r
Institute) (version
3.0). Le
Comité
de
surveillance
de
l
’
i
nn
o
c
u
i
t
é
et des
données
de l’essai
WJOG était chargé d’examiner
les
effets
indésirables graves pour juger
de
l
’
i
nn
o
c
u
i
t
é
de l’essai
durant
le
traitement administré dans
le
cadre
du
protocole.
Les
investiga
-
teurs ont évalué
la
réponse,
la
progression
et les
toxicités chez leurs
patients
; des
évaluations centrales indépendantes
de la
réponse
e
t
de la
progression
de la
maladie n’ont
pas été
effectuées.
Analyse
statistique
Le
critère
d
’
év
a
l
u
a
t
i
o
n
primaire était
la SG,
définie
c
o
mm
e
le
délai écoulé entre
la
randomisation
et le
décès, toutes causes
confondues.
Les
critères
d
’
év
a
l
u
a
t
i
o
n
secondaires étaient
la SSP,
définie comme
le
délai écoulé entre
la
randomisation
et la
progres
-
sion
de la
maladie ou
le
décès, toutes causes confondues
; le TR
;
la
toxicité
; et le
pourcentage
de
patients ayant reçu une chimio
-
thérapie ultérieure.
Les
études
à
un
seul bras
antérieures ont
mis en
évidence
une
SG
médiane
de 5 et de 6,9
mois dans
le
schéma
thérapeuti
-
que
à base de
paclitaxel
15,16
et
de 8
et
10
mois dans celui
à
b
a
s
e
d’irinotécan
19,20
.
L
’irinotécan
était contre-indiqué chez
les
patients
présentant
de
sévères métastases péritonéales parce que
ses
métabo
-
lites sécrétés
par voie
biliaire avaient provoqué
de
sévères
t
o
x
ici
t
é
s
.
Dans
le
cancer
de
l
’
e
s
t
o
m
a
c
,
des
métastases péritonéales
s
’
é
t
a
ie
nt
souvent développées au fur et
à
mesure
de
l
’
év
o
l
u
t
i
o
n
de la
m
a
l
a
d
ie
et
nous avons,
de ce fait,
supposé
qu’il
serait plus difficile d’admi
-
nistrer l’irinotécan après
le
paclitaxel chez
les
patients, comparé à
la
séquence
de
traitement inverse. D’après
ces
résultats antérieurs
et nos suppositions, cette étude
a
été conçue
avec la
p
u
i
ss
a
n
ce
adéquate pour détecter une amélioration
de 50 % au
niveau
de
la
SG
médiane,
soit
pouvant
aller de 5
mois dans
le
groupe
sous
pacli
-
taxel
j
u
s
q
u
’
à
7,5
mois dans celui sous irinotécan (hazard ratio
[
H
R
]
,
0,67).
En
présumant
des
périodes
de
recrutement
et de
suivi
de
36
et de 12
mois, respectivement,
et en
utilisant un
test du
log-rank
bilatéral
avec des
erreurs
α
de 5 %
et
α
de 20 %, 220
patients
é
t
a
ie
nt
requis pour l’étude. Aucune analyse intermédiaire n’était prévue.
Un ensemble
d
’
a
n
a
ly
s
e
s
complet (Full analysis set,
FAS)
incluait tous
les
patients randomisés
qui
répondaient
aux
cri
-
tères d’admission
à
l’étude
(les
patients s’avérant non admissi-
bles à
l’étude après
la
randomisation étaient exclus).
L
’ensemble
d’analyses
de
l’innocuité (Safety Analysis
Set, SAS)
incluait tous
les
patients randomisés ayant reçu
≥
une dose
du
médicament
à
l’étude.
La SG et la SSP
étaient analysées dans
le
cadre
du FAS
et
estimées
en
utilisant
la
méthode
de
Kaplan-Meier.
Le
taux de
réponse
(TR)
était évalué chez
les
patients présentant
≥
une lésion
mesurable
à
l’admission
à
l’étude.
La
toxicité était analysée dans
le
cadre
du SAS.
Patients Hazard ratio IC à
95%
Tous 219 1,13 0.86 à
1.49
Age, années
< 65 109 1,36 0.92 à
2.01
≥ 65 110 0,97 0.65 à
1.44
Sexe
Masculin 171 1,08 0.79 à
1.48
Féminin 48 1,38 0.76 à
2.49
IP ECOG
0-1 211 1,12 0,85 à
1,49
2 8 7,27 0,79 à
66,6
Gastrectomie
Oui 60 1,05 0,61 à
1,80
Non 159 1,24 0,90 à
1,71
Histologie
Intestinal 108 1,15 0,77 à
1,71
Diffuse 110 1,11 0,75 à
1,63
Lésions
mesurables
Présence 183 1,19 0,88 à
1,61
Absence 36 0,91 0,46 à
1,81
Métastases
péritonéales
Oui 56 1,31 0,76 à
2,28
Non 163 1,07 0,77 à
1,48
Nbre de sites
métastatiques
0-1 121 0,91 0,62 à
1,33
≥ 2 98 1,64 1,08 à
2,49
0,1 1
10
Favorise
l’irinotécan
Favorise le paclitaxel
hebdomadair
e
Fig. 3.
Graphique
en forêt des
analyses
de
sous-groupes. IP ECOG,
indice de performance
de
l’
Eas
t
er
n
Cooperative Oncology
Group

5
Tableau 2.
Effets
indésirables
Paclitaxel
hebdomadaire Irinotécan
(n 108) (n 110)
Grade 3 Grade 3
Tout grade à 4 Tout grade à 4
Effet indésirable Nbre % Nbre % Nbre % Nbre
%
Leucopénie 88 81.4 22 20.4 76 69.4 21 19.1
Neutropénie 85 78.7 31 28.7 77 70.0 43 39.1
Hémoglobine 69 63.9 23 21.3 84 76.4 33 30.0
Thrombopénie 6 5.6 1 0.9 15 13.6 2 1.8
Neutropénie fébrile 3 2.8 3 2.8 10 9.1 10 9.1
Nausées 33 30.6 2 1.9 61 55.5 5 4.5
Vomissements 22 20.4 3 2.8 40 36.4 1 0.9
Anorexie 50 46.3 8 7.4 78 70.1 19 17.3
Diarrhée 21 19.4 1 0.9 49 44.5 5 4.5
Neuropathie (sensible) 62 57.4 8 7.4 2 1.8 0 0
Bilirubine 10 9.3 3 2.8 21 19.1 4 3.6
AST 32 29.6 4 3.7 42 38.2 9 8.2
ALT 24 22.2 3 2.8 41 37.3 3 2.7
Hyponatrémie 21 19.4 4 3.7 35 31.8 17 15.5
Décès
associé au
traitement 0 0 0 0 2 1.8 2 1.8
Il
était prévu
de
réaliser l’analyse primaire
1
an après
le
recru-
tement
du
dernier patient
ou
après
la
survenue
de 205
événe-
ments approximativement, selon
ce qui se
produirait
en
premier
.
Un
statisticien indépendant
et
un centre d’analyse
de
données
se
sont chargés
de
l’analyse primaire pour
la SG avec
un
test
du
log-rank non stratifié dans
la
population prise
en
compte pour le
FAS.
L’aveugle
était maintenu quant
aux
données pour tous les
investigateurs jusqu’à
la fin de
l’analyse.
Des
modèles
des
risques
proportionnels
de Cox
ont
servi à
calculer
les HR et les IC. Le
test
exact
de
Fisher
a été
utilisé pour évaluer
les
différences
au
niveau
du TR, de
l’incidence
des
effets indésirables
et du
pourcentage de
patients ayant reçu une chimiothérapie
de
troisième ligne. Les
analyses
de
sous-groupes exploratoires
de la SG
ont
été
effectuées
en
utilisant
des
variables
de
stratification
et
pronostiques.
RÉSUL
T
A
T
S
Patients
Entre août 2007
et
août 2010,
223
patients provenant
de
37
centres
au
Japon ont
été
admis
à
l’étude.
Sur ces 223
patients, 111
ont
été
placés dans
le
groupe traité
par le
paclitaxel
et 112
dans
celui traité
par
l
’
i
r
i
n
o
t
éc
a
n
(fig. 1).
Quatre patients, qui
a
v
a
ie
nt
reçu une monothérapie antérieure
par la
fluoropyrimidine
(groupe
sous paclitaxel, n
= 2 ;
groupe sous irinotécan, n
= 1)
ou qui
présentaient une progression
de la
maladie non confirmée
p
ar
radiographie (groupe
sous
paclitaxel, n
= 1)
n’ont
pas
répondu
aux
critères d’inclusion
à
l’étude. Ainsi,
le FAS
prenait
en
compte 108
patients
du
groupe
sous
paclitaxel
et 111
patients
du
groupe sous
irinotécan.
Après la
randomisation, trois patients
du
groupe sous
paclitaxel
et
deux
du
groupe
sous
irinotécan n’ont
pas
reçu
le
trai
-
tement décrit dans
le
protocole.
De ce fait, le SAS
portait
sur
108
patients
du
groupe
sous
paclitaxel
et 110
patients
du
groupe sous
irinotécan. Dans
le FAS, les
caractéristiques initiales
des
patients
étaient bien équilibrées entre
les
deux groupes
de
t
r
a
i
t
e
m
e
nt
(tableau
1). Des
scores
de l’IP ECOG de 0 ou 1
ont
été
obtenus
chez une majorité
de
patients.
La
chimiothérapie
de
première ligne
la
plus fréquente était
à base de S-1
plus cisplatine (88,6
%),
s
u
ivie
de la
chimiothérapie
par
capécitabine plus cisplatine
avec ou
sans
récepteur
du
facteur
de
croissance anti-épidermique
ou
anticorps
dirigés contre
le
facteur
de
croissance endothélial
a
nt
i
-
v
a
s
c
u
l
a
i
r
e
(9,6 %) et de S-1
plus oxaliplatine
(1,8 %).
Une
ou
plusieurs lésions
mesurables étaient présentes chez approximativement
80 %
des
patients,
et des
métastases péritonéales légères
ou
modérées ont été
détectées dans
les
deux groupes chez quelque
25 % des
patients.
Deux
ou
plusieurs
sites
métastatiques ont
été
trouvés chez
< 50
%
des
patients.
Exposition
à la chimiothérapie
Le
nombre médian d’administrations atteignait 11,5
(valeurs
extrêmes
: 1 à 46)
dans
le
groupe
sous
paclitaxel
et 4,5
(valeurs
extrêmes
: 1 à 39)
dans celui
sous
irinotécan.
Les
raisons pour
les
-
quelles
le
traitement
a été
interrompu incluaient une
progression
de la
maladie (86,7
%), des
effets indésirables
(7,3 %), le
retrait
du
consentement
(3,2 %)
et d
’
a
u
t
r
e
s
raisons
(2,8 %). Le
p
o
u
r
ce
nt
a
g
e
de
patients chez
qui le
traitement
a dû être
interrompu
en
raison
d
’
u
n
e
toxicité était
de 5,6 %
dans
le
groupe sous paclitaxel et
d
e
9,1 %
dans celui sous
i
r
i
n
o
t
éc
a
n
.
Une chimiothérapie
de
troisième ligne
a été
administrée à
97
patients (89,8
%) du
groupe
sous
paclitaxel
et à 80
patients
(72,1
%) du
groupe
sous
irinotécan
(P =
0,001). Dans
le
groupe
sous
paclitaxel, une chimiothérapie
de
troisième ligne
à base
d’irino
-
técan
a
été utilisée chez
81
patients (75,0
%)
et, dans
le
g
ro
u
p
e
sous
irinotécan, un schéma
à base de
taxanes
a été
utilisé chez
67
patients (60,4
%).
Lignes tardives incluses,
87
patients (80,6
%
)
du
groupe
sous
paclitaxel ont reçu
de
l’irinotécan,
et 75
patients
(67,6
%) du
groupe
sous
irinotécan ont reçu
du
paclitaxel.
Efficacité
En
août 2011, après une période
de
suivi médiane
de
17,6
mois,
203
décès (92,7
%)
ont été rapportés dans
la
cohorte
d
e
patients.
En ce qui
concerne
la SG, qui
constituait
le
critère
d’éva
-
luation primaire, aucune différence statistiquement
s
i
g
n
i
fi
c
a
t
ive
n’a été
observée entre
les
groupes
sous
paclitaxel
et sous
irinoté
-
can
(HR,
1,13
; IC à 95 %,
0,86
à
1,49
; P
bilatéral
=
0,38).
La
SG
médiane était
de 9,5
mois
(IC à 95 %, 8,4 à
10,7) dans
le
g
ro
u
p
e
sous paclitaxel et
de 8,4
mois
(IC à 95 %, 7,6 à 9,8)
dans
le
g
ro
u
p
e
sous
irinotécan
(fig. 2A). La SSP
médiane était
de 3,6
mois
(IC
à
95 %, 3,3 à 3,8)
dans
le
groupe
sous
paclitaxel
et de 2,3
mois
(IC
à 95 %, 2,2 à 3,1)
dans
le
groupe sous irinotécan. Cette
d
i
ff
é
r
e
n
ce
n’était
pas
statistiquement
significative
(HR,
1,14
; IC à 95 %,
0,88
à
1,49
; P
bilatéral
=
0,33
; fig. 2B). Le
taux
de
réponse
(TR)
é
t
a
i
t
de
20,9
% (19 des 91
patients) dans
le
groupe sous paclitaxel et
d
e
13,6
% (12 des 88
patients) dans
le
groupe sous irinotécan
(
t
e
s
t
exact
de
Fisher
P =
0,24).
Les
résultats
de
l’analyse
de
sous-groupes portant
sur la
SG
sont illustrés
par la
figure
3. Bien
que
le
traitement
par le
paclitaxel
hebdomadaire ait apporté un
léger
bénéfice en matière
de
s
u
r
vie
dans presque tous
les
sous-groupes, aucune interaction
i
mp
or
t
a
nt
e
n
’
a
été observée dans aucun
des
sous-groupes. Dans une analyse
exploratoire,
la SG a
été analysée chez
les
patients ayant reçu
d
e
l
’
i
r
i
n
o
t
éc
a
n
et du paclitaxel
à
titre
de
chimiothérapie
de
s
ec
o
n
d
e
ligne
et de
ligne tardive.
La SG
médiane était
de
10,1 mois
dans
chaque groupe
et les
courbes
de
survie
de ces
deux
sous-groupes
se
chevauchaient presque
(HR,
0,96
; IC à 95 %,
0,69
à
1,32 ;
P
bilatéral
=
0,96).
 6
6
 7
7
 8
8
1
/
8
100%