Chapitre 1

Complément - Chapitre 6
Alcanes
Caractéristiques spectrales des alcanes
-Spectroscopie infrarouge (IR)
Les spectres IR des alcanes sont généralement très simples à analyser. Les bandes
caractéristiques fréquemment observées sont présentées dans le tableau 6.a.
Tableau 6.a Bandes IR caractéristiques des alcanes
Type de liaison Nombre d’onde
(cm-1) Mode de vibration Intensité
C-H (alcane) 2 960-2 850 Élongation Forte
-CH2- 1 470 Déformation Moyenne
-CH3 1 350 Déformation Faible à Moyenne
Dans le spectre de l’hexane illustré à la figure 6.a, on remarque d’abord le pic intense dans la
région située entre 2 960 cm-1 et 2 850 cm-1. C’est le pic caractéristique de l’élongation de la
liaison C–H. Il est très intense en raison du très grand nombre de liaisons C–H dans une molécule
d’alcane, telle que la molécule de l’hexane. Deux autres bandes d’absorption sont également
observées dans un spectre IR d’un alcane, soit vers 1 470 cm-1 et vers 1 350 cm-1. Ils
correspondent respectivement aux déformations angulaires des groupements méthylène CH2 et
méthyle CH3. Ces trois bandes d’absorption caractéristiques des alcanes sont retrouvées dans la
grande majorité des spectres IR des molécules organiques en raison de leur squelette carboné
commun. En effet, les groupements CH3, CH2 ou CH sont présents dans presque tous les
composés organiques.
Chapitre 6 – Complément © 2008 Les Éditions de la Chenelière inc. 1

Figure 6.a Spectre IR de l’hexane
Spectre réalisé sur Thermo Electronic Corporation, Nicolet IR 100
par Danielle Lapierre et Claude Gaudreault du Collège Jean-de-Brébeuf.
Enfin, un œil expert serait capable de déduire plusieurs informations dans l’empreinte digitale
d’un spectre d’alcane telle la présence de ramifications ou de cycles au sein de la structure
moléculaire. Toutefois, ces subtilités sont largement trop complexes pour qu’elles soient traitées
dans cet ouvrage.
- Résonance magnétique nucléaire (spectre RMN)
Les spectres RMN 1H des alcanes présentent souvent d’immenses multiplets dans les régions
caractéristiques des alcanes, soit de 0,9 ppm à 1,5 ppm. Ceci est dû à l’absence de groupements
fonctionnels dans les alcanes qui pourraient venir modifier l’environnement chimique des
hydrogènes en les blindant ou en les déblindant. De plus, puisque les rotations sont libres autour
de chacune des liaisons σ, tous les hydrogènes sont couplés à leur voisin immédiat respectant
alors la règle du n+1 avec des constantes de couplage d’environ 7 Hz. Enfin, puisque les groupes
d’hydrogènes non équivalents possèdent des déplacements chimiques semblables, des
recouvrements des pics sont souvent observés.
Chapitre 6 – Complément © 2008 Les Éditions de la Chenelière inc. 2

Dans le cas des spectres RMN 13C, les signaux des atomes de carbone des alcanes se situent dans
une région assez étendue allant de 0 ppm à 60 ppm. Les pics peuvent, en général, être aisément
associés au carbone correspondant.
Les spectres RMN 1H et RMN 13C de l’octane sont présentés à la figure 6.b.
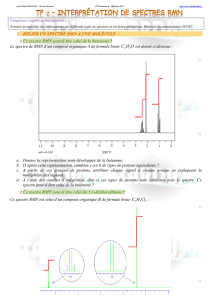
Figure 6.b A) Spectre RMN 1H de l’octane (solvant : CDCl3)
Spectre réalisé sur Bruker Avance 400 PJAB par François Raymond, étudiant
au doctorat au laboratoire du professeur James D. Wuest à l'Université de Montréal.
Chapitre 6 – Complément © 2008 Les Éditions de la Chenelière inc. 3

B) Spectre RMN 13C de l’octane (solvant : CDCl3)
Spectre réalisé sur Bruker Avance 400 PJAB par François Raymond, étudiant
au doctorat au laboratoire du professeur James D. Wuest à l'Université de Montréal.
Chapitre 6 – Complément © 2008 Les Éditions de la Chenelière inc. 4
1
/
4
100%