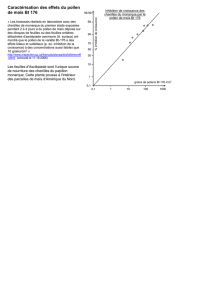
illustration P2B

Histoire du maïs
Ancêtre sauvage
Domestication
Mésoamérique
Présence de la téosinte
Mexique
Apparition du maïs vers le reste du monde
- 6000
- 4000
- 2000
0000
2000
2009
Séquençage
du génome
1990
Culture de maïs
OGM
1947
1er hybrides
en France
(1933 au USA)
1494
Introduction
en Europe

Écosystème maïs
Grains de Maïs
hannetons
taupins
limaces
corneilles
pucerons
chrysopes
hyménoptères
pyrales
adventices
carabes
Productivité:
9 à 16 t/ha/an
rapaces
coccinelle
s
MAÏS
volailles
vache
veau
campagnol
renard
Homme
LV
péricarpe transparent
vitreux
albumen
farineux
embryon
radicule
tigelle
scutellum
‘’germe’’ -
embryon
péricarpe
caryopse vu de face et
embryon en transparence
péricarpe
albumen
embryon
graine en coupe sagittale
embryon en coupe et de face
coléorhize
radicule
coléoptile
cotylédon
(scutellum)

Pyrale
Monohybridisme Maïs : F1, F2 et croisement-test
Dihybridisme chez le maïs
chenille ravageuse
oeuf
ponte
ponte
pyrale
maïs
maïs ‘’ravagé’’
F1
F1x
F1
F2
¾ de grains
noirs
¼ de grains
blancs
P
1/1
grains
noirs
épi F2 : 273
grains noirs et 92
grains blancs
épi test-cross :
173 grains noirs et
168 grains blancs
F1
P
½ de
grains
noirs
½ de
grains
blancs
FT
F1
P2
P1
F2
F1

Lignée pure : création, sélection scientifique dans le cas du maïs
« Pour obtenir des lignées parentales, il faut pendant de nombreuses générations, forcer artificiellement les plantes issues d'un croisement
de départ, à recevoir leur propre pollen, tout en évitant l'arrivée de pollens étrangers. Les fleurs femelles sont ensachées. L'autopollen est
recueilli à partir de la panicule de la plante et déposé sur les soies des fleurs femelles de la plante.
A chaque génération, seules les plantes les plus intéressantes sont retenues. L'obtention de lignées s'accompagne d'un effet dépressif
résultant des croisements consanguins répétés. Une lignée pure produit du pollen en quantité plus faible qu'un hybride.
Une lignée pure demande une attention particulière car elle est plus fragile et plus délicate à cultiver qu'un hybride.
Deux lignée pures sont croisées et les graines sont vendues pour être cultivées, c'est plante possédent la vigueur hybride.
Autopollinisation
« forcée »
Test d’aptitude
à la
combinaison
[Le sélectionneur recherche
parmi les lignées parentales en
cours de création, celles qui
donnent les meilleurs hybrides
lorsqu'elles sont croisées (test
d'aptitude à la combinaison).]
Sélection de
plantes dans une
population
hétérogène : variété
de pays ou F2
Plantes de 1ere
génération
50% d’homozygotie
Plantes de 2eme
génération
75% d’homozygotie
Plantes de 3eme
génération
87,5% d’homozygotie
Autofécondation
jusqu’à 7
générations
Vers => 100%
d’homozygotie
Lignée pure fixée : 100%
d’homozygotie

Domestication du blé
Caryotype haploïde
simplifié et loci de
gènes
Diversité
allèlique
-10000 -3000
ans
Domestication
Hybridations naturelles
Sélection par l’Homme
Premières
espèces
cultivées
Phénotypes
d’une espèce
sauvage
Sélection des
variétés
d’intérêt
Allèles
sélectionn
és
Variété moderne
Sélection moderne
Sélection moderne
Variété moderne
Transgénès
e
Variétés
locales
anciennes
Variété OGM
Hybridations naturelles ou provoquées
 6
6
 7
7
 8
8
1
/
8
100%