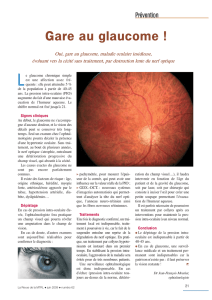
Modèle de collaboration entre les professions en matière de soins

Modèle de collaboration entre les professions en matière de
soins aux patients atteints de glaucome et à ceux qui
représentent des cas suspects de glaucome
Comité de la Société canadienne de glaucome sur la collaboration entre les professions en matière de
soins du glaucome
Les patients atteints de glaucome et ceux qui
représentent des cas suspects de glaucome englobent un
grand nombre de personnes—jusqu’à5%delapopu-
lation de plus de 40 ans, et la fréquence est encore plus
grande dans les groupes d’âge plus avancé. Avec le vie-
illissement de la population canadienne, le nombre de
personnes atteintes de glaucome ou de celles qui
représentent des cas suspects de glaucome devrait énor-
mément augmenter, ce qui mettra plus de stress sur les
ressources vouées aux soins de la vue.
Les patients atteints de glaucome et ceux qui représen-
tent des cas suspects de glaucome requièrent des soins de la
vue de deux types distincts de professionnels qualifiés—les
ophtalmologistes et les optométristes. Souvent, la commu-
nication entre ces professionnels est loin d’être idéale, et
peut mener au dédoublement des services et des examens.
Les ophtalmologistes sont des médecins (MD) qui,
après avoir passé quatre ans à l’école de médecine, pour-
suivent une formation spécialisée sur les maladies et les
chirurgies oculaires (résidence en ophtalmologie). Cette
formation spécialisée se poursuit pendant cinq ans. Après
leur programme en résidence, certains ophtalmologistes
vont suivre une autre formation en sous–spécialité (fellow-
ship) en glaucome, qui peut consister en un programme
d’un ou deux ans. Ces ophtalmologistes deviennent des
sous-spécialistes en glaucome. Les ophtalmologistes gé-
néralistes sont toutefois entièrement formés pour prendre
en charge autant l’aspect médical que chirurgical du glau-
come. Pour cette raison, nous ne faisons pas de différence
dans le présent document entre les ophtalmologistes gé-
néralistes et les ophtalmologistes avec formation sous-spé-
cialisée en glaucome.
Les optométristes suivent un programme de quatre ans
(école d’optométrie) au cours duquel ils sont formés pour
mener des examens visuels de routine, de réfractions et de
reconnaissance de certaines maladies de l’oeil, tel le glau-
come. Puisque les optométristes ne sont pas des médecins
en titre, ils ne sont pas formés pour pratiquer des chirurgies
ou toute forme de procédure au laser. Certains optométris-
tes choisissent de suivre une formation supplémentaire de
six à douze mois à la fin de leurs études optométriques, et ils
deviennent des « optométristes avancés»àlafindecette
formation supplémentaire.
Dans certaines provinces canadiennes, les optométristes
n’ont pas le droit de prescrire des médicaments contre le
glaucome et dans les provinces où ils sont habilités à le
faire, différents règlements s’appliquent. Dans le présent
document, nous avons décidé de ne pas tenir compte du
fait que les optométristes ont le droit ou non de prescrire
des médicaments, mais nous avons plutôt choisi de décrire
un modèle qui serait dans le meilleur intérêt des patients.
Il n’y a à l’heure actuelle ni modèle national ni recom-
mandations en ce qui touche la collaboration entre les pro-
fessions, soit entre les ophtalmologistes et les optométris-
tes, en matière de soins liés au glaucome. Même si la portée
de la pratique est mandatée par les provinces, l’existence
d’un ensemble national de recommandations axé sur le
patient ne peut qu’être bénéfique. Reconnaissant
l’importance de cette question, les membres de la Société
canadienne de glaucome (SCG) ont, en 2008, mis sur pied
un comité pour évaluer la nature d’une collaboration per-
tinente dans les soins du glaucome et proposer un modèle
de discussion pour les organismes régissant les ophtalmolo-
gistes et les optométristes (voir l’annexe A pour la liste des
membres de ce comité appartenant à la SCG). Après plu-
sieurs rencontres, des suggestions soumises par des mem-
bres de la SCG et des modifications supplémentaires ap-
portées par les membres du conseil d’administration de la
Société canadienne d’ophtalmologie (SCO) et du Conseil
des affaires provinciales, le document suivant est ressorti. Il
est à noter que les travaux demeurent inachevés et que les
parties intéressées pourraient être invitées à partager
d’autres commentaires. Notre but est de faire en sorte que
le présent document fournisse le cadre d’une collaboration
Comité de la Société canadienne de glaucome sur la collaboration entre les professions
en matière de soins du glaucome: Marcelo Nicolela, MD, FRCSC (président), Hal-
ifax, N.-É.; Yvonne Buys, MD, FRCSC, Toronto, ON; Catherine Birt, MD,
FRCSC, Toronto, ON; Shawn Cohen, MD, FRCSC, DABO, Montréal, QC; Gor-
don Douglas, MD, FRCSC, Calgary, AB; Bryce Ford, MD, FRCSC, Calgary, AB;
Lisa Gould, MD, FRCSC, Winnipeg, MB; Cindy Hutnik, MD, FRCSC, London,
ON; Caroline Lajoie, MD, FRCSC, DABO, Québec, QC; Raymond LeBlanc,
MD, FRCSC, OC, Halifax, N.-É.; Robert Schertzer, MD, FRCSC, Vancouver,
C.-B.; James Taylor, MD, FRCSC, Victoria, C.-B.
“English on page S1.”
Accepté pour publication le 15 juin 2011. Publication en ligne le Novembre
11, 2011
Can J Ophthalmol 2011;46:S11–S21
0008-4182/11/$-see front matter © 2011 Published by Elsevier Inc on behalf of
the Canadian Ophthalmological Society.
doi:10.1016/j.jcjo.2011.09.002
CAN J OPHTHALMOL—VOL. 46, SUPP. 1, December 2011 S11

provinciale entre les optométristes et les ophtalmologistes
dans les soins liés au glaucome.
PORTÉE ET CLAUSE EXONÉRATOIRE
Le présent document a été rédigé afin de mieux définir
les modèles de soins pour les patients atteints de glaucome
et pour ceux qui représentent des cas suspects de glaucome,
avec comme but ultime un meilleur accès aux soins et une
meilleure qualité des soins fournis à ces patients.
Les patients qui souffrent de glaucome ont différents
degrés de la maladie. Il est difficile de généraliser les
modèles de soins qui s’appliquent à toutes les présentations
cliniques possibles. Néanmoins, il est important de caté-
goriser les patients atteints de glaucome. Des modèles de
collaboration entre les professions sont nécessairement,
mais non exclusivement, liés à la gravité de la maladie et au
type de glaucome.
Ce modèle a été élaboré en tenant compte des meilleures
données probantes disponibles et son but n’est pas de re-
streindre l’innovation. Lefait de se conformer à ce modèle ne
donnera pas de résultats gagnants dans chaque cas. Le but de
ce modèle n’est pas de restreindre les champs d’activités ni de
servir comme normes de soins médicaux. Les normes de soins
médicaux sont pertinentes à tous les faits ou circonstances
dans un cas individualisé, et peuvent être sujettes à changer à
mesure qu’évoluent les connaissances scientifiques, la tech-
nologie et les tendances de la pratique.
Il faut reconnaître que dans un modèle de soins entre les
professions, chacun des membres de l’équipe de soins est
tenu responsable des soins qu’il prodigue et peut également
être tenu responsable de son rôle dans les résultats. (Les
lecteurs sont renvoyés à l’article de l’ACPM intitulé « Une
nouvelle réalité : l’élargissement des champs d’exercices »,
publication originale en mars 2006/révisée en août 2008,
mars 2009 [IS0661-E]). La portée du présent document ne
permet pas de discuter des conséquences médico-légales de
la collaboration entre les professions du domaine de la
santé dans la gestion du glaucome. Des consultations
devraient avoir lieu avec les fournisseurs de services
d’assurances médico-légales pertinents afin de déterminer
les conséquences des soins donnés en collaboration pour
chaque groupe professionnel touché.
PRINCIPES DE LA COLLABORATION ENTRE LES
PROFESSIONS
Lors des discussions menant à la rédaction de ce docu-
ment, plusieurs principes clés portant sur la collaboration
entre les professions dans les soins du glaucome ont été
déterminés. Le présent document a été élaboré en tenant
compte de ces principes.
Les principes clés de la collaboration entre les profes-
sions dans les soins du glaucome sont :
●Approche axée sur le patient
●Accès en temps opportun au professionnel pertinent
en soins de la vue
●Engagement continu envers les normes élevées de
qualité des soins
●Approche fondée sur des preuves
●Relations collégiales
●Communication efficace, claire et en temps opportun
●Utilisation optimale des compétences profession-
nelles et des ressources limitées
●Dédoublement des examens et des services gardé au
minimum
QUALIFICATIONS PRÉALABLES POUR LA PRISE EN
CHARGE DES PATIENTS PRÉSENTANT DES CAS
SUSPECTS DE GLAUCOME ET DES PATIENTS ATTEINTS
DE GLAUCOME
Les professionnels qui s’occupent de prendre en charge des
patients atteints de glaucome et ceux représentant des cas sus-
pects de glaucome doivent avoir les connaissances appropriées
sur la maladie, les compétences cliniques, l’accès aux examens
spécialisés et les habiletés pour bien interpréter les résultats
d’examens. Il n’est pas du ressort du présent document de
déterminer les méthodes d’évaluation des compétences de
tous les professionnels qui prennent en charge les patients
atteints de glaucome. Il ne relève pas non plus du présent
document de déterminer les méthodes d’enseignement des
nouvelles compétences aux professionnels qui ne sont pas
présentement compétents. Une modification du modèle ac-
tuel de prestation des soins aux patients atteints de glaucome
devra être combinée à l’enseignement, à l’acquisition et au
maintien des compétences pertinentes requises.
Tout professionnel qui prend en charge ces patients
devrait recueillir les antécédents pertinents oculaires,
médicaux et familiaux, en mettant particulièrement
l’accent sur l’identification des facteurs de risques possibles
du glaucome (voir l’annexe B).
Il est attendu que ces professionnels seront compétents
dans les habiletés suivantes. Il y aurait lieu de faire remar-
quer que les examens et procédures recommandés portent
sur les meilleures données probantes actuellement dis-
ponibles et que cela peut changer à l’avenir à mesure que la
pratique fondée sur les preuves évolue :
(1) Tonométrie par applanation au moyen de
tonomètres dûment calibrés. L’étalon d’or est la
tonométrie par applanation de Goldmann (TAG),
mais d’autres tonomètres peuvent être utilisés dans
des circonstances particulières où la TAG n’est pas
techniquement possible, comme dans le cas de pa-
tients ayant une cornée irrégulière. La tonométrie à
jet d’air et le Tono-Pen ne sont pas considérés
comme étant assez fiables pour suivre les patients
atteints de glaucome.
(2) Gonioscopie pour la détection des anomalies des
angles, comme les risques de glaucome par ferme-
Modèle de collaboration en matière de soins de glaucome—Nicolela et al.
S12 CAN J OPHTHALMOL—VOL. 46, SUPP. 1, December 2011

ture d’angle ou de glaucomes secondaires, répétée
selon les besoins cliniques. Par exemple, la goniosco-
pie devrait être répétée s’il y a une augmentation mar-
quée de la pression intraoculaire (PIO) ou lors de la
présence d’autres signes suggérant une modification
de la configuration de l’angle (comme une modifica-
tion de la profondeur de la chambre antérieure ou de
la présence de néovascularisation de l’iris).
(3) Biomicroscopie par lampe à fente stéréoscopique,
avec ou sans lentilles de contact, avec attention por-
tée à des résultats précis comme des hémorragies de
la papille, des modifications localisées de la papille,
etc. Une méthode reproductible de documentation
de l’état du nerf optique est requise afin de déter-
miner les changements se produisant avec le temps.
La documentation sur l’état de base et séquentiel de
la papille devrait se faire au moyen de la photogra-
phie de la papille et/ou des analyseurs de la tête du
nerf optique et de la couche de la fibre nerveuse de
la rétine. La photographie du fond de l’æil ou
l’imagerie seule ne devrait pas remplacer
l’inspection visuelle du nerf optique et de la couche
des fibres nerveuses de la rétine. Si des examens
d’imagerie automatisée sont possibles, une bonne
interprétation des résultats d’examen est essentielle,
en mettant particulièrement l’accent sur la qualité
de l’imagerie et l’intégration clinique des résultats
(pour le diagnostic et la progression).
(4) Évaluation du champ visuel, par la périmétrie au-
tomatisée standard et les instruments de mesure du
seuil (l’analyseur du champ visuel de Humphrey ou
le périmètre d’Octopus sont des exemples
d’instruments préférés). L’évaluation soignée du
champ visuel et de sa progression est essentielle.
L’évaluation de la fiabilité et de l’intégration des
résultats pertinents sont d’égale importance pour la
périmétrie et l’examen de la papille.
(5) Connaissance approfondie de l’efficacité, du profil
des effets secondaires et des contre–indications de
tous les médicaments utilisés dans le traitement du
glaucome, ainsi que les indications et complications
possibles le glaucome résultant des chirurgies par
incision et au laser.
Un préalable pour une collaboration économique entre
les professionnels en optométrie et en ophtalmologie dans
la gestion des patients atteints du glaucome et des patients
représentant des cas suspects de glaucome consiste en une
communication efficace, claire et en temps opportun. Ceci
comprend le partage des données et des résultats pertinents
des examens (comme les mesures de la PIO, les médica-
ments utilisés, les photos de la papille ou d’autres examens
d’imagerie et du champ visuel), afin de permettre une
bonne évaluation et la continuité des soins, sans le dé-
doublement non nécessaire des examens. L’utilisation
d’équipement d’examen diagnostique semblable dans
chaque bureau impliqué facilitera un partage fructueux des
résultats, en particulier pour l’évaluation du champ visuel.
Un exemple de demande de consultation appropriée pour
les patients atteints de glaucome est présenté à l’annexe C.
Comme le glaucome est une maladie chronique, la con-
tinuité des soins cliniques est d’importance capitale. Le
patient devrait savoir qui est le professionnel de la vue
responsable de ses soins à chaque étape de la gestion de la
maladie. Une excellente communication entre les professi-
onnels de la vue assurera également que le transfert des
soins est bien compris.
DÉFINITION DES GROUPES DE PATIENTS
Afin de mieux catégoriser les patients en fonction de leur
présentation clinique, de la gravité de la maladie et du
besoin de traitement hypotenseur, certains groupes de pa-
tients ont été identifiés. Il ne faut pas utiliser ce regroupe-
ment des patients comme étant une classification complète
du glaucome, mais plutôt comme une tentative de fournir
un cadre propice en vue de recommandations touchant la
prise en charge.
Cas suspects de glaucome avec risque faible/modéré
Ce groupe comprend un des scénarios cliniques suivants :
(1) Présence d’applanation élevée de la PIO ne dépas-
sant pas 27 mm Hg, avec des champs visuels nor-
maux (test de l’hémichamp du glaucome normal ou
examens équivalents) et papille (s) normale (s).
(2) Antécédents familiaux positifs de glaucome avec
champs visuels et papille (s) normaux.
(3) Papille (s) suspecte (s) chez les patients avec une
PIO normale (inférieure à 22 mm Hg) et champs
visuels normaux.
(4) Examens suspects du champ visuel non encore con-
firmés dans un second examen.
(5) Présence d’autres conditions communément associées
au glaucome, mais sans élévation de la PIO (comme la
dispersion pigmentaire, la pseudoexfoliation).
Cas suspects de glaucome avec risque élevé (ou
déjà sous traitement topique)
Ce groupe comprendra un des scénarios cliniques suivants :
(1) La présence de PIO élevée supérieure à 27 mm Hg
(ou dépassant 24 mm Hg associée à une épaisseur
relativement mince du centre de la cornée inféri-
eure à 550 microns).
(2) Papille suspecte de glaucome , comme des enco-
ches, des hémorragies de la papille, des anomalies
localisées de la couche des fibres nerveuses de la
rétine, mais avec des champs visuels normaux.
(3) PIO élevée associée à d’autres causes de glaucome
secondaire comme la pseudoexfoliation, la disper-
sion pigmentaire, l’uvéite, la néovascularisation de
Modèle de collaboration en matière de soins de glaucome—Nicolela et al.
CAN J OPHTHALMOL—VOL. 46, SUPP. 1, December 2011 S13

l’iris ou de l’angle, mais sans signes clairs de dom-
mage à la papille ou d’une perte du champ visuel.
(4) Les patients qui représentent des cas suspects de
glaucome qui sont déjà traités par la thérapie pour
la diminution de la PIO.
(5) Les patients ayant un angle estimé à risque élevé de
fermeture (généralement 180 degrés ou plus de
contact irido-trabéculaire).
Patients dans les premiers stades du
glaucome—stable
Les premiers stades du glaucome sont définis en fonc-
tion des critères énoncés dans les lignes directrices de la
pratique clinique sur le glaucome de la Société canadienne
d’ophtalmologie (voir l’annexe D). La stabilité est définie
comme la PIO dans les limites d’un écart de pression cible
et aucune détérioration du champ visuel ou de la papille au
cours des trois dernières années. Remarque : tout patient
récemment identifié comme atteint de glaucome serait
considéré comme instable jusqu’à ce que sa stabilité soit
prouvée lors d’un suivi à long terme.
Patients atteints de glaucome modéré/avancé—stable
Le glaucome modéré et avancé est défini selon les critères
énoncés dans les lignes directrices sur le glaucome de la SCO
(voir l’annexe D); la stabilité est définie comme ci-dessus.
Patients atteints de glaucome instable
Les patients instables sont ceux ayant une PIO qui dé-
passe la cible ou ayant une détérioration prouvée, dans le
passé récent, de la papille ou du champ visuel.
Glaucome aigu (ou les patients atteints de toute
forme chronique de glaucome présentant une PIO
très élevée)
Ce groupe comprend les patients présentant une PIO très
élevée (généralement supérieure à 40 mm Hg), ayant apparu
soudainement (d’habitude caractérisée par des symptômes
comme la nausée, la douleur, la diminution de l’acuité
visuelle, des halos) ou une présentation plus chronique.
RECOMMANDATIONS
Les recommandations sont présentées en relation avec
les groupes définis plus tôt. Il s’agit seulement de recom-
mandations et elles doivent s’adapter aux circonstances in-
dividuelles de la présentation clinique, à la disponibilité des
professionnels des soins de la vue et des ressources (voir
l’annexe E pour le sommaire des recommandations). Un
principe général inhérent dans ce modèle est que
l’ophtalmologiste qui sera probablement le plus impliqué
dans les soins futurs d’un patient donné devrait pouvoir
l’évaluer tôt au début de la maladie.
Cas suspects de glaucome à risque faible/modéré
Les patients représentant des cas suspects de glaucome et
ayant été évalués initialement par l’optométriste traitant et
estimés présenter un risque faible à modéré n’ont pas be-
soin d’être dirigés vers un ophtalmologiste. Si toutefois le
patient présente une combinaison de plus d’un des scé-
narios cliniques décrits ci–dessus (par exemple, une PIO
élevée et une papille suspecte), alors le patient devrait être
considéré comme représentant un risque élevé de cas sus-
pect de glaucome (voir 5b ci–dessus).
Une fois l’évaluation initiale complétée, la fréquence des
examens de suivi sera laissée à la discrétion du professionnel
responsable des soins de la vue. Les intervalles recomman-
dés apparaissent dans l’annexe F. À chacune des visites de
suivi, la stabilité de la maladie devrait être évaluée (c.–à–d.
est–ce que la PIO, la papille et le champ visuel sont sta-
bles?). Dans les cas où on soupçonne un changement dans
la papille ou dans le champ visuel depuis l’évaluation ini-
tiale, un second examen de confirmation devrait avoir lieu au
cours des quatre à six mois suivants (second examen du champ
visuel ou autre mesure de la PIO, par exemple). Si le change-
ment est confirmé, alors le patient devrait être pris en charge
comme un patient présentant un cas suspect de glaucome à
risque élevé ou comme un patient atteint de glaucome débu-
tant, selon le scénario clinique, et les recommandations pour
la catégorie pertinente devraient être suivies.
Cas suspects de glaucome—risque élevé
Un patient représentant un cas suspect de glaucome à
risque élevé est peut–être déjà sous thérapie pour abaisser la
PIO. Qu’il soit ou non sous cette thérapie, il doit être
évalué et/ou examiné plus fréquemment. Les patients de ce
groupe auront besoin de bons examens de base, préférable-
ment à tout le moins des images de base de la papille et de
deux champs visuels au cours des six premiers mois. De
plus, ces patients auront besoin d’évaluations périodiques
du champ visuel et de l’imagerie afin d’assurer la stabilité
du portrait clinique. La fréquence suggérée des tests est
présentée dans l’annexe F. Les patients devraient être in-
formés de leurs facteurs de risques à développer le glau-
come et la décision d’initier ou d’augmenter le traitement
hypotenseur doit être discutée avec eux.
Règle générale, les patients représentant un cas suspect à
risque élevé de glaucome peuvent être suivis par
l’optométriste avec des consultations périodiques avec
l’ophtalmologiste. L’intervalle de ces consultations péri-
odiques dépendra du scénario clinique, mais les consulta-
tions suivront de près l’évaluation initiale de l’optométriste
et auront ensuite lieu au moins tous les trois à quatre ans, ou si
l’une des conditions suivantes énumérées ci-dessous apparaît.
Dans le cas où la décision de commencer la thérapie oculaire
hypotensive est considérée, le patient devra d’abord être
acheminé à un ophtalmologiste pour une évaluation. Un plan
de traitement clairement défini et les cibles de PIO doivent
être communiqués à l’optométriste.
Les situations cliniques exigeant l’acheminement à un
ophtalmologiste sont les suivantes :
Modèle de collaboration en matière de soins de glaucome—Nicolela et al.
S14 CAN J OPHTHALMOL—VOL. 46, SUPP. 1, December 2011

(1) Si l’initiation ou l’augmentation de la thérapie ocu-
laire hypotensive est considérée.
(2) Si l’on soupconne une progression au niveau de la
papille ou le champ visuel.
(3) Si les données cliniques sont incertaines.
Patients atteints de glaucome débutant stable
Lorsque l’optométriste détecte un glaucome débutant, le
patient sera dirigé vers un ophtalmologiste en temps oppor-
tun. Tous les patients récemment diagnostiqués sont consi-
dérés comme étant susceptibles d’être instables jusqu’à ce que
la stabilité soit démontrée au cours du suivi. Les décisions
portant sur le traitement, la PIO cible appropriée et la
fréquence des examens doivent être clairement communi-
quées par l’ophtalmologiste à l’optométriste. Une fois stabi-
lisé, le patient peut être retourné à l’optométriste pour une
surveillance et une prise en charge au besoin. Ces patients
seront réévalués par un ophtalmologiste à intervalles réguliers,
au moins tous les deux à trois ans. L’ophtalmologiste continue
donc d’avoir des contacts cliniques avec le patient, ce qui peut
être particulièrement valable si le patient a éventuellement
besoin de chirurgie au laser ou incisionnelle. Comme le glau-
come est une condition à vie et qu’il peut causer la cécité, il est
essentiel que les optométristes et les ophtalmologistes se partagent
librement tous les renseignements cliniques pertinents ainsi que
l’information sur les examens. Ceci préviendra le dédoublement
et permettra ainsi de contrôler les coûts et les désagréments causés
au patient et au système médical.
La stabilité de la maladie sera confirmée au moyen
d’examens périodiques (voir l’annexe F), en s’assurant que la
PIO demeure dans la zone cible déjà déterminée et que les
champs visuels et les papilles ne montrent pas de signes de
détérioration. La détérioration du champ visuel devrait être
analysée au moyen du logiciel pertinent, comme l’analyse pro-
gressive guidée de l’appareil Humphrey (GPA),
PROGRESSOR, PeriData ou d’autres stratégies validées
semblables. La détérioration de la papille sera déterminée par
l’examen soigné des photographies de la papille et/ou par
l’interprétation qui convient du logiciel sur la progression dis-
ponible avec les instruments automatisés d’imagerie courants
(papille et/ou couche des fibres nerveuses de la rétine).
Patient stable au stade modéré/avancé
Les stades modérés et avancés de la maladie sont déter-
minés selon les critères définis dans l’annexe D. Les pa-
tients dont la maladie est plus grave courent un risque élevé
de handicap visuel et de cécité et devraient généralement
être traités de façon plus agressive et être suivis à des inter-
valles plus fréquents que ceux qui sont dans les premiers
stades de la maladie (voir l’annexe F).
Les patients stables au stade modéré ou avancé de la maladie
devraient principalement être pris en charge par un ophtalmolo-
giste, à moins que des obstacles de transport ou la non-dis-
ponibilité d’un ophtalmologiste constituent des problèmes ma-
jeurs. Ces patients courent un risque considérable que la maladie
progresse même si leur PIO est stable. Une attention particulière
devrait être mise sur la surveillance de l’état du champ visuel et de
la papille. Les intervalles recommandés de suivis pour les examens
sont présentés à l’annexe E.
La prise en charge clinique de ces patients devrait porter
sur l’assurance de la stabilité de la PIO, du champ visuel et
du nerf optique, sur la fidélité au traitement et sur la
tolérance aux médicaments.
Patients atteints de glaucome instable
Les patients devraient être considérés comme étant in-
stables s’ils ont montré des signes de dommage progressif
glaucomateux, ou s’ils n’atteignent pas les cibles précisées
antérieurement pour la PIO. De plus, ainsi que mentionné
plus tôt, les patients récemment diagnostiqués sont consi-
dérés comme instables jusqu’à ce que leur stabilité soit
prouvée lors du suivi. La progression du glaucome est dif-
ficile à définir et elle varie en fonction du stade de la mala-
die et de la méthodologie utilisée pour surveiller les papilles
et les champs visuels. Les lignes directrices de la SCO sur le
glaucome définissent la « progression » ainsi : « Le glau-
come d’un patient est estimé avoir progressé si les change-
ments structuraux et (ou) fonctionnels, associés à la mala-
die, sont détectés de manière vérifiable au moment de
l’examen clinique et (ou) des tests. »
L’instabilité de la maladie peut se manifester sous forme de
PIO incontrôlée, de progression du champ visuel et/ou de
progression de la papille. Ce qui suit représente une liste des
scénarios cliniques de patients atteints de glaucome instable :
(1) Instabilité de la PIO : Si un patient recevant un
traitement pour le glaucome est pris en charge par un
optométriste et que la PIO est supérieure à la cible
établie de la PIO, l’optométriste devrait réacheminer
le patient à un ophtalmologiste. L’optométriste com-
muniquera les renseignements relatifs aux médica-
ments utilisés et la PIO qui s’ensuit, et enverra aussi
tous les examens auxiliaires pertinents.
(2) Critères pour le champ visuel : Si un patient est pris
en charge par un optométriste et qu’il y a des change-
ments reproductibles et cliniquement importants
dans le champ visuel, il doit être réacheminé à un
ophtalmologiste. L’optométriste fera part de tous les
résultats cliniques pertinents et enverra tous les résul-
tats disponibles d’examen du champ visuel et
d’imagerie de la papille (sous format papier ou électro-
nique).
(3) Critères pour le nerf optique : Si un patient est
pris en charge par un optométriste et qu’il se
produit un changement reproductible et clinique-
ment important dans l’apparence de la couche des
fibres nerveuses de la rétine ou du nerf optique,
l’optométriste doit réacheminer le patient à un
ophtalmologiste. Si la technologie d’imagerie est
utilisée, le changement devrait pouvoir être démon-
tré comme pouvant être répété. L’optométriste
transmettra les résultats de l’imagerie à
Modèle de collaboration en matière de soins de glaucome—Nicolela et al.
CAN J OPHTHALMOL—VOL. 46, SUPP. 1, December 2011 S15
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
1
/
11
100%