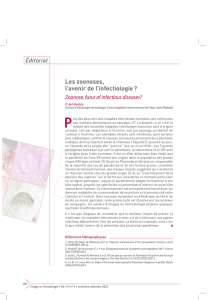
CIVD et gangrène périphérique dans un cas de paludisme sévère

CIVD et gangrène périphérique
dans un cas de paludisme sévère :
le cycle coagulation-inflammation appliqué
au Plasmodium falciparum
DIC and peripheral gangrene in a severe Plasmodium falciparum malaria:
the coagulation-inflammation cycle with Plasmodium falciparum as a model
A. Tessier-Marteau
1
S. le Cruguel
1
F. Grand
1
P. Asfar
2
M. Zandecki
1
L. Macchi
1
1
Laboratoire d’hématologie,
CHU Angers
<anmarteau@chu–angers.fr>
2
Service de réanimation, CHU d’Angers
Article reçu le 20 mai 2009,
accepté le 9 juillet 2009
Résumé. La survenue d’une gangrène périphérique avec coagulation intravas-
culaire disséminée (CIVD) au cours du paludisme sévère à Plasmodium falcipa-
rum est un événement rare et grave ; nous rapportons une telle observation chez
un homme de 62 ans au service de réanimation médicale dont la gangrène des
orteils a nécessité une amputation. Les mécanismes physiopathologiques res-
ponsables d’une coagulopathie de consommation dans cette situation sont
aujourd’hui mieux compris, et le paludisme peut être utilisé comme modèle
pour expliquer les relations entre coagulation et inflammation. L’utilisation de
molécules anticoagulantes, grâce à leurs propriétés anti-inflammatoires, est une
voie thérapeutique intéressante pour freiner le cycle coagulation-inflammation.
Mots clés : Plasmodium falciparum, facteur tissulaire, cytokines pro-
inflammatoires, gangrène, coagulation intravasculaire disséminée
Abstract. Peripheral gangrene with disseminated intravascular coagulation
(DIC) during severe Plasmodium falciparum malaria has already been descri-
bed but is unfrequent. We report here the case of a 62-year-old man admitted
in the intensive care unit of our hospital for severe Plasmodium falciparum
malaria with disseminated intravascular coagulation (DIC) and peripheral gan-
grene of his toes that needed amputation. Pathophysiological mechanisms lea-
ding to DIC in malaria can be used as a model to explain the relation between
coagulation and inflammation. Therapeutic targeting of coagulation, by acting
on inflammation, could be useful to limit the coagulation-inflammation cycle.
Key words: Plasmodium falciparum, tissue factor, pro-inflammatory cytokines,
gangrene, disseminated intravascular coagulation
Les formes graves de paludisme représentent environ 1 %
des infections palustres et la mortalité associée est estimée
de 10 à 30 % [1] malgré une prise en charge dans des
services de réanimation. Les troubles majeurs de la coa-
gulation font partie des critères de gravité [2, 3]. Une coa-
gulation intravasculaire disséminée (CIVD) est retrouvée
dans 5 % à 30 % des cas [1-4] et une vingtaine de cas de
gangrène associée au paludisme ont été décrits [4-6], la
plupart en zone endémique et associés à une CIVD. Une
amputation a été effectuée dans la moitié des cas.
L’observation
Il s’agit d’un patient de 62 ans, effectuant des séjours
répétés au Cameroun avec une prophylaxie antipalu-
pratique quotidienne abc
Ann Biol Clin 2009 ; 67 (5) : 569-72
doi: 10.1684/abc.2009.0367
Ann Biol Clin, vol. 67, n
o
5, septembre-octobre 2009 569
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 04/06/2017.

déenne par l’association atovaquone/chlorhydrate de pro-
guanil (Malarone
®
). Le traitement n’a pas été suivi lors du
dernier séjour de 15 jours. Il est retrouvé la notion d’un
court épisode fébrile résolutif sur place. Dix jours après
son retour, le patient présente une fièvre élevée avec pics,
des céphalées, une toux sèche, une diarrhée et une anore-
xie. Un traitement par antibiotique (amoxicilline + acide
clavulanique) et paracétamol est prescrit par son médecin
traitant.
Devant l’absence d’amélioration, le patient consulte au
service des urgences de sa ville. L’examen clinique mon-
tre une fièvre à 40 °C, une légère obnubilation, une hypo-
tension (84/61 mmHg), une tachycardie et une polypnée
ainsi qu’une cyanose des extrémités. Le bilan biologique
montre une leucopénie (2,8 G/L, N : 4-10), une insuffi-
sance rénale (urée : 18 mmol/L, N : 2,50-8,30 ; créati-
nine : 153 μmol/L, N : 80-120), une insuffisance hépa-
tique (ASAT à 3 N, bilirubine totale : 112 μmol/L, N :
5-20 ; bilirubine conjuguée : 74 μmol/L, N : 0-4 ; biliru-
bine libre : 38 μmol/L, N : 4-16), lactatémie : 4,6 mmol/L
(N : 0,4-2) et une CRP élevée : 222 mg/L (N < 3). Il n’ya
pas d’anémie (hémoglobine : 166 g/L ; N : 130-180).
Le bilan de CIVD est positif avec un score de l’Internatio-
nal Society of Thrombosis and Haemostasis (ISTH) [7] à 6 :
thrombopénie à 11 G/L (N : 150-400 G/L), allongement du
temps de Quick de 4 secondes par rapport au témoin, dimi-
nution du fibrinogène plasmatique (1,23 g/L ; N : 2-4 g/L),
D-dimères entre 32 et 64 μg/mL (N < 0,5 μg/mL). La recher-
che de complexes solubles par le test à l’éthanol est posi-
tive. Le frottis sanguin met en évidence la présence de Plas-
modium falciparum avec 9 % d’hématies parasitées.
Le diagnostic de paludisme grave [2] est posé ; le patient
est transféré en réanimation médicale à l’hôpital d’Angers.
À son admission, il présente des troubles confusionnels,
un ictère cutanéomuqueux avec une aggravation de
l’insuffisance rénale et une parasitémie à 20 %. Il n’ya
pas de déficit neurologique excepté des douleurs neuro-
gènes des orteils à type de brûlures. Les orteils à l’admis-
sion sont décolorés et deviennent cyanosés dès le lende-
main malgré un enveloppement dans de la ouate pour
essayer d’augmenter la température locale. Le patient n’a
pas reçu de traitement anticoagulant pendant son séjour en
réanimation. Les hémocultures à la recherche d’une co-
infection bactérienne sont négatives. L’état du patient
s’améliore après traitement par quinine et ceftriaxone.
L’hémodynamique reste stable sous de faibles doses de
noradrénaline. Les complexes solubles se négativent en
3 jours et la goutte épaisse en 7 jours. La fonction rénale
s’améliore après dialyse, les enzymes hépatiques se nor-
malisent et le patient quitte le service de réanimation
11 jours après son admission. Une héparinothérapie pré-
ventive par héparine non fractionnée à 5 000 UI/12 heures
est prescrite pour son transfert en soins de suite.
Durant son hospitalisation, le patient a présenté une
hémorragie suite à la pose d’un cathéter de dialyse jugu-
laire (la concentration d’hémoglobine passant de 148 à
91 g/L) qui a nécessité la transfusion de 4 culots globu-
laires et 4 fractions de plasma frais congelé. La persistance
des zones de nécrose au niveau des orteils a conduit à
l’amputation de 4 orteils gauches et 3 orteils droits
3 semaines après la sortie du patient.
Discussion
La CIVD
La CIVD au cours d’un paludisme peut être secondaire à
une infection bactérienne associée dans 14 % des cas [2],
et la fréquence de l’association est assez importante pour
recommander une antibiothérapie concomitante au traite-
ment antipaludéen dans les formes sévères [2]. Concer-
nant l’observation rapportée, la CIVD peut être secondaire
àl’infection palustre en elle-même, mais l’exclusion
d’une septicémie associée est difficile car le patient a
reçu une antibiothérapie préalable pouvant expliquer les
hémocultures négatives. Dans le cas d’infection palustre
isolée, il a été démontré que les anomalies de la coagula-
tion étaient corrélées à la parasitémie, la thrombopénie et
la sévérité de l’infection [8] : les troubles de la coagula-
tion semblent donc jouer un rôle dans la progression de la
maladie et la défaillance viscérale du paludisme [3, 8].
Les anomalies de la coagulation observées dans le palu-
disme à Plasmodium falciparum sont très semblables à
celles observées lors d’une CIVD : l’activation plaquet-
taire est responsable de la thrombopénie, l’activation de
la cascade de la coagulation, la diminution des inhibiteurs
de la coagulation (antithrombine, protéine C, protéine S)
et l’hypofibrinolyse concourent au phénomène d’hyper-
coagulabilité [9]. L’activation de la coagulation reste
généralement modérée dans les formes de paludisme peu
sévères (absence de signes cliniques, allongement modéré
voire absent des temps de coagulation mais présence de
D-dimères), ce qui peut correspondre à une CIVD com-
pensée ou biologique [7]. Au contraire, dans les formes
sévères comme le neuropaludisme, l’activation de la coa-
gulation est plus importante avec un score ISTH signifi-
catif [7] et des manifestations cliniques à type de saigne-
ments dans 10 % des cas [8], ce qui peut être observé lors
d’une CIVD décompensée.
La physiopathologie de la CIVD, notamment secondaire à
un sepsis, est maintenant bien connue [10-12]. Le stimulus
initiateur est l’exposition systémique et excessive de fac-
teur tissulaire (FT) à la circulation sanguine : l’interaction
de composés de la membrane bactérienne (lipopolysac-
charides des bacilles à Gram négatif par exemple) avec
pratique quotidienne
570 Ann Biol Clin, vol. 67, n
o
5, septembre-octobre 2009
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 04/06/2017.

des récepteurs spécifiques comme les Toll like receptors
(TLR) induisent l’expression de FT au niveau des cellules
endothéliales et des cellules de l’inflammation comme les
monocytes, aboutissant à une génération très importante
de thrombine. L’activation ou l’apoptose cellulaire (mono-
cytes, plaquettes, cellules endothéliales) associée à la
réponse inflammatoire est responsable de la formation de
microparticules riches en FT et en phospholipides chargés
négativement comme les phosphatidylsérines indispensa-
bles à la formation des complexes enzymatiques de la
cascade de la coagulation. Les acteurs de la coagulation
ont un rôle pro-inflammatoire via les protease activating
receptors (PAR) : les facteurs de la coagulation activés
activent les PAR de différents types cellulaires (cellules
endothéliales, monocytes…). Ces récepteurs une fois acti-
vés ont un effet pro-inflammatoire et procoagulant direct
et indirect via l’expression de cytokines : ils sont respon-
sables d’une expression accrue de molécules d’adhésion
(ICAM-1, VCAM-1, E-sélectine) à la surface des cellules
endothéliales, favorisant leur interaction avec les cellules
de l’inflammation (cellules mononucléées, polynucléaires,
plaquettes) et leur activation. Ils peuvent induire la forma-
tion de microparticules riches en FT et en phosphatidylsé-
rines à partir de différents types cellulaires dont les pla-
quettes, les monocytes et les cellules endothéliales. Enfin,
l’activation des PAR est associée à la production de cyto-
kines pro-inflammatoires, comme TNFα, IL-1 et IL-6.
Ces cytokines entretiennent la réponse inflammatoire et
l’activation de la coagulation par l’expression de molécu-
les d’adhésion, l’activation des cellules endothéliales et la
formation de microparticules. Les cytokines pro-
inflammatoires et les facteurs de la coagulation ont donc
une action synergique locale sur la réponse inflammatoire.
Dans le paludisme, la séquestration des hématies parasi-
tées au niveau des capillaires est associée à une activation
des cellules endothéliales : l’expression membranaire par
ces hématies de molécules, les Plasmodium falciparum
erythrocyte membrane proteins (PfEMP), permet l’adhé-
sion à l’endothélium et l’activation des cellules endothé-
liales [13]. Les hématies parasitées sont capables d’activer
aussi les plaquettes grâce à la sécrétion de différentes
substances pro-agrégantes comme l’adénosine diphos-
phate (ADP) [9]. L’activation des cellules endothéliales
et des plaquettes constitue une étape indispensable pour
l’hémostase primaire, ainsi que pour l’initiation de la coa-
gulation grâce à l’expression par les cellules endothéliales
activées de FT. L’hémolyse des hématies parasitées per-
met l’extériorisation en grande quantité de phosphatidyl-
sérines [4], phospholipides intervenant dans l’amplifica-
tion de la cascade de la coagulation [13]. Le résultat est
une génération très importante de thrombine et la forma-
tion de fibrine dans la microcirculation. Comme dans le
sepsis, les facteurs de la coagulation activés activent les
PAR des cellules endothéliales et des monocytes, ce qui
aboutit à une amplification des réponses inflammatoire et
procoagulante via un cycle d’entretien entre les deux
réponses. D’autres intervenants (complexes immuns,
voie contact, complément, polynucléaires) et certaines
substances contenues dans les hématies parasitées (hémo-
zoïne, glycosylphosphatidylinositol, hème oxydé) sont
capables d’activer aussi la réponse inflammatoire et
d’entretenir le cycle inflammation-coagulation.
Les désordres de l’hémostase semblent spécifiques à
P. falciparum [8], alors que la réponse inflammatoire
décrite plus haut est retrouvée aussi bien dans le palu-
disme à P. falciparum qu’àP. vivax. Par exemple, la
thrombopénie est observée dans les deux formes, mais
elle est de nature immunologique dans l’infection à
P. vivax alors qu’elle est secondaire à une consommation
dans l’infection à P. falciparum. La différence majeure est
l’expression du FT, retrouvée uniquement dans l’infection
àP. falciparum [8]. Cette expression de FT, déjà mise en
évidence dans le sepsis bactérien et responsable de
l’entretien du cycle inflammation-coagulation, contribue-
rait à l’interaction entre endothélium et éléments sanguins
circulants (polynucléaires neutrophiles, monocytes, pla-
quettes), entraînant des lésions endothéliales, une aug-
mentation de la perméabilité vasculaire, une vésiculation
et une apoptose cellulaire. Ce cycle a sans doute un rôle
non négligeable dans la défaillance multiviscérale obser-
vée dans les formes graves de paludisme. Il est très ampli-
fié au niveau du cerveau, dû à l’absence de thrombomo-
duline, inhibiteur de la thrombine, et pourrait expliquer les
formes graves cérébrales observées dans le neuropalu-
disme où il a été mis en évidence une accumulation de
monocytes et de plaquettes, la présence de microparticules
et une apoptose des cellules endothéliales au niveau des
vaisseaux cérébraux [8].
La gangrène
La gangrène associée à un paludisme sévère à P. falcipa-
rum a surtout été décrite en zone endémique (13 cas endé-
miques et 5 touristes) et reste un événement peu fréquent
[4-6]. Elle peut être observée précocement (10 des cas
décrits dont notre patient) ou se développer quelques
jours après la prise en charge et le début du traitement
(à J3 pour les 8 autres cas décrits), comme d’autres com-
plications associées au paludisme sévère [12]. La survenue
d’une gangrène au cours d’un paludisme est multifacto-
rielle [4, 5] et la CIVD est un de ces facteurs : dans la
majorité des cas de gangrène décrits [4-6], il est retrouvé
une CIVD associée (au moins 14 cas sur 18). La CIVD
chez les cas décrits ne semble pas être majoritairement
secondaire à une infection bactérienne [3, 4, 11], considérée
comme la principale cause de CIVD dans le paludisme [2].
Gangre
`ne, CIVD et paludisme
Ann Biol Clin, vol. 67, n
o
5, septembre-octobre 2009 571
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 04/06/2017.

La séquestration des hématies au niveau de la microcircu-
lation et le traitement par catécholamines nécessaire au
maintien d’une hémodynamique correcte sont aussi des
facteurs favorisants [4, 5, 14]. La survenue d’une gangrène
a nécessité une amputation dans presque la moitié des cas
décrits (6 amputations et 7 résolutions). L’amputation
semble plus fréquente dans les cas importés (5 amputations
et une résolution) que dans les cas endémiques (2 amputa-
tions et 6 résolutions), ce qui concorde avec la notion que
l’ethnicité serait un facteur pronostique [15].
Conclusion
Le diagnostic précoce de l’infection, la mise en place
rapide du traitement antipaludéen et la prise en charge
en réanimation [16] permettent un meilleur pronostic
pour les patients atteints de paludisme sévère, mais la
mortalité reste importante malgré toutes ces mesures [1,
12]. La prise en charge d’un paludisme sévère à Plasmo-
dium falciparum est bien établie [2], mais les options thé-
rapeutiques efficaces pour les patients qui présentent un
paludisme associé à une CIVD sont limitées, et il n’existe
pas de consensus sur la prise en charge de telles compli-
cations. L’héparine est utilisée empiriquement comme
dans toute CIVD avec manifestations ischémiques mais
ne modifie pas le pronostic vital [2]. Des traitements
thrombolytiques comme la streptokinase ont été utilisés,
mais leur usage ne peut être recommandé du fait du risque
hémorragique élevé chez des patients thrombopéniques
[2]. De nombreuses autres stratégies thérapeutiques ont
été testées [2-4, 11], mais aucune n’a démontré une réelle
efficacité. La compréhension des mécanismes de survenue
d’une CIVD dans le paludisme et plus généralement dans
le sepsis [11, 12] permet d’envisager de nouvelles cibles
thérapeutiques comme celles agissant sur la voie du FT
[17, 18] ou celles modulant la fonction endothéliale
[19], afin de limiter l’apoptose endothéliale et de freiner
l’activation de la coagulation et de l’inflammation respon-
sables de la défaillance multiviscérale qui met en jeu le
pronostic vital.
Références
1. Saïssy JM, Rouvin B, Koulmann P. Severe malaria in intensive care
units in 2003. Med Trop 2003 ; 63 : 258-66.
2. WHO guidelines for the treatment of malaria. World Health Organi-
zation, 2006.
3. Bruneel F, Hocqueloux L, Alberti C, Wolff M, Chevret S, Bedos JP,
et al. The clinical spectrum of severe imported falciparum malaria in the
intensive care unit: report of 188 cases in adults. Am J Respir Crit Care
Med 2003 ; 167 : 684-9.
4. Liechti ME, Zumsteg V, Hatz CF, Herren T. Plasmodium falciparum
cerebral malaria complicated by disseminated intravascular coagulation
and symmetrical peripheral gangrene: case report and review. Eur J Clin
Microbiol Infect Dis 2003 ; 22 : 551-4.
5. Helbok R, Lackner P, Schmutzhard E. Severe Plasmodium falcipa-
rum malaria with peripheral gangrene. Lancet Infect Dis 2008 ; 8 :
400.
6. Thanachartwet V, Krudsood S, Wilairatana P, Phumratanaprapin W,
Silachamroon U, Looareesuwan S. Peripheral gangrene in patients with
severe falciparum malaria: report of 3 cases. Korean J Parasitol 2006 ;
44 : 139-43.
7. Toh CH, Hoots WK. The scoring system of the Scientific and Stan-
dardisation Committee on Disseminated Intravascular Coagulation of
the International Society on Thrombosis and Haemostasis: a 5-year
overview. J Thromb Haemost 2007 ; 5 : 604-6.
8. Francischetti IMB. Does activation of the blood coagulation cascade
have a role in malaria pathogenesis? Trends Parasitol 2008 ; 24 :
258-63.
9. Ghosh K, Shetty S. Blood coagulation in falciparum malaria: a
review. Parasitol Res 2008 ; 102 : 571-6.
10. Lerolle N, Borgel D, Diehl JL. Coagulation intravasculaire dissémi-
née en réanimation : physiopathologie, épidémiologie, diagnostic et
prise en charge thérapeutique. Hématologie 2007 ; 13 : 409-20.
11. Kendrick BJ, Gray AG, Pickworth A, Watters MPR. Drotrecogin
alfa (activated) in severe falciparum malaria. Anaesthesia 2006 ; 61 :
899-902.
12. Hemmer CJ, Vogt A, Unverricht M, Krause R, Lademann M, Rei-
singer EC. Malaria and bacterial sepsis: similar mechanisms of endothe-
lial apoptosis and its prevention in vitro.Crit Care Med 2008 ; 36 :
2562-8.
13. Francischetti IMB, Seydel KB, Monteiro RQ, Whitten RO, Erexson
CR, Noronha ALL, et al. Plasmodium falciparum-infected erythrocytes
induce tissue factor expression in endothelial cells and support the
assembly of multimolecular coagulation complexes. J Thromb Haemost
2007 ; 5 : 155-65.
14. Hayes MA, Yau EH, Hinds CJ, Watson JD. Symmetrical peripheral
gangrene: association with noradrenaline administration. Intensive Care
Med 1992 ; 18 : 433-6.
15. Phillips A, Bassett P, Zeki S, Newman S, Pasvol G. Risk factors for
severe disease in adults with falciparum malaria. Clin Infect Dis 2009 ;
48 : 871-8.
16. Schwake L, Streit JP, Edler L, Encke J, Stremmel W, Junghanss T.
Early treatment of imported falciparum malaria in the intermediate and
intensive care unit setting: an 8-year single-center retrospective study.
Crit Care 2008 ; 12 : R22.
17. Ruf W. Protease-activated receptor signaling in the regulation of
inflammation. Crit Care Med 2004 ; 32 : S287-92.
18. Carraway MS, Welty-Wolf KE, Miller DL, Ortel TL, Idell S, Ghio
AJ, et al. Blockade of tissue factor: treatment for organ injury in esta-
blished sepsis. Am J Respir Crit Care Med 2003 ; 167 : 1200-9.
19. Barthel SR, Gavino JD, Descheny L, Dimitroff CJ. Targeting selec-
tins and selectin ligands in inflammation and cancer. Expert Opin Ther
Targets 2007 ; 11 : 1473-91.
pratique quotidienne
572 Ann Biol Clin, vol. 67, n
o
5, septembre-octobre 2009
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 04/06/2017.
1
/
4
100%