+ k - La Fed

Stage de Pré-Rentrée 2013
UE 1 – Enzymologie
1
Diaporama réalisé par les tuteurs de La Féd’

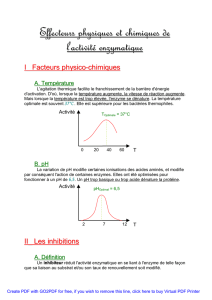
I - L’association PL
En biochimie, un ligand est une molécule capable de se fixer sur une protéine
avec une certaine affinité.
Protéine
(P)
Ligand (L)
Complexe
(PL)
L peut être : un ion, une petite molécule, une protéine plus petite, etc…
L’interaction est en général réversible.
Elle fait intervenir des liaisons faibles non covalentes.
Elle peut être michaëlienne ou allostérique.
Par soucis de simplification, nous ne traiterons aujourd’hui que la michaëlienne.

P + L PL
k1
k-1
Exprimons :
• La vitesse d’apparition du complexe PL : v1 = k1 x [P] x [L]
• La vitesse de disparition du complexe PL : v-1 = k-1 x [PL]
A l’équilibre, il se forme autant de complexes PL qu’il en disparait
Alors on peut écrire : v1 = v-1
D’où l’égalité : k1 x [P]eq x [L]eq = k-1 x [PL]eq
I - L’association PL
Nous allons modéliser cette interaction

Définition de la constante de dissociation KD
On définit KD, la constante de dissociation.
Il s’agit d’une concentration (unité mol.L-1)
KD est un rapport de constantes de vitesse :
Nous avions écrit : k1 x [P]eq x [L]eq = k-1 x [PL]eq
Nous en déduisons :
k-1
k1
KD =
[P]eq x [L]eq
[PL]eq
KD =
I - L’association PL

Définition de la saturation Y
On définit Y, la fraction de saturation de la protéine.
Il s’agit d’une valeur entre 0 et 1, sans dimension.
NB : La somme ([P] + [PL]) peut être notée P0
Cherchons un moyen de déterminer Y en fonction de Leq et de Kd
I - L’association PL
[PL]
[P] + [PL]
Y =
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
1
/
28
100%