Consulter le livret de la rencontre

Fondation pour l'aide à la recherche
sur la sclérose en plaques
Encourager le dialogue direct entre les chercheurs et les malades
Une journée naonale, organisée à deux dates, l’une en Ile de France le
4 novembre 2011, et l’autre le 25 novembre 2011 dans plusieurs sites de
recherche en région, va ouvrir les laboratoires de l’Inserm ayant reçu le souen
de la Fondaon Arsep, aux personnes malades et leur famille. L’ objecf est
simple : faciliter la rencontre et le contact direct entre les chercheurs qui
travaillent sur la sclérose en plaques et les malades.
Pourquoi une telle iniave ? Parce que les malades ont besoin d’être informés
sur l’évoluon de la recherche. Leurs raisons sont doublement légimes : la
recherche représente pour eux l’espoir de bénécier de thérapies ecaces,
et nombre d’entre eux se sont mobilisés dans des associaons pour soutenir
la recherche sur leur maladie. C’est ainsi que la Fondaon Arsep, grâce aux
malades et à leurs donateurs, a réuni des fonds pour nancer les équipes de
recherche ainsi que les jeunes chercheurs, contribuant ainsi à assurer la relève
de la recherche sur la maladie, et, au delà, pour informer le public en général.
Ce lien entre les malades et la recherche est très important. L’Inserm a
reconnu le rôle essenel que jouent les associaons et les fondaons issues de
l’engagement des malades en établissant un groupe permanent de réexion
avec les Associaons de malades (GRAM).
Construire un espace de savoir partagé avec les malades, reconnu par tous et
d’où pourraient émerger des formes de partenariat nouvelles et enrichissantes
est l’un des objecfs prioritaires de l’Inserm ; cee journée de rencontre
chercheurs-paents en est la première brique.
Les chercheurs ont préparé leur présentaon, les délégués de la Fondaon
ARSEP et les chargés de communicaon régionaux ont organisé l’accueil, la
mission Inserm Associaons et le siège de la Fondaon ARSEP ont coordonné
l’ensemble.
Cee journée est celle du dialogue, n’hésitez pas à poser vos quesons, toutes
vos quesons !
La Fondaon Arsep La Mission Inserm Associaons
Une journée dans les laboratoires
de recherche autour de la sclérose en plaques

30 ans). Il existe, beaucoup plus rarement, des cas de SEP chez l’enfant et l’adolescent.
Les signes cliniques sont soit isolés, soit associés entre eux. Ils surviennent en quelques heures ou quelques
jours pour disparaître totalement ou partiellement en quelques semaines. Il s’agit d’une poussée.
Le diagnostic
Lors des premiers troubles, il est souvent difcile d’évoquer le diagnostic de SEP. En revanche, la récurrence
des signes neurologiques, témoin d’une dissémination dans le temps et dans l’espace permet de poser le
diagnostic.
L’examen clinique est primordial car il permet au neurologue d’exclure une autre affection et de conrmer la
souffrance du système nerveux central. Des examens complémentaires, tels que l’IRM, seront proposés. Le
diagnostic de SEP sera établi avec certitude, par l’analyse combinée des données cliniques et des examens
complémentaires.
Les différentes formes cliniques et leur évolution
Il existe plusieurs formes cliniques de la maladie :
les formes rémittentes qui évoluent par poussées
et les formes progressives évoluant sans
poussées (formes secondairement progressive
et formes progressives d’emblée).
Dans 85% des cas, la SEP débute par une
forme à poussées. Ces crises répétées seront
espacées de façon variable dans le temps.
Certains patients vont ensuite évoluer vers une
forme secondairement progressive, lorsque
les atteintes neurologiques vont s’aggraver
progressivement.
Dans les formes progressives d’emblée, qui débutent généralement plus tardivement (après 40 ans), il
y a rarement des poussées surajoutées au début de la maladie et les signes neurologiques s’aggravent
progressivement.
L’évolution et l’expression de la maladie sont extrêmement imprévisibles et variables. Il n’existe pas de
marqueurs prédictifs du handicap. Néanmoins, 20 à 40% des patients ne présentent pas de handicap dans
leur vie quotidienne après 15 à 20 ans d’évolution (SEP bénigne).
Les traitements
Malgré les progrès thérapeutiques accomplis ces dernières années, il n’existe pas encore de traitement pour
guérir la SEP. Néanmoins, certains médicaments ralentissent l’évolution de la maladie, d’autres permettent
de soulager les symptômes associés (douleur, fatigue, incontinence urinaire, ...) :
• Le traitement des poussées a pour but de diminuer l’intensité et la durée des signes neurologiques.
Seuls les corticoïdes donnés en perfusion ont prouvé leur efcacité.
• Les traitements symptomatiques ont pour objectif de réduire la gêne quotidienne provoquée par les
symptômes cliniques. Ils sont proposés pour améliorer la qualité de vie du malade.
• Les traitements de fond sont pris sur le long cours. Ils diminuent la fréquence des poussées et réduisent
la progression du handicap. Ce sont des immunomodulateurs (qui limitent l’intensité de la réponse
inammatoire) ou des immunosuppresseurs (qui agissent directement sur les cellules immunitaires en
bloquant la réponse immunitaire). Ces traitements sont principalement destinés aux patients ayant des
formes rémittentes ou secondairement progressives avec poussées surajoutées.
Qu’est ce que
la Sclérose en Plaques (SEP) ?
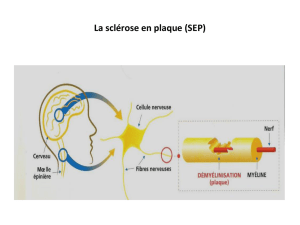
La SEP est une maladie du système nerveux central (SNC), qui
comprend le cerveau et la moelle épinière. Il est composé de
neurones, qui véhiculent l’information entre le cerveau et le reste
du corps. Ces neurones sont composés d’un corps cellulaire et
d’un prolongement, l’axone, entouré d’une gaine protectrice, la
myéline, qui a pour but de nourrir et de protéger le neurone et de
permettre une conduction rapide de l’information.
Dans la SEP, une réaction inammatoire attaque la gaine de
myéline. C’est la démyélinisation. Elle entraîne des perturbations
dans la conduction de l’information élaborée par le cerveau et
transmise aux différentes parties du corps, expliquant les signes
de la maladie. Parallèlement à l’attaque de la myéline, une
souffrance précoce de l’axone apparaît.
La plupart du temps, l’inammation disparaît et des mécanismes
de réparation permettent la restauration, plus ou moins complète,
de la myéline conduisant à une régression partielle ou complète
des symptômes. C’est la remyélinisation.
Malheureusement, au cours de l’évolution de la maladie ou
lors d’attaques inammatoires importantes, les mécanismes de
remyélinisation sont insufsants et des signes neurologiques
persistants s’installent. Une souffrance peut également coexister.
Une maladie auto-immune
La SEP est considérée comme une maladie auto-
immune. Normalement, les lymphocytes T (cellules du
système immunitaire) ne franchissent pas la barrière
qui sépare le sang du cerveau (barrière hémato-
encéphalique). Cependant, dans la SEP, le lymphocyte
«normal au repos», présent dans le sang, se transforme
en lymphocyte «activé agressif».
Cette transformation lui permet d’entrer dans le SNC de
proliférer, de se diviser, provoquant ainsi une réaction
inammatoire qui aboutit à la destruction de la myéline
et de l’axone.
Les symptômes
Les symptômes varient beaucoup d’une personne à l’autre
et d’un moment à l’autre chez une même personne. Ils sont
multiples et variés. Les signes observés au début de la maladie
sont souvent transitoires et très variés car ils dépendent de la
localisation des plaques dans le cerveau ou la moelle épinière
rendant le diagnostic difcile.
Ces symptômes sont évocateurs s’ils surviennent chez un
adulte jeune (dans 2/3 des cas, la maladie débute entre 20 et
Plusieurs formes cliniques
Rémittentes RR
Secondairement progressives
SP
Progressives primaires PP
SANG PÉRIPHÉRIQUE SYSTÈME NERVEUX CENTRAL
Environnement
Génétique
La sclérose en plaques (SEP)
Comment, pourquoi ?
Barrière sang - cerveau
Cellules
immunitaires
Activation des
lymphocytes
Libération de molécules
toxiques
Démyélinisation
Perte axonale
Amplification des lymphocytes actifs
Les troubles dans la SEP
• moteurs : faiblesse musculaire.
• oculaires : de l’acuité visuelle d’un œil, vision
double...
• sensitifs : perte de la sensibilité
(engourdissements, fourmillements), brûlures.
• troubles de l’équilibre,
• troubles urinaires ou sexuels,
• etc.
Démyélinisation dans la SEP
Transmission altérée (poussée)
Myéline endommagée
(démyélinisation)
Transmission de message le long de l’axone
Neurone normal
Corps cellulaire Myéline Axone
Plus de transmission (progression)
Destruction de la
bre nerveuse
Atteinte de la l’axone dans la SEP

Qu’est-ce que
la recherche médicale?
Une dénition ?
La recherche scientique dénit l’ensemble des actions entreprises en
vue de produire et de développer la connaissance, pour étudier, explorer
et comprendre. C’est avant tout un travail d’équipe qui se déroule dans
des organismes de recherche publics, (Inserm, CNRS, universités,
hôpitaux) ou privés (entreprises).
Essayons de dénir la recherche médicale : quel en est le cadre, les
domaines qu’elle aborde, qui sont ses acteurs et à quels principes
obéissent-ils ?
La chaîne de la recherche en sciences du vivant: de la molécule à l’homme
• Etape 1 - La recherche fondamentale
Absolument nécessaire, son objectif principal est de faire avancer les connaissances et
pas directement de soigner. La quête du «comment ça marche?» contribue à l’élaboration
de nouveaux médicaments et de nouvelles pistes de recherche, ou de nouveaux outils
permettant de détecter plus tôt une maladie. Elle avance grâce à la curiosité et à la
créativité des chercheurs: les cellules ne se regardent qu’au microscope; quant aux
molécules, aux protéines et aux gènes ils ne se laissent deviner qu’en grande quantité
au fond d’un tube.
• Etape 2 - La recherche pré-clinique
Après la découverte d’une molécule pouvant avoir un potentiel effet diagnostique ou thérapeutique, il est
nécessaire de tester son impact sur l’organisme entier et de vérier les effets secondaires. Cette étape
préalable réalisée sur des animaux de laboratoire est obligatoire avant de tester un éventuel traitement chez
l’homme, d’où son nom de recherche pré-clinique.
• Etape 3 - La recherche clinique
Cette étape permet de mettre en place un protocole à visée diagnostique (des machines IRM plus performantes)
ou thérapeutiques (des médicaments ciblés, donc mieux tolérés et plus efcaces). Les essais cliniques se
déroulent dans les hôpitaux, en quatre phases, évaluant successivement la sécurité du traitement, la dose
optimale, l’efcacité du nouveau traitement par rapport à un traitement de référence déjà existant et enn
l’observation des interactions entre médicaments (plus d’informations sur www.notre-recherche-clinique.fr).
La recherche est aussi un domaine de curiosité et de questionnement
• La démarche scientique c’est :
- poser une question
- énoncer une hypothèse qui permettrait de l’expliquer
- proposer un protocole et des modèles expérimentaux sur lequel le tester. En général on part du modèle
le plus simple (la cellule) vers le plus compliqué (l’organisme entier). Souvent les chercheurs utilisent des
lignées cellulaires comme modèle simplié d’une cellule spécialisée
- tester tous les paramètres, observer et analyser les résultats
- recommencer, reformuler, générer d’autres expériences jusqu’à obtenir des résultats reproductibles
- utiliser les tests statistiques pour vérier la probabilité que la conclusion a d’être juste
• Les acteurs et les métiers de la recherche : un travail d’équipe
Les chercheurs statutaires, docteurs en sciences, médecins ou non, portent les projets. Ils ont pour mission
de trouver les moyens humains, techniques et matériels, en répondant à des appels d’offres de l’état, de
l’industrie, des associations ou des fondations. Ils expertisent les projets de leurs pairs dans leur spécialité,
forment la relève, coordonnent les membres de leur équipe : chercheurs, ingénieurs, techniciens et étudiants,
en lien avec les administratifs.
• Le temps de la recherche et le temps des malades: pourquoi est-ce si long ?
Chaque étape en recherche nécessite des délais qui dépendent de la complexité de l’étude. Transposer
rapidement les résultats obtenus chez l’animal à des espoirs de traitement chez l’homme est légitime pour
les patients, mais le passage vers la recherche clinique jusqu’à l’accord des autorités de santé est long et
indispensable. L’émergence de la recherche translationnelle devrait aider à raccourcir ce temps.
Un domaine de collaboration, de synergie et de communication
Pour faire avancer la recherche, les chercheurs et cliniciens doivent collaborer entre eux, à l’échelle
mondiale, publier des articles scientiques et partager les informations lors de congrès spécialisés. Pour
avancer de manière encore plus ciblée, ils doivent aussi collaborer avec les malades et les associations qui
les représentent.
La recherche translationnelle
ou de transfert assure le lien entre les découvertes les plus récentes de la recherche fondamentale
ou pré-clinique et la recherche clinique. Elle est bidirectionnelle, de la recherche fondamentale au
patient, et inversement.
Quelques grands domaines de recherche impliqués dans la SEP.
- La biologie cellulaire s’intéresse à l’étude de des quelques 50 000 milliards de cellules du corps humain.
- La génétique caractérise dans les cellules les gènes présents, incomplets, en double ou non fonctionnels
et cherche surtout à comprendre pourquoi ces modications sont souvent associées à une maladie.
- L’épidémiologie étudie une maladie dans une population donnée et cherche ses causes quelles soient
biologiques, médicales, environnementales ou autres, pour mieux la prendre en charge.
- La physiologie analyse la communication entre les organes. Le corps humain est un système intégré
très sophistiqué : les cellules sont regroupées en tissus qui vont composer les organes.
- L’immunologie étudie le système immunitaire qui doit être parfaitement régulé. Certaines cellules sont
là pour maintenir l’intégrité de l’organisme et le protéger des agressions. Parfois ce système se dérègle
et l’organisme détruit ses propres cellules comme dans les maladies auto-immunes, la SEP en est un
exemple.
- La neurobiologie et les domaines de recherche qui en dérivent comme la neurophysiologie, vont
s’intéresser au développement des cellules du cerveau. Ils peuvent aussi, dans le cas de la SEP, chercher
à identier les signaux qui régulent la fabrication de la myéline, qui normalement protège et permet aux
neurones de communiquer.
- L’endocrinologie étudie comment les hormones sont produites par un tissu et véhiculées par le sang
pour inuencer le développement d’un autre tissu.
Ces exemples illustrent le type de questions auxquelles répond la recherche et soulignent le caractère
imprévisible en termes de résultats et de temps nécessaire à leur obtention.
Conclusion
La recherche en marche est le lien entre ce qui est déjà connu et ce qui ne l’est
pas encore. Les malades ont une expérience à partager. Ce regard nouveau au
sein de la communauté des chercheurs est un élément structurant pour les études
qu’ils mènent, un regard qui pourrait orienter différemment leurs recherches.

Résumés des projets de recherche
des chercheurs Inserm soutenus
nancièrement par la fondaon
ARSEP
RÉGION MIDI-PYRÉNÉES - TOULOUSE
David Brassat - Intérêt des
biomarqueurs liés à l’ARN dans
la réponse thérapeutique au
Natalizumab chez les patients
atteints de SEP.
La sclérose en plaques est une maladie qui peut
entrainer un handicap sévère. Heureusement
la recherche fait des progrès constants dans ce
domaine. Cependant, il reste des améliorations
possibles notamment concernant le choix du
meilleur traitement à adopter. En effet, les
médicaments actifs dans la sclérose en plaques
ont de plus en plus un mécanisme d’action ciblé,
c’est-à-dire qu’ils vont agir sur une molécule, une
action spécique à la maladie.
Or les critères actuels ne tiennent pas compte
de ces aspects, puisque le choix du traitement
repose uniquement sur des données cliniques et
radiologiques.
Notre but est donc d’identier des marqueurs
spéciques, an de prendre en compte non
seulement les critères clinique et radiologique mais
aussi le mécanisme d’action que le traitement doit
aller cibler. Pour cela, à l’aide d’une prise de sang
faite juste avant la prescription, nous cherchons
à déterminer quel traitement est le mieux adapté
an d’optimiser la prise en charge thérapeutique.
Jean-Charles Guery - Importance
du récepteur aux oestrogènes dans
les lymphocytes T dans l’effet anti-
inammatoire des oestrogènes,
sur un modèle animal de SEP.
Des phases de rémission sont fréquemment
observées dans la SEP chez les femmes
enceintes, suggérant que les hormones sexuelles
et plus particulièrement les œstrogènes pourraient
exercer un effet bénéque sur la maladie. Les
oestrogènes agissent grâce à un récepteur,
molécule située dans les tissus. Dans un modèle
animal de SEP, l’administration d’œstrogènes
bloque le développement de la maladie. Cette
observation valide l’hypothèse d’un effet bénéque
de ces hormones.
Par ailleurs, l’induction de la maladie sur un autre
modèle murin ne possédant plus ce récepteur (donc
plus aucun effet des œstrogènes n’est possible)
montre que l’administration d’œstrogènes ne
protège plus de la maladie soulignant le rôle capital
du récepteur. Avec l’aide de ces deux modèles,
notre projet est de comprendre quels sont les
mécanismes d’action qui aboutissent à la réponse
inammatoire spécique dans le système nerveux
central et au développement de la maladie.
L’objectif est de conrmer le rôle protecteur
des hormones sexuelles féminines qui pourrait
servir de base au développement de nouvelles
stratégies thérapeutiques dans le traitement de
cette maladie auto-immune.
Abdelhadi Saoudi - Comprendre
les mécanismes d’action de
VAV1 dans les fonctions des
lymphocytes T et la susceptibilité
à la sclérose en plaques.
Les facteurs génétiques qui
prédisposent à la sclérose en plaques sont mal
connus. Leur recherche est difcile du fait des
différences génétiques des populations humaines
et du rôle que joue l’environnement sur ces
facteurs. Les études génétiques sont plus faciles
chez des animaux conditionnés pour développer
une maladie qui reproduit la sclérose en plaques,
du fait de l’utilisation de lignées pures de souris
et de rats (tous les animaux d’une lignée sont
génétiquement identiques) et du contrôle de
l’environnement.
Grace à ces études menées chez le rat, nous
avons découvert que le gène Vav1 détermine la
sensibilité à développer cette maladie et contrôle
le fonctionnement d’une population de cellules
spécialisées dans la régulation du système
immunitaire. Ce gène est associé chez l’Homme
à la susceptibilité à développer une sclérose en
plaques.
Notre projet vise à élucider dans des modèles
animaux les mécanismes par lesquels Vav1
contrôle le fonctionnement du système immunitaire
et le développement de la SEP. Les connaissances
ainsi acquises sur les mécanismes de la sclérose
en plaques pourraient à terme déboucher sur de
nouveaux modes de diagnostic et de traitements
de cette maladie.
Roland Liblau - Rôle des cytokines
dans un nouveau modèle animal de
cellules T « tueuses » médiées par la
neuroinammation.
Il est hautement vraisemblable que
la SEP résulte d’une attaque auto-immune du
système nerveux central et qui est à l’origine de
handicap.
Les acteurs principaux d’une telle attaque sont les
lymphocytes T, classés en 2 sous populations :
les lymphocytes T auxiliaires et les lymphocytes T
cytotoxiques. Les premiers sont largement
étudiés grâce aux modèles animaux de la SEP
actuellement disponibles. Cette connaissance
a guidé le choix des cibles thérapeutiques.
Cependant, il existe des différences entre le
modèle animal et la maladie humaine. Alors que
dans le modèle animal ce sont les lymphocytes T
auxiliaires qui sont responsables de l’attaque du
système nerveux, dans l’affection humaine, les
lymphocytes T cytotoxiques prédominent dans le
cerveau atteint et contribuent très probablement
aux dégâts tissulaires, sources de handicap.
Notre hypothèse est donc que la transposition des
recherches sur la SEP à la prise en charge des
patients atteints de SEP a partiellement échoué
parce que nous devons d’abord comprendre
comment les lymphocytes T cytotoxiques dirigés
contre le système nerveux central sont régulés.
Nous proposons donc d’étudier le rôle des
cytokines impliquées dans
l’inammation du cerveau
induite par les cellules T
cytotoxiques.
Daniel Gonzales Dunia - Analyse
des mécanismes de la destruction
neuronale et axonale provoquée par
les lymphocytes T cytotoxiques :
une cible alternative pour l’immuno-
thérapie dans la sclérose en plaques ?
La réponse inammatoire auto-immune qui caractérise la SEP conduit à des atteintes des neurones
et des axones. Ces atteintes participent aux décits neurologiques et aux défauts de remyélinisation
chez les patients. Les acteurs immunologiques impliqués sont mal connus, mais des résultats récents
suggèrent que les lymphocytes T cytotoxiques, ou cellules tueuses, pourraient jouer un rôle majeur. Or,
la capacité de ces cellules à tuer les neurones n’a jamais été démontrée formellement. Ici, nous utilisons
des modèles animaux où certains antigènes peuvent être exprimés spéciquement dans les neurones,
combinés avec des modèles d’inammation faisant intervenir les lymphocytes T cytotoxiques. Nous
réaliserons des cultures de neurones à partir de ces modèles et nous analyserons les modalités de leur
attaque par diverses sous-populations de lymphocytes T cytotoxiques.
Notre objectif est de mieux comprendre les mécanismes à l’œuvre dans ces atteintes, permettant
ensuite de rechercher des moyens d’empêcher la destruction neuronale. Ceci pourrait permettre
d’identier de nouvelles approches thérapeutiques pour un meilleur contrôle des lésions axonales et
neuronales observées chez les patients atteints de SEP.
Lymphocytes T

Eric Thouvenot - Recherche de marqueurs de sclérose en plaques
rémittente après un premier évènement démyélinisant par analyse
protéomique quantitative du liquide céphalorachidien.
La recherche de biomarqueurs de la SEP (des protéines qui sont
caractéristiques de la maladie) est un enjeu majeur pour établir un
diagnostic précoce de la maladie et offrir une meilleure prise en charge
des patients. Le liquide céphalorachidien (LCR) est un uide biologique de choix pour la découverte
de molécules biologiques spéciques de la SEP, car il est en contact avec le cerveau et la moelle
épinière. Le programme proposé a pour objectif la recherche de biomarqueurs précoces grâce à la
protéomique, approche récente et puissant d’analyse de protéines dans un échantillon biologique,
comme le sang ou le LCR. Nous allons utiliser cette approche pour différencier parmi les patients ayant
présenté des signes évocateurs de SEP, ceux qui ont un risque élevé de développer effectivement une
SEP dans l’année. Cette étude permettra de traiter ces patients de manière très précoce et adaptée,
an de retarder l’apparition d’un handicap neurologique.
RÉGION LANGUEDOC ROUSSILLON - MONTPELLIER
Klaus Petry - Identication et
caractérisation sur des cellules
endothéliales de nouvelles cibles
moléculaires à l’origine des
événements neuroinammatoires
dans le modèle
expérimental de SEP.
Nos recherches visent à
caractériser et suivre in vivo,
c’est-à-dire dans le cerveau,
les événements associés au
processus neuroinammatoire
observé dans la SEP. Grace à une approche
de décryptage, nommée «phage-display»,
nous avons isolé 81 nouvelles molécules qui
permettent de dénir très tôt les modications que
subit la barrière hémato-encéphalique. Il s’agit de
caractériser ces molécules et d’identier celles
avec lesquelles elles se lient, les « molécules
cibles » Notre démarche comporte plusieurs
étapes: dans un 1er temps nous concentrons nos
expériences sur une lignée de cellules cérébrales,
la lignée hCMEC/D3. Nous analysons les gènes
présents par des études de biologie moléculaire
et les protéines présentes par des études de
protéomique. Dans un 2ème temps nous étudierons
ces interactions dans un modèle plus complexe,
le modèle animal de la SEP. La perspective de ce
projet est de dénir des stratégies thérapeutiques
spéciques pour bloquer l’expression des
molécules cibles et ainsi prévenir la rupture de
la barrière hématoencéphalique et nalement
interrompre les processus neuroinammatoires
de la SEP.
RÉGION AQUITAINE - BORDEAUX
Serge Nataf - Analyse de
l’inammation dans les méninges
médullaires chez les patients
présentant une forme progressive
de SEP.
Dans les formes les plus sévères
de SEP, la moelle épinière est très souvent atteinte
par un processus inammatoire diffus. Comparé
au cerveau, très peu d’études ont analysé la
réaction inammatoire dans la moelle épinière de
patients atteints de SEP.
Nous avons récemment montré que chez les
patients, l’inammation des méninges est
prépondérante dans la molle épinière et qu’elle
est corrélée à l’étendue des lésions neuronales.
Ce projet vise à mieux caractériser l’inammation
méningée dans la moelle épinière des patients.
Par ailleurs, il doit permettre l’identication de
molécules qui sont impliquées dans l’atteinte
neuronale potentiellement induite par cette
inammation méningée.
Notre objectif est donc de mieux comprendre les
mécanismes de l’inammation méningée pour, à
terme, pouvoir la contrer.
RÉGION RHÔNE-ALPES - LYON
Jean-François Ghersi-Egea -
Déterminants moléculaires de
la migration des lymphocytes T
à travers l’interface sang-liquide
céphalo-rachidien dans un contexte
physiologique et neuroinammatoire.
Pour inltrer le système nerveux central, les
cellules immunes circulant dans le sang doivent
franchir des interfaces cellulaires, sorte de
barrières de cellules qui protègent le cerveau.
Les plexus choroïdes forment l’une de ces
interfaces, localisés entre le sang et le liquide
céphalo-rachidien (LCR) qui circule dans les
cavités du cerveau.
Des travaux récents indiquent que les plexus
choroïdes sont une voie d’entrée pour les
lymphocytes T dans le cerveau, au cours de la
surveillance immunitaire normale et également
au cours de la sclérose en plaques, contribuant
ainsi à la localisation préférentielle des plaques
et des zones dégénératives à proximité des
compartiments contenant le liquide céphalo-
rachidien.
Grâce à des modèles animaux de sclérose en
plaques et à un modèle cellulaire de l’interface
sang-liquide céphalo-rachidien que nous avons
développé, nous proposons d’identier, en
situation normale et inammatoire, les molécules
impliquées dans la migration des lymphocytes T à
travers cette barrière.
Ces travaux permettront de comprendre le rôle des
plexus choroïdes et du liquide céphalo-rachidien
dans l’apparition de la maladie, et d’identier
de nouvelles cibles thérapeutiques permettant
de réguler l’inltration des lymphocytes dans le
cerveau.
David-Axel Laplaud -
Implication des sous-populations
lymphocytaires dans la SEP.
La cause de la maladie implique
divers facteurs génétiques (une
cinquantaine de gènes ont
été découverts récemment) et des facteurs
environnementaux, plus mal connus. La SEP
se développe dans un contexte auto-immun où
le système immunitaire se retourne contre les
propres cellules nerveuses du malade.
Dans notre équipe de recherche nous essayons
de comprendre le rôle des différents composants
du système immunitaire dans l’attaque
orchestrée contre le système nerveux central.
Nous travaillons sur différentes composantes du
système immunitaire comme les lymphocytes T
ou les lymphocytes B. Les expérimentations se
font essentiellement à partir du sang de certains
malades participants à ces
recherches. récemment, nous
avons développé des stratégies
pour travailler directement sur
le cerveau de malades décédés
qui ont donné leurs organes à
la recherche scientique. Enn,
nous travaillons sur un modèle
animal de SEP an de mieux comprendre
la relation entre le système immunitaire et
le système nerveux. Ces travaux devraient
nous permettre à terme de mieux comprendre
les mécanismes conduisant à la maladie et
contribuer au développement de nouvelles
approches diagnostiques ou thérapeutiques
.
RÉGION PAYS DE LOIRE - NANTES
Coupe du cerveau obtenu en IRM
copyright inserm - Emmanuel-Alain Cabanis
 6
6
 7
7
1
/
7
100%