Les alcènes

Chimie
cours
Les Alcènes 22-juin-10
1STLA
I/ Formule générale
:
Les hydrocarbures non cyclique insaturés, de formule générale
ܥ
ܪ
ଶ
, sont des ALCENES.
II/ Nomenclature :
La nomenclature des alcènes dérive de celle des alcanes.
⇒
Alcènes à chaîne carbonée linéaire :
Le premier alcène porte un nom consacré par l’usage:
ࡴ
est l’éthylène.
Les alcènes suivants (݊
≥
3 ) ont un nom systématique :
La chaîne carbonée est numérotée de sorte à attribuer au 1
er
carbone doublement lié un numéro le plus petit
possible.
La terminaison « ane » de l’alcane correspondant est remplacée par la terminaison « ène » précédée de
l’indice de position de la double liaison.
Exemples :
n=3
ࡴ
propène
n=4
ࡴ
ૡ
But-1-ène
But-2-ène
⇒
Les alcènes à chaîne ramifiée :
La chaîne principale est la chaîne carbonée la plus longue contenant la double liaison C=C. C’est donc
elle qui fixe le nom de l’alcène, selon les règles des alcènes linéaires.
La numérotation des carbones portant éventuellement une ramification est alors automatiquement
définie.
Le nom de l’alcène est alors obtenu en respectant l’ordre suivant :
-
n° de position du (ou des) substituants.
- un tiret.
- nom du groupe alkyle (sans le « e » final).
- nom de l’alcène sans la terminaison « ène »attaché au nom du groupe alkyle.
- un tiret.
- indice de position de la double liaison.
- un tiret.
- terminaison « ène ».
- si stéréoisomérie Z/E, le nom est précédé de (Z)- ou (E)- .(voir chapitre stéréoisomérie dans ce document))
Exemples :
2
-
méthylprop
-
1
-
ène
4,4
-
diméthylpent
-
2
-
ène
3
-
éthyl
-
2
-
propylpent
-
1
-
ène
III/ Géométrie des alcènes :
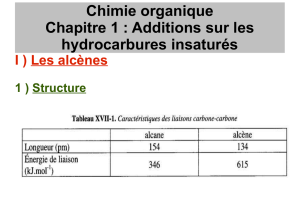
Toutes les liaisons du groupement sont dans un même plan. Du fait de la double liaison, ces deux atomes
de carbones ne peuvent pas tourner l’un par rapport à l’autre comme dans des liaisons simples.
En conséquence, si chaque atome de carbone de la double liaison porte des atomes ou groupes d’atome
différents, il peut exister deux stéréoisomères.
Les alcènes 3.docx
Page
1
sur
6

Exemple
:
A
B
Ces deux molécules ne sont pas superposable et ne sont pas l’image l’une de l’autre : on parle de
diastéréoisomère.
⇒
Nomenclature :
Dans la molécule A, les deux groupes méthyle sont de part et d’autre de l’axe de la liaison C=C (on dit en
position « trans »). Il s’agit de l’isomère E (de l’allemand entgegen : opposé )
A : (E)-but-2-ène
Dans la molécule B, les deux groupes méthyle sont du même coté de l’axe de la liaison C=C (on dit en
position « cis »). Il s’agit de l’isomère Z (de l’allemand zusammen : ensemble )
B : (Z)-but-2-ène
IV / Caractères physiques :
Les alcènes possédant jusqu'à 4 atomes de carbone sont gazeux dans les conditions ordinaires. Les suivants
sont liquides et leur point de fusion augmente avec leur masse molaire.
Les plus lourds sont solides.
Les alcènes sont insolubles dans l’eau mais solubles dans les hydrocarbures.
V / Réactivité :
A la différence des alcanes, les alcènes possèdent un site très réactif : la double liaison.
Le caractère principal de la double liaison est d’être insaturée. Les alcènes donnent des réactions d’addition
par ouverture de la liaison ߨ (cette liaison est plus facile à « casser » que la liaison σ C-C).
D’autre part, une double liaison est un site de forte densité électronique ou se trouve des électrons
faiblement liés aux noyaux. Cela permet à des réactifs électrophiles « d’attaquer » ce site.
Enfin, la double liaison constitue un point vulnérable de l’enchainement carboné. Certaines réactions
entrainent la coupure entre les deux carbones.
⇒
Réaction d’addition
Le schéma général des réactions d’additions sur une liaison éthylénique est figuré par :
Lors d’une réaction d’addition, il y a rupture de la liaison π de l’alcène.
Hydrogénation :
Cette addition se fait en présence d’un catalyseur (Nickel, platine finement divisé en phase gazeuse ou
liquide).
L’addition du dihydrogène sur un alcène conduit à l’alcane correspondant.
Exemple :
Cette réaction présente peu d’intérêt pratique. Elle est cependant utilisée pour la fabrication des
margarines (graisse obtenue par hydrogénation d’huile ou de graisses insaturées). Cela augmente la
température de fusion et cela permet de conserver les produits plus longtemps. (On limite par exemple
l’oxydation due à l’air)
Les alcènes 3.docx
Page
2
sur
6

Additions électrophiles
:
Notions de mécanisme réactionnel :
La plupart des réactions d’addition sur les doubles liaisons se font en deux étapes :
Attaque sur les électrons de la liaison π : La molécule qui s’additionne subit une rupture. On obtient
deux fragments : un cationique et un anionique. Le fragment cationique se fixe sur le premier
carbone éthylénique en se liant sur la liaison π.
Liaison du fragment anionique : Le fragment anionique (ܤ
ି
: ) se lie avrc son doublet libre sur l’autre
carbone qui possède maintenant une lacune électronique.
Addition d’halogénure d’hydrogène HX :
Exemple : Addition du chlorure d’hydrogène HCl
Le chlorure d’hydrogène se dissocie en ܪ
ା
et ܥ݈
ି
1
ère
étape :
2
nde
étape :
Application :
ܥ
ܪ
ଷ
−
ܥܪ
=
ܥܪ
−
ܥ
ܪ
ଷ
+
ܪܥ݈
→
ܥ
ܪ
ଷ
−
ܥ
ܪ
ଶ
−
ܥܪܥ݈
−
ܥ
ܪ
ଷ
2
-
chlorobutane
Remarque: si l’environnement de la double liaison n’est pas symétrique, on peut obtenir deux produits
différents
Exemple
ܥ
ܪ
ଶ
=
ܥܪ
−
ܥ
ܪ
ଷ
+
ܪܥ݈
→
ܥ
ܪ
ଷ
−
ܥܪܥ݈
−
ܥ
ܪ
ଷ
2
-
chloropropane
ou
→
ܥ
ܪ
ଷ
ܥ݈
−
ܥ
ܪ
ଶ
−
ܥ
ܪ
ଷ
1
-
chloropropane
En réalité on obtient très majoritairement du 2-chloropropane (réaction régiosélective)
Règle Markownikov :
Lors de l’addition d’un composé hydrogéné ܣܪ sur un alcène dissymétrique, l’hydrogène se fixe sur le
carbone le moins substitué (ou le plus hydrogéné)
Les alcènes 3.docx
Page
3
sur
6

Addition de l’eau
:
L’addition de l’eau sur un alcène conduit à un alcool suivant la réaction :
Cette réaction a lieu en présence d’un catalyseur, en général l’acide sulfurique concentré.
La règle de Markownikov s’applique : l’hydrogène se fixe sur le carbone le moins substitué et le groupe ܱܪ
sur l’autre.
A part l’addition de l’eau sur l’éthylène qui conduit à un alcool primaire (l’éthanol), toutes les autres
conduisent à des alcools secondaires ( le groupe ܱܪ n’est pas en bout de chaine)
Exemple :
ܥ
ܪ
ଶ
=
ܥܪ
−
ܥ
ܪ
ଷ
+
ܪ
ଶ
ܱ
→
ܥ
ܪ
ଷ
−
ܥܪܱܪ
−
ܥ
ܪ
ଷ
Propan
-
2
-
ol
Addition d’un halogène :
Les halogènes ܺ
ଶ
(ܥ݈
ଶ
, ܤݎ
ଶ
, ܫ
ଶ
) s’additionnent sur les alcènes pour donner des dérivés dihalogénés.
Exemple :
ܥ
ܪ
ଶ
=
ܥܪ
−
ܥ
ܪ
ଷ
+
ܥ݈
ଶ
→
ܥ
ܪ
ଶ
ܥ݈
−
ܥܪܥ݈
−
ܥ
ܪ
ଷ
1,2
-
dichlorop
ropan
e
Cl2 et Br2 se fixent facilement à froid. Ces réactions sont souvent utilisées pour la caractérisation des
doubles liaisons (décoloration de la solution d’eau de brome initialement rouge/orangé )
Ces additions sont stéréospécifique : c’est une cis-addition.
⇒
Réactions d’oxydations
Epoxydation :
L’action d’un peracide R-CO-O-OH
sur un alcène conduit à la formation d’un époxyde.
Exemple :
+
→
+
Ethylène peracide époxyéthane
Les époxydes sont très réactifs et peuvent être hydrolysés en milieu acide pour donner des glycols.
(hydrolyse : coupure d’une liaison sous l’action de l’eau (à ne pas confondre avec l’hydratation qui est
l’addition de l’eau.)
௬ௗ௬௦
ሱ
ۛ
ۛ
ۛ
ۛ
ۛ
ۛ
ሮ
Ethylène glycol
(ou éthane-1,2-diol )
L’éthylène glycol est employé en tant qu’antigel dans les liquides de refroidissement.
Ozonolyse :
Cette réaction sert en synthèse organique, pour transformer des alcènes en cétone/aldéhyde/acide
carboxylique.
L’ozone réagit avec la double liaison pour donner un molozonide qui se réarrange en ozonide.
Les ozonides sont très instables :
Ils peuvent se décomposer spontanément de manière explosive ;
Leur hydrolyse produit des composés carbonylés (aldéhydes ou cétones)
Les alcènes 3.docx
Page
4
sur
6

Exemple d’ozonolyse
+ܱ
ଷ
→
→
௬ௗ௬௦
ሱ
ۛ
ۛ
ۛ
ۛ
ۛ
ۛ
ሮ
+
molozonide
ozonide
cétone
aldéhyde
⇒
Polymérisation
Une polymérisation est une réaction dans laquelle les molécules se fixent les unes aux autres en grand nombre.
Exemple :
polymérisation de l’éthylène :
L’éthylène peut se polymériser en polyéthylène.
Monomère
polymère
Formule
:
(
−
ܥ
ܪ
ଶ
−
ܥ
ܪ
ଶ
−
)
N de 100 à environ 200 000
Ethylène
Polyéthylène
(P
E
)
La masse molaire du polyéthylène peut atteindre plusieurs millions de gramme/mole.
Le polyéthylène est le polymère de synthèse le plus employé. L'utilisation la plus visible du polyéthylène est les sacs plastiques.
Les polyéthylènes sont classés en fonction de leur densité qui dépend du nombre et de la longueur des ramifications présentes sur les
chaînes moléculaires.
PE basse densité (LDPE) Ce sont des produits souples : sacs, films, sachets, sacs poubelles, récipients
souples (ketchup, crèmes hydratantes...), etc…
PE haute densité (HDPE) Ce sont des produits rigides : flacons (détergents, cosmétiques...), bouteilles,
boîtes type Tupperware, jerricans, etc…
Le polyéthylène réticulé (PER) Il montre une meilleure tenue thermique que le PE « standart ». Il est utilisé pour
la fabrication de gaines de câbles, de tubes (plomberie ) …
PE à poids moléculaire
« ultra-haut » (UHMWPE)
On obtient des fibres de performance remarquable : 15 fois plus résistante que
l'acier, la fibre est utilisée pour la protection (casques et gilets pare-balles ), pour
les cordages, les filets, les articles de sports, les gants et pantalons de protection.
Concurrencée par les fibres aramides (Kevlar) et les fibres de polyamide et de
polyester, la fibre de polyéthylène est plus légère pour des performances
supérieures.
D’autres composés peuvent se polymériser comme les dérivés vinylique du type :ܣ − ܥܪ = ܥܪ
ଶ
n(
)
→
…(
)…
Exemples :
Polymérisation du chlorure de vinyle :
Monomère
polymère
Formule
:
(
−
ܥܥ݈
−
ܥ
ܪ
ଶ
−
)
n de 700 à 1500
Chlorure de vinyle
Polychlorure de Vinyle (PVC)
Utilisation :
Pvc rigide : tuyau de canalisation, carte format carte de crédit
Pvc souple : isolant sur des manches de pinces, revêtement de sols
Pvc plastifié utilisé comme film adhésif (palettisation, marquage publicitaire…) film étirable (emballage…)
Les alcènes 3.docx
Page
5
sur
6
 6
6
1
/
6
100%