Les alcènes I- Préparation 1) Réduction des Alcynes a

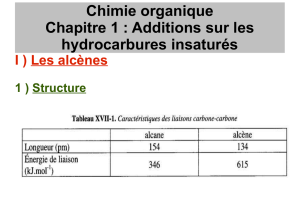
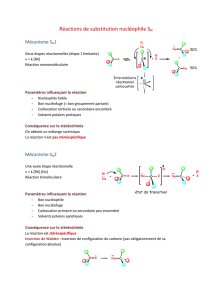
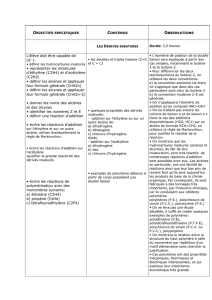
Les alcènes
I- Préparation
1) Réduction des Alcynes
a) Hydrogénation
b) Réduction par les métaux dissous
c) Les organoboranes
2) La réaction de Wittig

II- Réactivité des alcènes
1) Réduction
La réaction a lieu à la surface d’un catalyseur finement divisé qui est généralement du palladium. On
peut utiliser Ni et Pt à la place. La réaction est stéréospécifique, il s’agit d’une syn addition. La
configuration des produits d’arrivé dépend de la configuration des produits de départ. Les deux atomes
d’hydrogène attaquent la même face de l’alcène.
Remarque : les deux faces peuvent être attaquées.
2) Additions électrophiles
Un alcène est riche en électrons, c’est donc un site nucléophile.
a) Réaction avec les hydracides

C’est une réaction régiosélective.
Mécanisme :
Le carbocation tertiaire se forme plus rapidement que le carbocation primaire car il est plus stable.
3) Hydratation des alcènes
La réaction doit être catalysée par un acide fort.

1) Réaction d’addition des halogènes
C’est une réaction stéréospécifique.
Mécanisme :

Remarque : Lorsque la réaction est effectuée en présence d’eau ou en présence d’un alcool on obtient
les produits suivant :
Acides hypohalogéneux (XOH)
Les additions radicalaires
La régioselectivité s’inverse par rapport aux conditions ioniques.
Mécanisme
 6
6
 7
7
 8
8
 9
9
 10
10
1
/
10
100%