rétinite pigmentaire - The Foundation Fighting Blindness

Larétinitepigmentaireestuneaffection
génétiquequiendommagelentementla
rétine.Cetteaffectionprogressetoutaulong
delavied’unepersonnequienestatteinteet
toucheenvironunCanadiensur3500.
Premierssymptômes
Généralement,larétinitepigmentaireest
diagnostiquéeàl’enfanceouàl’adolescence,
maiscertainespersonnesneprésentent
aucunsymptômecaractéristiqueavantl’âge
adulte.Ladifficultéàvoirlanuitetà
s’adapteràl’obscuritéestlepremier
symptômelepluscourant:c’estcequ’on
appellel’héméralopie(céciténocturne).La
visionpériphériquecommenceaussiàse
détériorerauxtoutpremiersstadesdela
maladie.
Descriptionmédicale
Larétinitepigmentairesurvientpar
suited’unedétériorationlentedes
cellulesphotosensiblesdelarétine,
appeléesphotorécepteurs,causée
parunemutationgénétique
héréditaire.Denombreuses
mutationspeuventcauserlarétinite
pigmentaire.
Lesphotorécepteurssontdedeux
types,soitlesbâtonnetsrétinienset
lescônesrétiniens.Lesbâtonnets
rétinienssontresponsablesdela
visionpériphériqueetnocturne,
tandisquelescônesrétinienssont
responsablesdelavisioncentraleet
delaperceptiondesmenusdétailset
descouleurs.Lacéciténocturne
apparaîtdèslespremiersstadesdela
rétinitepigmentaire,carles
mutationsquicausentlarétinite
pigmentaireportentd’abordatteinte
auxbâtonnetsrétiniens.
Lesbâtonnetsrétinienscontinuentde
disparaîtreet,avecletemps,les
cônesrétinienscommencentaussià
disparaître.Oncomprendmal
pourquoiilenestainsi,maisilsemble
queladisparitiondescônesrétiniens
soitdéclenchéeparlamortdes
bâtonnetsrétiniens.Ladisparitiondes
cônesrétiniensentraînelapertedela
visioncentraleetdel’acuitévisuelle.
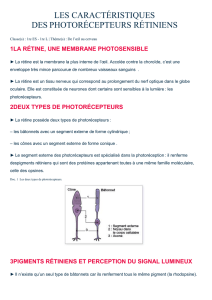
Unprofessionneldelavuequi
examinelarétined’unepersonne
atteintederétinitepigmentaire
constatehabituellementqu’elleaun
aspecttacheté,cequiestattribuable
Feuilletd’information
RÉTINITEPIGMENTAIRE
LaFoundationFightingBlindnessa
préparéunguidesurlarétinite
pigmentaireetlestroublesconnexes
(GuidetoRetinitisPigmentosaand
RelatedConditions,enanglais
seulement)pouraiderlepatient,sa
familleetsesamisàmieuxcomprendre
lamaladieetfaciliterlesdiscussions
avecl’ophtalmologiste.Commandez‐le
encomposantle1‐800‐461‐3331.

àdesamasdepigmentsnoirâtresqui
s’accumulentlorsquelarétineest
endommagée,d’oùlenomdelamaladie
(rétinitepigmentaire).D’autresrésultats
typiquesd’unexamendelarétine
comprennentl’amincissementdesvaisseaux
sanguinsetuneapparencepâleetcireusedu
nerfoptique;touscessignessontplus
marquésaustadeultimedelarétinite
pigmentaire.
Danslaplupartdescas,lessymptômesdela
rétinitepigmentairesontlimitésàl’œil.
Cependant,dans20à30%descas,larétinite
pigmentairefaitpartied’unsyndromequi
touched’autrespartiesdel’œil.Lesexemples
lespluscourantssontlesyndromedeUsher
etlesyndromedeBardet‐Biedl.Plusde
30troubleshéréditairesrarespeuvent
entraînerunepertedevisiondutypedecelle
associéeàlarétinitepigmentaire.
Diagnostic
Unophtalmologistepeutsoupçonnerla
présencedelarétinitepigmentaireenraison
dessymptômesetdesrésultatsd’unsimple
examendelavue.Lesdeuxtestsquisuivent
permettentdeclarifierlediagnostic.
L’électrorétinographie(ERG)mesureles
réponsesélectriquesdelarétineàlalumière;
cetestpeutmesurerlesréponsesdes
bâtonnetsetdescônesrétiniens.Bienque
tantlesbâtonnetsquelescônesrétiniens
puissentêtretouchéschezlespersonnes
atteintesderétinitepigmentaire,les
changementslesplusmarquésaudébutdela
maladiesontobservésdanslesbâtonnets
rétiniens;cettecaractéristiqueparticulière
contribueaudiagnosticdelarétinite
pigmentaire.Pourl’ERG,onvousdemandera
dedemeurerdansunepiècesombrependant
30minutesetonvousmettrades
gouttesdansunœiloudanslesdeux
yeux.Letestconsisteàplacerun
verredecontactspécialouune
électrodeenorsurl’œilousurla
paupièreinférieure,puisàexposer
l’œilàdeséclairslumineux.
Letestduchampvisueldétecte,
mesureetsurveillelestachesnoires
danslechampdevision.Pourcetest,
vousdevezregarderdansunappareil
quiémetdeséclairslumineuxet
indiquerceuxquevouspercevez.En
prenantnotedeséclairsquevous
percevez(ounon),onpeut
déterminerdansquellemesurevotre
vueesttouchée.
Outrelestestsci‐dessus,la
consultationgénétiqueestunaspect
importantduprocessusdiagnostique.
Génétiquedelarétinitepigmentaire
Larétinitepigmentaireestune
maladiecauséepardesmutations
génétiquesquiportentatteinteaux
photorécepteursdelarétine.Ilya
diversmodesdetransmission
héréditairedelarétinite
pigmentaire:autosomiquedominant,
autosomiquerécessifourécessiflié
auchromosomeX.Unconseilleren
génétiquepourradiscuterdevos
antécédentsfamiliauxavecvousafin
dedéterminerlequeldecesmodes
estassociéàvotrepertedevision.
Cesinformationspourraient
permettreauconseillerdevousen
diredavantagesurlaprogressionde
larétinitepigmentairechezvouset
devousrenseignersurlerisquede

pertedevisionchezlesmembresdevotre
famille.
Danscertainscas,onpeuteffectueruntest
génétiqueàpartirdesangprélevéchezune
personneatteintederétinitepigmentaire.Un
teltestpeutpermettrededéterminerles
mutationsquisontàl’originedelamaladie.
Règlegénérale,chezunepersonneatteinte
derétinitepigmentaire,iln’yadesanomalies
quedansuneseulepairedegènes.Les
scientifiquesontàcejourcernéplusde
50gènesdanslesquelsdesmutationsqui
causentlarétinitepigmentairepeuventse
produire.Onfiniraprobablementparcerner
desmutationsdansplusde100gènes
différents.Puisqu’unsigrandnombrede
mutationsgénétiquescausantlarétinite
pigmentairedemeurentinconnues,les
chancesqu’untestgénétiquedonnedes
résultatsdéfinitifssontd’environ50%.Ense
fondantsurvosantécédentsfamiliauxetsur
lemodedetransmissionhéréditairedela
rétinitepigmentairechezvous,leconseiller
engénétiquepourravousdiresilesrésultats
dutestgénétiquesontsusceptiblesd’être
définitifs.Veuillezconsulternotrefeuillet
d’informationsurletestgénétiquepour
obtenirdeplusamplesrenseignements.
Diversesmutationsgénétiquespeuvent
porteratteinteàlarétineouentraverson
fonctionnementdedifférentesfaçons.Par
exemple,certainesmutationsmodifientla
façondontlarétinetransformeles
nutriments,tandisqued’autresportent
atteinteauxphotorécepteurs.Ilestimportant
dedéterminerlegèneetlamutation
responsablesdelamaladie,cardenombreux
traitementscontrelarétinitepigmentaireen
coursdedéveloppementcibleront
destypesgénétiquesparticuliers.
Évolutiondelamaladie
Aveclaprogressiondelarétinite
pigmentaire,ilyaunelente
détériorationdelavision
périphérique,cequientraîneune
visiontubulaire.À40ans,de
nombreusespersonnesatteintesde
rétinitepigmentairesontaveuglesau
sensdelaloietontunchampde
visiontrèsétroit,bienqu’elles
puissentencorelireetreconnaîtreles
visages.Lasensibilitétrèsaccrueàla
lumièreetàl’éblouissementest
courante,toutcommelaphotopsie
(perceptiond’éclairslumineuxou
d’étincelles).
Laperted’acuitévisuelle(capacitéde
voirclairement)estaussicauséepar
larétinitepigmentaire,maisson
apparitionestplusvariable.Certains
patientsconserventuneacuité
visuellenormalemalgréunevision
tubulaire,tandisqued’autresperdent
leuracuitévisuelleàunstadebien
plusprécocedelamaladie.Unjour
oul’autre,laplupartdespersonnes
atteintesderétinitepigmentaire
commencerontàperdreleurvision
centraleetquelques‐unesperdront
touteperceptionlumineuse.
Traitement
Aucuntraitementn’estactuellement
approuvépourprévenirouralentirla
pertedevisionassociéeàlarétinite
pigmentaire.Lespersonnesatteintes
doiventnéanmoinssubirdesexamens
réguliersdelavue,mêmeen

l’absencedemodificationsdelavision,pour
éviterlescomplicationsgraves,mais
traitablesquipeuventaggraverladéficience
visuelle,tellesquelescataractesetl’œdème
maculaire.
Recherche
Plusieursgroupesderecherches’intéressent
audéveloppementdetraitementscontrela
rétinitepigmentaire.Lestraitements
expérimentauxpeuventêtredivisésentrois
grandescatégories:
traitementsprotecteurs
traitementscorrectifs
traitementsquipermettentde
recouvrerlavue.
Lestraitementsprotecteursvisentàstopper
(ou,dumoins,àralentir)leslésionscausées
parlesmutationsgénétiques.Souvent,les
traitementsprotecteursneciblentpasune
seulemutationetpeuventêtreutilescontre
diverstypesderétinitepigmentaire.Ces
traitementscomprennentceuxquistoppent
leprocessusdemortdesphotorécepteurs
(apoptose),demêmequelesthérapies
dérivéesdescellulesquicontribuentàla
surviedesphotorécepteurs,dontNT‐501,un
produitdeNeurotechPharmaceuticalsen
coursdedéveloppement.Ils’agitd’unepetite
capsulecontenantdescellulesvivantes
génétiquementmodifiéespourlibérerdes
facteursdecroissancequipeuventprotéger
lesphotorécepteurs,quiestintroduitedans
unepetiteincisionpratiquéedansl’œil.Ce
traitementfaitactuellementl’objetd’unessai
menéàl’UniversitédeCalifornieàSan
Francisco.Onmèneaussiunessaisurun
autretraitementprotecteur,soitun
médicamentàprendreparvoieorale(l’acide
valproïque),quipourraitêtreutilecontre
certainesformesautosomiques
dominantesdelarétinite
pigmentaire.
Certainstraitementsprotecteurs
visentspécifiquementàprévenirla
mortdescônesrétinienschezles
personnesatteintesderétinite
pigmentaire–etdonclapertedela
visioncentrale–auxstadesavancés
delamaladie.Veuillezconsulter
notrefeuilletd’informationpouren
savoirdavantagesurlestraitements
quiprotègentlescônesrétiniens.
Lestraitementscorrectifsvisentà
inverserledéfautgénétiquesous‐
jacentquicauselapertedevision.Si
cestraitementss’avèrentefficaces,ils
pourraientprévenirlapertedevision
chezunepersonnetraitéedèsla
rétinitepigmentairediagnostiquée.
Lestraitementscorrectifspourraient
aussicontribueràralentirl’évolution
delamaladiechezlespersonnesdont
lavisionestdéjàtouchée,surtoutaux
premiersstadesdelamaladie.Les
traitementscorrectifsencoursde
développementciblentcertaines
formesderétinitepigmentaire
transmisesselonlemoderécessif.Les
thérapiesgéniques,quiremplacent
ungènequinefonctionneplus,
représententuntypedetraitement
correctif.Desessaiscliniquessurdes
thérapiesgéniquescontreplusieurs
typesderétinitepigmentairesonten
coursetleursrésultatsàcejoursont
encourageants.Desmédicamentsqui
remplacentlafonctionperdue,
commeceluiactuellementdéveloppé
parl’entreprisecanadienneQLTInc.

Misàjourle7novembre2014:Cefeuillet
d’informationaétémisàjourparlaDreMary
Sunderland,directriceprincipale,Rechercheet
éducation,FoundationFightingBlindness.Le
feuilletavaitétéinitialementrevuparlaDreJane
Green,professeurederechercheengénétique
oculaire,UniversitéMemorial,St.John’s,
Terre‐NeuveetLabrador,etleDrBillStell,
conseillerscientifique,FoundationFighting
Blindness,etprofesseurdebiologiecellulaireet
d’anatomie,UniversitédeCalgary.
AppuyezlarecherchesurlaprotectiondelavueenfaisantundonàlaFoundationFightingBlindness
1‐800‐461‐3331www.ffb.ca
pourletraitementdelarétinitepigmentaire
causéepardesmutationsdesgènesrétinite
pigmentaireE65etLRAT,pourraientaussiêtre
correctifs.
Lestraitementsquipermettentderecouvrer
lavuereprésententaussiundomainedans
lequellarechercheestdeplusenplus
fructueuse.Cestraitementssontdestinésaux
personnesquiontdéjàcomplètementou
presquecomplètementperdulavue.Les
thérapiesàbasedecellulessouchesvisentà
remplacerlesphotorécepteursrétiniens
disparus.Lesrésultatspréliminairesdesessais
cliniquessurl’utilisationdecesthérapies
contred’autresmaladiesrétiniennes
dégénérativessonttrèsprometteurs;des
essaiscliniquesmenésauprèsdepersonnes
atteintesderétinitepigmentaireseprofilent
àl’horizon.Lesprothèsesrétiniennes,comme
ArgusII,ou«œilbionique»,utilisentla
technologieinformatiquepourgénérerla
vision.LaFoundationFighting
Blindnesssoutientlepremieressai
cliniquecanadiensurArgusII.Des
médicamentsetthérapiesgéniques
encoursdedéveloppement
pourraientdonnerauxcellules
nerveusesnonphotoréceptricesdela
rétinelacapacitédepercevoirla
lumière.
Grâceànosgénéreuxdonateurs,
nousfinançonsdesrecherches
d’avant‐gardedanscesdomaines.
ConsulteznotresiteWebau
www.ffb.capourensavoirdavantage.
1
/
5
100%