Avril2016-Tempo Médical

MÉDECINE DE DEMAIN
10ITEMPO MÉDICAL – AVRIL 2016 – WWW.MEDIPRESS.BE
Les maladies ostéo-musculaires représentent le plus important
groupe de maladies chroniques et la plus grande cause d'invalidité
de la population active, et l’ostéoarthrose du genou en est le cas
pathologique le plus fréquent. Souvent, le développement dégénéra-
tif commence par une blessure au cartilage sur la surface portante
du condyle, après un traumatisme ou des lésions méniscales. Cela
entraîne des dégénérescences dans le cartilage environnant, indi-
catives d'arthrose. Malheureusement, le cartilage articulaire montre
une capacité très limitée de guérison, car il ne peut se régénérer
par lui-même. Les défects du cartilage articulaire du genou ont en
effet un très faible potentiel d’autoréparation, à cause de la capacité
mitotique réduite des chondrocytes in vivo. De tels défects de car-
tilage articulaire peuvent être réparés, pour éviter leur progression
vers l’arthrose.
Différentes méthodes de greffe de cellules-souches sont également
étudiées depuis plus de vingt ans, afin de permettre par exemple la
reconstitution spontanée de cartilage hyalin naturel. Ces méthodes
de greffe montrent des perspectives thérapeutiques prometteuses.
Ainsi, récemment, une équipe rapportait au Congrès de l’American
Academy of Orthopaedic Surgeons (AAOS) des résultats spectacu-
laires de restitution du cartilage hyalin avec des cellules souches
allogéniques, c’est-à-dire d’un donneur non apparenté, en présence
de chondrocytes du patient lui-même et d’un support permettant
de maintenir les cellules en place. A distance, les cellules d’origine
allogénique disparaissent et sont remplacées par les cellules car-
tilagineuses du patient. D’autres applications dans le traitement
des fractures et pertes de substance osseuse chez l’animal ont
également été présentées, démontrant la reconstruction osseuse
en présence de tissu de granulation induit par un corps étranger et
l’implantation d’une matrice et de protéines isolées à partir d’une
culture de cellules-souches. Ces résultats précliniques laissent pré-
sager de belles perspectives. Les médecins disposent cependant
de trop peu d’évidence clinique pour pouvoir remplacer les moyens
actuels de traitement par des trai-
tements avec les cellules-souches.
Néanmoins, des premières données
semblent montrer leur intérêt dans le
traitement d’infarctus osseux, sans frac-
ture associée.
L’utilisation de PRP (plasma riche en plaquettes) semble également
intéressante, bien qu’il y ait actuellement une vingtaine de façons
de le préparer, et qu’il soit encore impossible d’en déterminer avec
précision la formulation la plus efficace. De même, il est admis que
des injections de cellules-souches ou de PRP, notamment dans le
but d’améliorer la cicatrisation de tissus lésés, exercent un rôle
anti-inflammatoire, mais recommander leur usage représenterait un
coût significatif à charge du patient, comparativement à la simple
injection d’un dérivé cortisoné.
La thérapie cellulaire et les thérapies biologiques rentrent lentement
dans l’arsenal thérapeutique. Elles doivent encore être confinées
dans le cadre de protocole de recherche, et nécessitent davantage
d’études avec groupe-contrôle pour affirmer leur apport réel. Il
reste encore à préciser les maladies pour lesquelles elles seraient
le mieux indiquées, établir leurs bénéfices et les risques auxquelles
elles exposent.
Orthopédie et cellules-souches :
Un avenir thérapeutique certain, dans le futur
Les lésions ou défects osseux et cartilagineux du genou, des chevilles ou des hanches sont
fréquentes, et nécessitent souvent, à long terme, la pose d’une prothèse. Ces remplacements
articulaires peuvent malheureusement ne donner satisfaction qu’incomplètement (17 % pour
les prothèses totales de genou) ou présenter une faillite mécanique ou des signes d’usure
à long terme, qui vont nécessiter leur remplacement. Certaines prothèses ont une durée de
vie relativement plus limitée que d’autres et leur remplacement peut s’avérer problématique
dans certains cas, ce qui est la raison pour laquelle les orthopédistes ne recourent à
cette alternative que le plus tard possible, lorsqu’elle reste la seule option envisageable.
Globalement, on peut estimer qu’environ 20.000 poses de prothèse de la hanche et
30.000 prothèses du genou sont pratiquées chaque année en Belgique.
Vincent Wautier
Les médecins disposent de trop
peu d’évidence clinique pour
pouvoir remplacer les moyens actuels
de traitement par des traitements
avec les cellules-souches.
T
E
M
P
O
F
O
C
U
S
M
É
D
E
C
I
N
E
D
E
D
E
M
A
I
N

TEMPO MÉDICAL – AVRIL 2016 – WWW.MEDIPRESS.BEI11
MÉDECINE DE DEMAIN
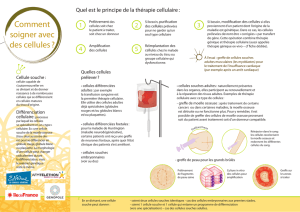
Les techniques de greffe de cellules-
souches se développent lentement
Des recherches et techniques se déve-
loppent, principalement depuis une quin-
zaine d’années, reposant sur la greffe
de cellules-souches programmées pour
reconstituer des tissus ou des organes
spécifiques, et des os, des tendons ou
du cartilage. Ces techniques en cours de
développement pourraient à l’avenir per-
mettre de réparer bon nombre de lésions,
en reposant sur la faculté de pouvoir iso-
ler ces cellules-souches et de savoir les
implanter. Une chirurgie prothétique et
régénérative des os et du cartilage se déve-
loppe au départ de différentes techniques
de greffe de cellules-souches, exercées soit
par arthrotomie, soit sous une arthroscopie
nettement moins invasive lorsque l’inter-
vention chirurgicale le permet. Ces tech-
niques de greffe consistent à greffer des
cellules-souches sur les zones osseuses,
cartilagineuses, tendineuses ou ligamen-
taires lésées ou endommagées. Selon la
technique utilisée, le prélèvement, la sélec-
tion des cellules et leur greffe peuvent se
dérouler dans un processus en une seule
phase continue, ou en plusieurs phases.
Recours aux cellules-souches
mésenchymateuses
Les cellules-souches sont des cellules
indifférenciées, capables d’auto-renou-
vellement et d’auto-différenciation en cel-
lules matures pour assurer la tenue et le
renouvellement des organes tissulaires.
Les cellules souches mésenchymateuses
(CSM) sont des cellules souches tissulaires
multipotentes, donnant un nombre limité
de types cellulaires différents. Ce sont des
cellules-souches d’origines mésodermiques
présentes dans divers tissus de l'organisme
adulte tels que la moelle osseuse ou le tissu
adipeux, dans lesquels elles sont isolées, et
qui donnent naissance notamment aux os
et cartilages. Il est possible de les prélever
de la moelle osseuse autologue aspirée au
niveau de la crête iliaque postérieure, ou
du tissu graisseux obtenu par lipoaspiration
de graisse au-dessus de la crête iliaque
externe. Les CSM du tissu graisseux sont
environ cent fois plus nombreuses que
celles de la moelle osseuse.
Elles peuvent être isolées de la couche
mononucléaire de la moelle osseuse ou du
tissu adipeux après séparation par centri-
fugation, pour enlever les cellules rouges
et hématopoïétiques. Cette centrifugation
prend une quinzaine de minutes. Les CSM
sont présentes en très faibles quantités
chez l'adulte. Le réservoir de CSM dans la
moelle osseuse est de 0,01 à 0,001 % des
cellules mononuclées. Les techniques de
leur utilisation en chirurgie orthopédique
évoluent constamment. Malheureusement,
le capital en cellules-souches du patient
peut être réduit en raison des traitements
dont il bénéficie, rendant cette source de
nouvelles thérapeutiques moins efficientes
(c’est le cas par exemple dans l’ostéoné-
crose cortisonique où l’on observe une di-
minution significative des cellules-souches,
ce qui expliquerait les résultats mitigés des
traitements par cellules souches dans cette
indication).
Perspectives de régénération des os
et des cartilages
Le caractère multipotent des CSM favorise
leur utilisation en thérapie cellulaire répara-
trice dans le cas de pathologies osseuses et
articulaires. Sous l’action d’inducteurs spé-
cifiques ou facteurs de croissance, les CSM
sont capables de se différencier en ostéo-
blaste (os) ou en chondrocytes (cartilage).
Les facteurs de croissance sont des pro-
téines produites par les cellules présentes
dans le tissu osseux, qui se libèrent loca-
lement en cas d'ostéolyse ou de fracture.
La greffe de CSM directement sur la lésion
arthrosique permet ainsi la réparation ou
la reconstitution de tissus non vascularisés
et non innervés tels que le cartilage, qui ne
peut se réparer naturellement. Après une
première période d’apprentissage durant
laquelle le traitement se limitait principale-
ment à la greffe de CSM sous arthroscopie
dans les cas de genoux à bonne mécanique,
la thérapie cellulaire a été étendue expéri-
mentalement à des cas de désaxation avec
ostéotomie associée, et depuis peu, à des
cas complexes d'ostéotomie avec recons-
truction du ligament croisé ou du ménisque.
Une première technique de thérapie cellu-
laire consiste à implanter des CSM en une
seule étape, sans culture. Dans la même
salle de bloc opératoire, on procède suc-
cessivement à une anesthésie locale ou gé-
nérale, au prélèvement de moelle osseuse
ou de tissu graisseux et à leur centrifuga-
tion, à la préparation des CSM avec des
facteurs protéiques stimulant leur crois-
sance et avec du PRP pouvant favoriser
la cicatrisation, et à la mise en place des
CSM sur une matrice biologique permettant
leur transport et l’implantation directe sur
la lésion arthrosique pour la repousse de
cartilage, après préparation arthroscopique
des lésions arthrosiques. La génération de
cartilage et d’os s’effectue ensuite par les
CSM autologues. Ces CSM sont des cel-
lules multipotentes, quiescentes et inac-
tives, et leur croissance doit être stimulée
pour une utilisation en une seule étape.
Elles doivent être incitées à se multiplier
pour coloniser le défect ostéochondral ou
la lésion arthrosique avec perte d’os et de
cartilage, et se transformer pour les recons-
tituer. Elles sont fortement stimulées dans
leur multiplication lorsqu’elles sont mixées
avec des protéines osseuses particulières,
et activées par une matrice osseuse pro-
téique déminéralisée avant leur transplan-
tation ou injection, pour ensuite régénérer
les défects ostéo-cartilagineux.
Le capital en cellules-souches du patient
peut être réduit en raison des traitements
dont il bénéficie

MÉDECINE DE DEMAIN
12ITEMPO MÉDICAL – AVRIL 2016 – WWW.MEDIPRESS.BE
Une autre technique de thérapie cellulaire consiste à utiliser les CSM en plusieurs
étapes, avec prélèvement et ensuite mise en culture, lors de laquelle il faut éviter
soigneusement les risques de manipulation, de contamination bactérienne et
d’altération génétique des cellules souches qui sont cultivées avant leur implan-
tation. Jusqu’il y a peu, ces CSM étaient ensuite injectées dans l’articulation non
activées, donc sans possibilité de cicatrisation des lésions arthrosiques. Injecter
des CSM dans l’articulation sans les transplanter contre la lésion peut créer un
risque de destruction de la plupart d’entre elles dans le liquide synovial articulaire.
Certaines techniques permettent cependant d’activer ces CSM qui sont ensuite
implantées directement contre la lésion arthrosique du genou sous arthroscopie, en
utilisant une matrice de transport (ou scaffold) bio-résorbable à base, par exemple
d’hydroxyapatite et de collagène. Dans certains cas d’arthrose du genou précoce
avec critères d’exclusion de transplantation de cellules souches ou d’arthrose pré-
coce de hanche, des injections intra-articulaires de forte concentration de cellules
souches activées peuvent être pratiquées, seules ou en association avec d’autres
composants.
Dans tous les cas, la quantité de CSM utilisée joue un rôle critique dans le succès
de ces interventions chirurgicales. Au stade actuel, on peut considérer qu’il ne
s’agit encore que d’opérations cliniques relativement isolées, et peu généralisées.
Perspectives de thérapie cellulaire et greffe ligamentaire
On observe actuellement une augmentation significative du nombre de blessures
des articulations et notamment de lésions du ligament croisé antérieur du genou
(LCA). On recense chaque année environ 6.000 réparations chirurgicales du LCA
en Belgique, et plus de 450.000 dans le monde.
Les tendons et ligaments peuvent faire l’objet de diverses pathologies de gravités
très variables. Parmi les lésions les plus fréquentes de ces tissus, on trouve les
tendinites qui sont des pathologies touchant les tendons et faisant intervenir un
mécanisme inflammatoire, et les entorses qui sont des blessures consistant en une
élongation temporaire ou permanente du ligament parfois accompagnée d’un arra-
chement osseux, ou consistant en une déchirure partielle ou totale du ligament. Si
le tissu possède une capacité de cicatrisation suffisante, un processus de guérison
spontanée pourra survenir après lésion. Dans le cas de rupture d’un ligament tel
que le LCA qui est constitué de zones peu ou non vascularisées, le tissu n’a pas la
capacité de cicatriser, et la blessure ne peut pas guérir spontanément.
Les greffes autologues sous arthroscopie sont aujourd’hui largement pratiquées
pour la réparation du LCA. Elles consistent à prélever chez le patient blessé un
tendon ou une portion de tendon dans une autre localisation anatomique et à
l’utiliser comme greffon pour remplacer le LCA rompu. Malgré l’efficacité de ces
traitements chirurgicaux dont les résultats sont satisfaisants dans 70 à 90 % des
cas selon la technique utilisée, certains inconvénients subsistent.
On recense chaque année environ 6.000 réparations chirurgicales
du LCA en Belgique, et plus de 450.000 dans le monde.

TEMPO MÉDICAL – AVRIL 2016 – WWW.MEDIPRESS.BEI13
MÉDECINE DE DEMAIN
Les affections ostéoarticulaires sont un des problèmes
majeurs dans nos populations. Les handicaps qu’elles
provoquent sont très lourds à porter tant pour les patients
– qu’ils soient jeunes et en développement, adultes et
impliqués professionnellement, ou plus âgés perdant en
tout ou en partie leur autonomie – que pour la société
qui assure techniquement et financièrement les soins de
santé. Les progrès thérapeutiques accumulés dans ces
affections sont importants. La performance de ces soins
dépend de l’importance des destructions des tissus (os,
cartilages, ligaments, tendons, muscles). Dans les cas
majeurs, la chirurgie prothétique, qui a elle aussi fait des
progrès, peut fournir des solutions palliatives. Néanmoins,
la reconstruction des tissus lésés et la restitution « ad
integrum » reste le ‘graal’ recherché, redonnant au patient
une fonction ostéoarticulaire complète.
Cette médecine dite régénératrice n’est plus une utopie
même si elle est encore sujette à diverses recherches.
Depuis plus de 50 ans, des processus de régénération
ostéoarticulaire ont été identifiés et leurs applications
thérapeutiques investiguées et établies. Citons successi-
vement l’ostéo-induction produite par la matrice osseuse
déminéralisée, les facteurs de croissance comme les
Bone Morphogenetic Protein (BMP), les chondrocytes
autologues, les cellules souches mésenchymateuses
(MSC) et les thérapies géniques. Les éléments clés de
ces traitements réparateurs sont des cellules particu-
lières, des facteurs de croissances, des matrices ou
support mécaniques (« scaffold ») et aussi des stimuli
mécaniques.
Les publications se sont multipliées. Les principaux sujets
de ces études sont les défauts de (re)construction osseuse
tels que le retard de consolidation osseuse (pseudarthrose,
kystes osseux), l’ostéonécrose, les lésions cartilagineuses
traumatiques ou dégénératives (arthrose), les lésions
méniscales, ligamentaires, tendineuses (ruptures, tendi-
nopathies mécaniques ou dégénératives). L’acquis scien-
tifique montre que ces stratégies thérapeutiques peuvent
être efficaces mais aussi que les processus impliqués
sont complexes et nécessitent encore la poursuite des re-
cherches tant sur les processus biologiques fondamentaux
– le concept de cellule souche ne cesse de se modifier
au fil des découvertes – que sur les protocoles thérapeu-
tiques. Néanmoins, ce type de thérapie a déjà franchi le
cap des applications cliniques. Dans ce domaine, nous en
sommes à la croisée des chemins entre la recherche et
l’utilisation « dans la vraie vie », dans la prise en charge
de nos patients.
LE CHIREC DANS LES THERAPIES CELLULAIRES OSTEOARTICULAIRES

MÉDECINE DE DEMAIN
14ITEMPO MÉDICAL – AVRIL 2016 – WWW.MEDIPRESS.BE
Sous l’action d’inducteurs spécifiques, les
CSM sont également capables de se diffé-
rencier en ténocytes qui sont des cellules
de tendons et de ligaments, et elles peuvent
aider à augmenter significativement la pro-
duction du collagène nécessaire pour la
reconstitution de ligaments et de tendons
solides et flexibles.
La principale complexité des greffes liga-
mentaires consiste à utiliser une matrice
de régénération qui est tolérée par l’orga-
nisme tout en permettant et favorisant la
réaction cellulaire appropriée ainsi que la
régénération tissulaire, avant d’être en-
suite éliminée de l’organisme de manière
naturelle. Cette matrice doit également
être capable de remplir la fonction du
LCA au cours de la reformation des tis-
sus, ce qui implique des spécifications
mécaniques bien particulières, tout en
permettant aux CSM de la coloniser et
d’y reconstituer une structure tissulaire
menant à un nouveau ligament. Pour que
celui-ci soit fonctionnel, il faut que les
CSM greffées possèdent au départ les
phénotypes adaptés.
Les ligaments et les tendons sont des tis-
sus denses formés d’un réseau cellulaire
tridimensionnel de fibroblastes (ligamento-
cytes et ténocytes), qui contient également
en faible quantité des chondrocytes. Ces
fibroblastes sont entourés d’une matrice
extracellulaire (MEC), dont ils assurent la
sécrétion. Ce sont les principales cellules
constituant les ligaments et les tendons
ainsi que la plupart des autres tissus
conjonctifs. Lorsque les CSM sont activées
et greffées sur la lésion ligamentaire, elles
se différencient et produisent des fibro-
blastes, qui jouent un rôle important dans
le renouvellement de la MEC et des colla-
gènes en sécrétant certaines enzymes, les
protéinases, lesquelles dégradent les colla-
gènes qu’il faut remplacer et participent à
l’homéostasie du tissu cellulaire.
Il y a actuellement trois catégories de
matériaux utilisables pour une matrice de
régénération ligamentaire : les matériaux
biologiques, les polymères d’origine natu-
relle et les polymères synthétiques bio-
résorbables. La matrice, qui joue le rôle
de support de régénération, doit être bio-
compatible et capable d’assurer la fonction
mécanique du tissu lorsqu’elle est desti-
née à être implantée avant la régénération
du ligament qui se fait parallèlement à sa
propre résorption. Il s’agit d’une prouesse
technique et technologique innovante, qui
se développe jour après jour et qui influera
sur les perspectives de la chirurgie ortho-
pédique, à l’avenir.
Vingt ans de recherches qui
nécessiteront encore beaucoup de
patience
Les recherches médicales se développent
de jour en jour, à tous niveaux. La théra-
pie cellulaire montre ses avancées dans
de nombreux domaines d’application, mais
sa validation nécessite des études qui
demanderont encore beaucoup de temps,
et de patience. Il faut éviter de conclure
trop rapidement à des perspectives miracu-
leuses nées d’une biotechnologie omnipo-
tente, et il faut également bien considérer
les besoins d’une médecine dont le coût
doit être accessible à tous. Au niveau pra-
tique, la thérapie cellulaire appartient donc
davantage au futur qu’au présent, mais il
n’en reste que son avenir semble très pro-
metteur. ■
Le CHIREC, qui est un des plus importants centres d’Or-
thopédie de Belgique, a décidé de s’impliquer dans l’appli-
cation clinique de ces thérapies nouvelles.
Le CHIREC a décidé que ces programmes devraient se
développer de façon responsable : proposer au patient
les choix thérapeutiques les plus performants mais aussi
les mieux validés. C’est pourquoi un comité spécifique
a été créé à l’initiative de certains médecins puis validé
par la direction générale pour encadrer ces thérapies. Le
« Comité CHIREC pour les thérapies régénératrice des af-
fections ostéoarticulaires » (le CCTROA) est composé des
chefs de pôles locomoteurs (le docteur Patrick Zygas pour
les sites Delta, Edith Cavell et Parc Léopold Basilique, le
docteur Bernard Geulette pour le site de Braine l’Alleud, et
le docteur Saussez pour les sites SARE = Ste Anne et St
Rémi) et de médecins représentant les différents sites. Il
a été mis sous la présidence du professeur Jean-Philippe
Hauzeur. Le CCTROA travaille en collaboration étroite, au
sein du CHIREC, avec les départements d’imagerie et de
biologie, la pharmacie et le comité d’hygiène.
Ces traitements sont dès à présent assurés par 18 pra-
ticiens spécialisés dans ces thérapies : orthopédistes,
médecins sportifs, radiologues, rhumatologues.
Une évaluation permanente des indications et des pro-
tocoles thérapeutiques a été mise en place, incluant un
suivi spécifique de tous les cas traités, des contrôles de
qualité des produits cellulaires utilisés et des séminaires
de discussion des pratiques et de la littérature.
Le CHIREC veut ainsi participer au développement d’un
programme de thérapies nouvelles et prometteuses dans
les affections ostéoarticulaires et les mettre à disposition
de notre population.
La thérapie cellulaire
appartient davantage
au futur qu’au présent,
mais son avenir semble
très prometteur.
1
/
5
100%