Un mobile autoporteur de masse m = 500g repose sur une table à

Un mobile autoporteur de masse m = 500g repose sur une
table à coussin d’air inclinée d’un angle =20,0°.
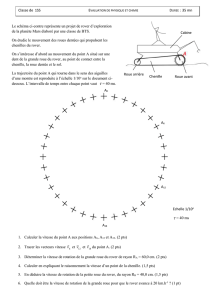
On lance le mobile vers le haut de la table, et grace à un dispositif approprié, on enregistre les
positions de son centre d’inertie à des intervalles de temps réguliers de durée = 20ms. Le
mobile décrit une trajectoire parabolique. (Voir feuille ci-contre)
1. Les forces appliquées au mobile se compensent-elles au cours du mouvement ? (Justifiez)
2. Claculer et tracer les vecteurs vitesse du mobile aux positions M7 et M9.
(Echelle 2cm pour 1m.s-1)
3. Tracer au point M8 le vecteur vitesse
v
tel que
v
=
9
v
-
7
v
.
Le mobile autoporteur au cours de son mouvement est soumis à deux forces : son poids
P
et la
réaction du support
R
4. Calculer l’intensité de ces deux forces appliquées au mobile et redessiner la figure ci-
dessous.en y faisant apparaître à l’échelle (1cm pour 1N) ces deux forces.
5. Tracer sur votre figure la force
F
tel que
F
=
P
+
R
.
6. Comparer
F
et
v
(Justifiez).
On s’interesse maintenant au travail des forces
P
et
R
.
7. Calculer le travail du poids
P
et de la force
R
de la position M0 à la position M12.
A l’aide d’un montage électrique simple, on mesure la conductance d’une solution électrolytique de
chlorure de potassium à 1,0.10-3mol.L-1
1. Faire un schéma de ce montage.
2. Pourquoi essaye-t-on de maintenir la tension U, dans ce montage, égale à 1,0V ?
La cellule conductiméttrique utilisée est formée de deux électrodes de cuivre, planes et parallèles,
de surface S égale à 1,70 cm² et distantes de l = 1,00 cm.
3. Calculer la conductance de cette solution si sa conductivité = 15,0mS.m-1
4. La conductivité molaire ionique de l’ion chlorure est Cl- = 7,6.10-3 S.m².mol-1, en déduire la
conductivité molaire ionique de l’ion potassium : K+
5. La solution de chlorure de potassium dont on a mesuré la conductance a été diluée 250 fois,
déterminer la concentration de la solution mère.
6. En déduire la masse de chlorure de potassium à peser pour préparer 250mL de solution
mère.
Physique
Intensité de pesanteur : g = 9,81 N.kg-1
Chimie
Massses molaires : MK=39,1g.mol-1 ; MCl=35,5g.mol-1
Contrôle de Physique / Chimie
Exercice 1
Exercice 2
1
/
1
100%