énoncé

CH 7 : REPRESENTATION DE QUELQUES MOLECULES
Notion contenu
Compétences expérimentales
- Formules développées et
semi-développées
- Utiliser des modèles moléculaires et des logiciels de représentation.
- Représenter des formules développées et semi-développées correspondant à des
modèles moléculaires.
- Savoir qu'à une formule brute peuvent correspondre plusieurs formules semi-
développées.
1. Les modèles moléculaires
Une molécule est un édifice chimique neutre formé par l’association d’un nombre précis d’atomes grâce à des liaisons
chimiques.
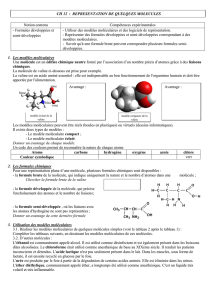
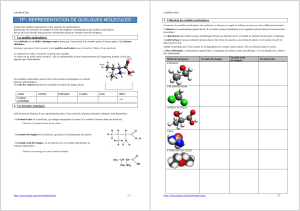
La molécule de valine ci-dessous est prise pour exemple.
La valine est un acide aminé essentiel : elle est indispensable au bon fonctionnement de l'organisme humain et doit être
apportée par l'alimentation.
Les modèles moléculaires peuvent être réels (boules en plastiques) ou virtuels (dessins informatiques).
Il existe deux types de modèles :
- Le modèle moléculaire compact ;
- Le modèle moléculaire éclaté.
Donner un avantage de chaque modèle.
Un code des couleurs permet de reconnaître la nature de chaque atome
Atome
carbone
hydrogène
oxygène
azote
chlore
Couleur symbolique
vert
2. Les formules chimiques
Pour une représentation plane d’une molécule, plusieurs formules chimiques sont disponibles :
- la formule brute de la molécule, qui indique uniquement la nature et le nombre d’atomes dans une molécule ;
Chercher la formule brute de la valine
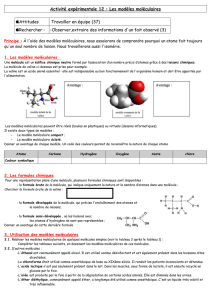
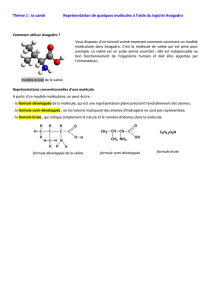
- la formule développée de la molécule, qui précise
l'enchaînement des atomes et le nombre de liaisons;
- la formule semi-développée , où les liaisons avec
les atomes d'hydrogène ne sont pas représentées ;
Donner un avantage de cette dernière formule
3. Utilisation des modèles moléculaires
3.1. Réaliser les modèles moléculaires de quelques molécules simples (voir le tableau 2 après le tableau 1) :
Compléter les tableaux suivants, en dessinant les modèles moléculaires de ces molécules.
3.2. D’autres molécules :
L'éthanol est communément appelé alcool. Il est utilisé comme désinfectant et est également présent dans les boissons
dites alcoolisées. Le chloroforme était utilisé comme anesthésique de base au XIXème siècle. Il rendait les patients
inconscients et détendus. L'acide lactique n'est pas seulement présent dans le lait. Dans les muscles, sous forme de
lactate, il est ensuite recyclé en glucose par le foie.
L'urée est produite par le foie à partir de la dégradation de certains acides aminés. Elle est éliminée dans les urines.
L'éther diéthylique, communément appelé éther, a longtemps été utilisé comme anesthésique. C'est un liquide très
volatil et très inflammable.
modèle compacte de la
valine
modèle éclaté de la
valine
blanc
roug
e
bleu
roug
e
noir
Avantage :
Avantage :

Molécules proposées
Formule développée
Formule semi-développée
Formule brute
ETHANOL
CHLOROPHORME
ACIDE LACTIQUE
UREE
ETHER DIETHYLIQUE
Molécule
Dihydrogène H2
HCl
Eau H2O
Ammoniac NH3
Formule développée
Molécule
Méthane CH4
Dioxygène O2
Diazote N2
CO2
Formule développée

4. Synthèse
A partir du travail fait précédemment, compléter le tableau :
Atome
carbone
hydrogène
oxygène
azote
chlore
N° Colonne dans la classification
Nombre de liaisons que fait
toujours l’atome
Nombre de cases qui sépare
l’élément du gaz rare le plus
proche dans le TPE
Comment peut-on expliquer cette observation ?
En déduire le nombre de liaisons des autres atomes du tableau
Atome
Fluor
Soufre
Silicium
azote
chlore
N° Colonne dans la classification
Nombre de liaisons que fait
toujours l’atome
Nombre de cases qui sépare
l’élément du gaz rare le plus
proche dans le TPE
5. Isomérie
Une formule brute donnée correspond-elle à une molécule unique ?
A l'aide du logiciel Avogadro, essayer d'apporter une réponse à cette question. On pourra travailler sur le cas de l'éthanol.
Remplir la dernière ligne du tableau précédent avec l’isomère de l’éthanol trouvé.
1
/
3
100%