série électrochimie

Collège Voltaire, chimie 3ème, 2015-2016
EXERCICES
Électrochimie
http://dcpe.net/POII/sites/default/files/cours%20et%20ex/ex-ch3- electrochimie .pdf
Table des matières
Série 10 Chimie / 3e / Électrochimie / février 2016.....................................................................................2
Rappel sur l'oxydoréduction (oxydant. réducteur,réduction, oxydation, etc.)..........................2
Prévoir les réactions (qui oxyde quoi ?)....................................................................................2
Introduire la notion de pouvoir oxydant/réducteur et de classement en fonction des potentiels
(E0) d'oxydoréduction des couples redox.................................................................................2
Série 11 Chimie / 3e / Électrochimie / février 2016.....................................................................................6
Déterminer les réaction qui ont lieu spontanément à l'aide des potentiels standards
d'oxydoréduction des couples redox.........................................................................................6
Utiliser les potentiels pour résoudre un problème pratique (en laboratoire ou dans la vie
courante)....................................................................................................................................6
Écrire les équations complètes (sous forme ionique et moléculaire) d'oxydoréduction...........6
Série 12 Chimie / 3e / Électrochimie / mars 2016.......................................................................................10
Introduire la notion de pile avec une expérience.....................................................................10
Comprendre le fonctionnement d'une pile..............................................................................10
Développer l'esprit critique.....................................................................................................10
Série 13 Chimie / 3e / Électrochimie / mars 2016........................................................................................11
Expliquer le fonctionnent d'une pile (schéma, légendes, réactions,etc. )................................11
Calculer le potentiel d'une pile................................................................................................11
Série 14 Chimie / 3e / Électrochimie / avril 2016........................................................................................15
Expliquer le fonctionnent de diverses piles (Volta, Leclanché,etc. )......................................15
Série 15 Chimie / 3e / Électrochimie / avril 2016........................................................................................19
Expliquer le but et le fonctionnent de l’électrolyse.................................................................19
Utiliser la loi de Faraday pour calculer la masse de substance fabriquée...............................19
Série 16 Chimie / 3e / Électrochimie / mai 2016.........................................................................................26
Comprendre et expliquer la corrosion des métaux et la manière de protéger les métaux de la
corrosion..................................................................................................................................26
www.dcpe.net/ eleve/ volt1234

Série 10 Chimie / 3e / Électrochimie / février 2016
Objectifs
✔Rappel sur l'oxydoréduction (oxydant. réducteur,réduction, oxydation, etc.)
✔Prévoir les réactions (qui oxyde quoi ?)
✔Introduire la notion de pouvoir oxydant/réducteur et de classement en fonction des potentiels
(E0) d'oxydoréduction des couples redox
http://dcpe.net/POII/sites/default/files/cours%20et%20ex/ex-ch3- electrochimie .pdf
Ex.1.
Soit les réactions :
Zn2+ + Cu
→
Zn + Cu2+
Zn + Cu2+
→
Zn2+ + Cu
a) Que pouvez vous observer ?
b) Quelle réaction est spontanée ?

Ex.2.
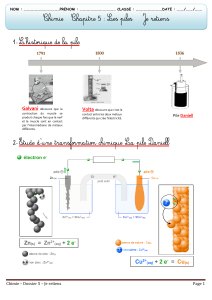
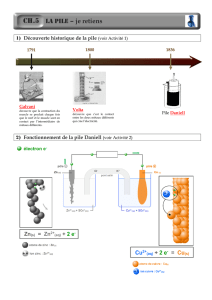
Lorsque l'on place un morceau de zinc dans une solution aqueuse de cuivre (II), du cuivre
métallique se dépose sur le zinc tandis qu'une partie de celui-ci se dissout.
Spontanément, deux électrons des atomes de zinc sont donnés aux atomes de cuivre.
a) Donnez l’équation de oxydoréduction. Donnez les deux couples redox.
Zn
Cu2+
Par contre, lorsqu’on place un morceau de cuivre dans une solution aqueuse de zinc (II),
aucun zinc métallique ne se dépose sur le cuivre.
b) Que pouvez-vous conclure sur la réaction précédente ?
c) Comment est-il possible de faire réagir le cuivre métallique et la solution de zinc (II) ?
Cu
Zn2+
Classification qualitative des couples redox

Si les réactions d’oxydation et de réduction sont réversibles, elles ne le sont pas dans
n’importes quelles conditions. Cela dépend du pouvoir d’oxydation ou de réduction des
substances mises en réaction.
Nous étudierons plusieurs couples et vérifierons expérimentalement quelles sont les
espèces qui réagissent spontanément entre elles. L’objet de l’étude est de connaître le
sens de la réaction spontanée entre 2 couples oxydant/réducteur.
Prenons, par exemple, les couples : Zn2+/Zn, Cu2+/Cu, Fe2+/Fe, Ag+/Ag et Mg2+/Mg et
préparons 5 solutions aqueuses contenant les ions suivants :
Zn2+ Cu2+ Fe2+ Ag+ Mg2+
Introduisons dans chacune de ces solutions le métal correspondant aux 4 autres couples
et voici les résultats obtenus.
Résultats
Les résultats sont notés : + (lorsque une réaction d’oxydoréduction a lieu)
- (pas de réaction)
Ion/Métal Ag Cu Fe Zn Mg
Ag++ + +
Cu2+ - + + +
Fe2+ - - + +
Zn2+ - - - +
Mg2+ - - - -
d) Quelle est la substance la plus oxydante ?
e) Classez-les dans l’ordre décroissant du pouvoir oxydant (du plus au moins oxydant).
f) Quelle est la substance la plus réductrice?

g) Classez-les dans l’ordre croissant du pouvoir réducteur.
Cette classification appelée classification électrochimique des métaux peut être
généralisée à d’autres couples. Elle permet de prévoir le sens des réactions d’oxydation
spontanée entre 2 couples oxydant/réducteur.
h) Classez-les substances précédentes sur les échelles ci-dessous
Échelles
i) Comparez avec les potentiels standards d’oxydoréduction de la table CRM (CRM, p.225)
et complétez :
- un potentiel élevé indique :
- un potentiel bas indique :
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
1
/
27
100%