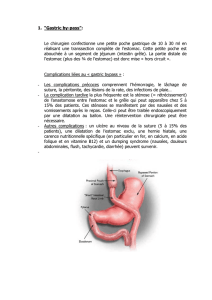
Adénocarcinome de l`estomac

Ad
enocarcinome
de l’estomac
Gastric adenocarcinoma
Pierre Michel, Isabelle Iwanicki-Caron
H^
opital Charles-Nicolle,
unit
e d’oncologie digestive,
service d’h
epatogastroent
erologie et nutrition,
1, rue de Germont,
76031 Rouen Cedex,
France
e-mail : <[email protected]>
R
esum
e
L’ad
enocarcinome de l’estomac se d
eveloppe sur des
l
esions induites par l’infection
aHelicobacter pylori (HP). Les
donn
ees r
ecentes permettent d’identifier des sujets
asymptomatiques
arisque
elev
e qui justifient d’une
surveillance endoscopique (^
age sup
erieur
a 60 ans, taux
bas de pepsinog
ene I, anticorps anti HP, ant
ec
edent familial
de cancer gastrique). Chez les sujets ayant une endoscopie,
l’utilisation syst
ematique du score OLGA fond
e sur l’analyse
histologique des biopsies antrales et fundiques est un
moyen d’identifier les sujets
a risque tr
es
elev
e. Le pronostic
du cancer de l’estomac reste grave et n
ecessite une
am
elioration de la qualit
e de la chirurgie avec un curage
ganglionnaire D1,5 analysant au moins 25 ganglions et des
traitements m
edicaux p
eriop
eratoires avec actuellement
un avantage
a la chimioth
erapie pour tous les patients
ayant une tumeur de stade II-III (T3 et/ou N+). En phase
m
etastatique, plusieurs protocoles de polychimioth
erapie
permettent d’augmenter la dur
ee de vie des patients. Il est
indispensable de chercher l’hyperexpression du r
ecepteur
HER2, pr
esente dans 15
a 20 % des cas, pour permettre
l’utilisation du trastuzumab (inhibiteur de HER2) en
association
a la chimioth
erapie. L’utilisation du trastuzu-
mab avec le 5 fluorouracile et le cisplatine permet
d’augmenter significativement la dur
ee de vie des patients.
nMots cl
es : ad
enocarcinome de l’estomac, gastrite
aHelicobacter
pylori, chirurgie, chimioth
erapie
Abstract
Adenocarcinoma of the stomach grows due to gastritis
lesions induced by infection with Helicobacter pylori (HP).
Recent data help to identify asymptomatic individuals at
high risk to justify endoscopy surveillance (age over
60 years, low serum pepsinogen I, antibodies to HP, family
history of gastric cancer). In those undergoing an
endoscopy, the routine use of OLGA score based on
histological analysis of antral and fundic biopsies is a way to
identify those at highest risk. The prognosis of stomach
cancer is serious and needs to improve the quality of surgery
with a D1,5 lymph node dissection, analyzing at least
25 lymph nodes and peri-operative medical treatment with
currently an advantage to chemotherapy for all patients
with tumor stage II-III (T3 and/or N+). In metastatic stage,
several chemotherapy regimens can increase the survival
time of patients. Currently, it is important to determine the
Pour citer cet article : Michel P, Iwanicki-Caron I. Ad
enocarcinome de l’estomac. H
epato Gastro 2011 ; 18 : 305-312. doi : 10.1684/
hpg.2011.0592
doi: 10.1684/hpg.2011.0592
305
HEPATO-GASTRO et Oncologie digestive
vol. 18 n83, mai-juin 2011
ossier th
ematiqueD
HEPATO
GASTRO
et Oncologie
digestive
Ad
enocarcinome
gastrique
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 26/05/2017.

Introduction
L’incidence du cancer de l’estomac diminue en France
depuis plus de 30 ans, mais son pronostic reste grave. Le
r^
ole de l’infection
aHelicobacter pylori (HP) est primordial
dans la canc
erog
en
ese de l’ad
enocarcinome de l’estomac.
La connaissance des m
ecanismes aboutissant
a
l’ad
enocarcinome doit aider le clinicien
as
electionner la
population
a risque justifiant d’une surveillance endosco-
pique. Une fois l’ad
enocarcinome constitu
e, la prise en
charge comporte le bilan pr
eth
erapeutique et la d
efinition
de la strat
egie de traitement. Il est utile de connaı
ˆtre
les
evolutions r
ecentes pour participer activement
ala
proposition de traitement d
efinie en r
eunion de concerta-
tion pluridisciplinaire d’oncologie digestive. L’h
epato-
gastroent
erologue occupe une place centrale dans le
diagnostic, le bilan et la prise en charge th
erapeutique de la
situation pr
ecanc
ereuse
a la phase m
etastatique.
Canc
erogen
ese appliqu
ee
a la gestion
du risque de cancer : la canc
erogen
ese
gastrique
Plusieurs facteurs favorisants la canc
erog
en
ese gastrique
ont
et
e identifi
es [1]. Les facteurs g
en
etiques, la consom-
mation de sel, de tabac, l’infection par le virus Epstein-Barr
p
esent pour 20 % alors que l’infection
aHPrepr
esente
80 % des facteurs de risque (figure 1). L’infection
aHPest
la premi
ere
etape du processus conduisant
al’ad
eno-
carcinome gastrique. Apr
es plusieurs d
ecennies, l’infection
a HP provoque une gastrite atrophique antrale et fundique.
L’
etape cl
eetirr
eversible est repr
esent
ee par l’apparition de
foyers de m
etaplasie intestinale au sein de la gastrique
chronique fundique. L’objectif principal du gastroent
e-
rologue est d’identifier puis de surveiller lespatients
a risque
elev
e de cancer.
‘‘ L’infection
aHelicobacter pylori
est la premi
ere
etape du processus
conduisant
a l’ad
enocarcinome gastrique’’
Chez les sujets asymptomatiques, plusieurs travaux
montrent que l’^
age sup
erieur
a 60 ans, le sexe masculin,
la pr
esence d’anticorps anti HP dans le s
erum et le taux
s
erique de pepsinog
ene I inf
erieur
a 70 ng/mL sont des
facteurs li
es au risque de cancer gastrique avec un risque
relatif multipli
e par six
a dix [2]. La pr
esence d’ant
ec
edents
familiaux repr
esente
egalement un facteur de risque
souvent n
eglig
e qui justifie l’
eradication syst
ematique
d’HP chez les apparent
es au premier degr
e d’un patient
porteur d’un ad
enocarcinome de l’estomac [3]. Il n’y a pas
de recommandation sur l’attitude
a proposer
a ce groupe
de sujets, mais il est raisonnable de proposer une
endoscopie digestive haute d
es le moindre doute clinique.
‘‘ La pr
esence d’ant
ec
edents familiaux
repr
esente un facteur de risque souvent
n
eglig
e qui justifie l’
eradication syst
ematique
de Helicobacter pylori chez les apparent
es au
premier degr
e d’un patient porteur d’un
ad
enocarcinome de l’estomac’’
En cas d’ant
ec
edent familial ou personnel de cancer de
l’estomac avant l’^
age de 50 ans et/ou de cancer lobulaire
du sein, il faut syst
ematiquement
evoquer une pr
edisposi-
tion h
er
editaire soit par mutation du g
ene de la E cadherine
(CDH1) soit dans le cadre d’un syndrome de Lynch et
pr
esenter le dossier en r
eunion de concertation pluridisci-
plinaire d’oncog
en
etique. Tr
es r
ecemment, une mise
a
jour des recommandations sur ce sujet a
et
e publi
ee [4].
Chez les sujets justifiant une endoscopie, il est recom-
mand
e de faire au moins cinq biopsies dans l’estomac en
overexpression of the HER2 receptor, present in 15-20% of
cases, to allow the use of trastuzumab (HER2 inhibitor) in
combination with chemotherapy. The use of trastuzumab
with 5 fluorouracil and cisplatin significantly increases the
survival time of patients.
nKey words: gastric adenocarcinoma, Helicobacter pylori gastritis,
surgery, chemotherapy
Hélicobacter pylori
Génétiques
Cancer
80 % + 20 %
Gastrite atrophique
Métaplasie intestinale
Autres (EBV,
alcool, tabac,...)
Figure 1. Les principaux facteurs de risque de l’ad
enocarcinome
gastrique d’apr
es Talley NJ [1].
306 HEPATO-GASTRO et Oncologie digestive
vol. 18 n83, mai-juin 2011
ossier th
ematiqueD
HEPATO
GASTRO
et Oncologie
digestive
Ad
enocarcinome
gastrique
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 26/05/2017.

l’absence de l
esion macroscopique, deux dans l’antre,
deux dans le fundus et une sur l’angulus [5]. En effet, le
risque de d
evelopper un ad
enocarcinome est li
e
a
l’intensit
e de la gastrite atrophique, mais
egalement
a
son si
ege
evalu
e par le score Operative Link on Gastritis
Assessement (OLGA) (tableau 1) [6]. Le si
ege fundique des
alt
erations de la muqueuse (gastrite de grade III,
m
etaplasie intestinale) est un signe important qui justifie
la surveillance endoscopique r
eguli
ere.
Les donn
ees r
etrospectives de la base de donn
ees
hollandaise montre que le risque de d
evelopper un
ad
enocarcinome gastrique en cas de m
etaplasie intestinale
est de l’ordre de 1,8 %
a dix ans [7]. Cependant, la
localisation de la m
etaplasie n’est pas pr
ecis
ee dans ce
travail. Il est probable que le risque est tr
es largement
sup
erieur en cas de m
etaplasie intestinale extensive
multifocale au sein de la muqueuse fundique. Ce travail
montre
egalement qu’en pratique, 28
a 38 % seulement
des sujets
a risque
elev
e sont surveill
es par endoscopie.
Est-il possible de r
eduire le risque de cancer par l’
eradication
d’HP alors que le processus de canc
erog
en
ese est avanc
e
(m
etaplasie intestinale, cancer in situ)?
La r
eponse est oui. L’
etude randomis
ee japonaise a
montr
e une diminution du risque de cancer apr
es
traitement endoscopique de cancer superficiel avec une
diminution du risque de 66 %
a trois ans (hazard ratio de
0,339 IC 95 % 0,157-0,729) [8]. Dans cette situation,
l’
eradication ne permet pas d’arr^
eter la surveillance
endoscopique mais diminue le risque de r
ecidive.
‘‘ L’estomac c’est comme le c^
olon il faut
surveiller les sujets
a risque
elev
e:
–homme de plus de 60 ans avec pespinog
ene
I inferieur
a 70 ng/mL et Ac anti HP ;
–sujet avec ant
ec
edent familial de cancer
de l’estomac ;
–et les sujets avec une gastrite OLGA III qui ont un
risque tr
es
elev
e’’
L’ad
enocarcinome gastrique
non m
etastatique
Le traitement endoscopique concerne les ad
enocarcino-
mes superficiels bien diff
erenci
es limit
es
a la muqueuse
sans envahissement vasculaire ou lymphatique, quel que
soit le type histologique [9].
Le traitement curatif du cancer gastrique repose sur la
r
esection chirurgicale compl
ete de la tumeur primitive et
des territoires de drainage lymphatique. En cas de r
esection
histologiquement compl
ete (R0), le principal facteur
pronostique est la pr
esence d’un envahissement ganglion-
naire. La survie
a cinq ans est de 60
a 80 % en l’absence
d’envahissement ganglionnaire et de 15
a30%en
pr
esence d’un envahissement ganglionnaire [10]. La
connaissance du statut ganglionnaire d
epend du nombre
de ganglions examin
es et du site du curage [11]. Deux
etudes r
ecentes sugg
erent que les pratiques
evoluent avec
une augmentation du nombre de ganglions d
etect
es sur les
pi
eces op
eratoires et une am
elioration de la survie [12, 13].
Les donn
ees des
etudes de phase III europ
eennes r
ecentes
fournissent une estimation du r
esultat d’un traitement
chirurgical seul. L’influence de la qualit
e de l’acte
chirurgical est majeure avec des r
esultats de survie
a
cinq ans qui varient de 23
a 49 % pour des tumeurs de
stade
egal [14, 15].
‘‘ L’influence de la qualit
e de l’acte chirurgical
est majeure avec des r
esultats de survie
a
cinq ans qui varient de 23
a 49 % pour des tumeurs
de stade
egal’’
En pratique, la grande majorit
e des malades op
er
es en
France ont un ad
enocarcinome gastrique de stade
sup
erieur ou
egal
a IIA de la classification UICC (en
pratique N+ et/ou T 3). L’am
elioration des pratiques
chirurgicales avec l’adoption syst
ematique du curage
Tableau 1.
Evaluation du risque de cancer de l’estomac en fonction de l’intensit
e de la gastrite atrophique et
de son si
ege dans l’estomac. Score OLGA selon Rugge M et al. [6].
Corps
Score d’atrophie Pas d’atrophie Atrophie l
eg
ere Atrophie mod
er
ee Atrophie s
ev
ere
(score 0) (score 1) (score 2) (score 3)
Antre Pas d’atrophie Stade 0 Stade I Stade II Stade II
Antre Atrophie l
eg
ere Stade I Stade I Stade II Stade III
Antre Atrophie mod
er
ee Stade II Stade II Stade III Stade IV
Antre Atrophie s
ev
ere Stade III Stade III Stade IV Stade IV
307
HEPATO-GASTRO et Oncologie digestive
vol. 18 n83, mai-juin 2011
ossier th
ematique Mise-au-pointD
HEPATO
GASTRO
et Oncologie
digestive
Ad
enocarcinome
gastrique
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 26/05/2017.

D1,5 (25 ganglions examin
es) peut permettre d’esp
erer
un risque de r
ecidive de l’ordre de 50 %. Pour
descendre sous ce seuil. Il est n
ecessaire d’envisager
des traitements compl
ementaires
a la chirurgie adapt
es
aux sites de r
ecidive de la maladie. Les curages extensifs
D2 ou D3 n’ont pas montr
e d’effet b
en
efique sur la
survie [16].
Curage des ganglions p
eri-gastriques : D1 (en pra-
tique sup
erieur
a 15 ganglions)
Curage des ganglions p
eri-gastriques et r
egionaux :
D2 (en pratique sup
erieur
a 25 ganglions plus
spl
enectomie)
Curage des ganglions p
eri-gastriques et r
egionaux
sans spl
enectomie : D1,5
Les sites de r
ecidive apr
es une chirurgie
a vis
ee curative
(R0) ont
et
e
etudi
es dans deux grandes s
eries asiatiques
comportant plus de 500 patients op
er
es selon une
proc
edure rigoureuse [17, 18]. La r
ecidive
etait locor
e-
gionale dans 32,5 %, p
eriton
eale dans 45,9 % et
h
ematog
ene (
a distance) dans 34,2 % des cas. Pour le
sous-groupe des tumeurs T3 la r
ecidive
etait locor
egionale
dans 66 % des cas et pour les tumeurs N1-2 la r
ecidive
etait locor
egionale dans plus de 30 % des cas. Cette
analyse justifie l’
evaluation de traitements syst
emiques et
locor
egionaux associ
es
a la chirurgie.
L’efficacit
e de la chimioth
erapie syst
emique a
et
e
evalu
ee
en utilisation postop
eratoire (adjuvante) et en utilisation
p
eriop
eratoire (pr
e- et postop
eratoire).
Une m
eta-analyse des donn
ees individuelles de 17 essais
portant sur 3 838 patients montre un effet b
en
efique de
la chimioth
erapie postop
eratoire
a base de 5 fluorouracile
avec une diminution du risque de d
ec
es de 18 % (hazard
ratio 0,82 IC 95 % : 0,76-0,90, p<0,001) [19]. Pour
les
etudes europ
eennes, l’effet b
en
efique reste statisti-
quement significatif (hazard ratio 0,83 IC 95 % :
0,74-0,94).
Deux
etudes randomis
ees ont
evalu
e la chimioth
erapie
p
eriop
eratoire. Une
etude britannique multicentrique
randomis
ee [15] a
evalu
e l’int
er^
et d’une chimioth
erapie
pr
e et postop
eratoire par epirubicine-cisplatine-5FU
versus chirurgie seule. Les risques de r
ecidive et de d
ec
es
etaient significativement diminu
es dans le bras chi-
mioth
erapie de respectivement 30 et 25 %, avec des
hazard ratio de 0,7 (IC 95 % 0,56-0,88) p= 0,002 et
0,75 (IC 95 % 0,60-0,93) p= 0,009. Le taux de survie
a
cinq ans des patients du groupe chirurgie seule
etait
particuli
erement faible (23 %) et les crit
eres de qualit
ede
la chirurgie n’
etaient pas connus. La survie du groupe
chimioth
erapie et chirurgie
etait de 36 %
a cinq ans. Une
etude franc¸aise, multicentrique randomis
ee, a compar
ela
chirurgie seule
a la chirurgie encadr
ee de deux cures de
chimioth
erapie par 5 fluorouracile et cisplatine. Parmi les
224 patients inclus, 64 % avaient une tumeur du cardia.
Les risques de r
ecidive et de d
ec
es
etaient significative-
ment diminu
es dans le groupe chimioth
erapie de 35 et
21 % respectivement, avec des hazard ratio de 0,65
(IC 95 % 0,48-0,89) et 0,69 (IC 95 % 0,50-0,95). Le
pourcentage de patients vivants sans r
ecidive
a cinq ans
etait significativement sup
erieur dans le groupe chi-
mioth
erapie (34 vs 17 %, p= 0,018) [20]. Cette strat
egie
de chimioth
erapie p
eriop
eratoire est r
ealisable en routine,
dans les deux
etudes la chimioth
erapie pr
eop
eratoire
a
et
er
ealis
ee chez plus de 85 % des patients et la
chimioth
erapie postop
eratoire n’a
et
e possible que dans
40 % des cas.
Parmi les traitements locor
egionaux, la radioth
erapie a
et
e
la plus
evalu
ee.
La radioth
erapie perop
eratoire est une technique
s
eduisante, mais son accessibilit
e est toujours r
eduite
en raison de la lourdeur du plateau technique n
ecessaire.
La radiochimioth
erapie postop
eratoire a
et
evalid
ee par les
r
esultats de l’
etude am
ericaine publi
ee en 2001 [21]. La
population
etudi
ee
etait compos
ee de l
esions T3 dans plus
de 60 % des cas avec un envahissement ganglionnaire
dans 85 % des cas.
A trois ans, les risques relatifs de
r
ecidive et de d
ec
es en l’absence de traitement adjuvant
etaient augment
es respectivement de 52 (hazard ratio 1,52
IC 95 % 1,23-1,86) et 35 % (hazard ratio 1,35 IC 95 %
1,09-1,66). La survie sans r
ecidive
a trois ans
etait de 31 %
dans le bras chirurgie contre 48 % dans le bras chirurgie
plus radiochimioth
erapie. La survie globale
a trois ans
etait
de 41 % dans le bras chirurgie seule et de 50 % dans le
bras chirurgie plus radiochimioth
erapie. L’analyse de la
courbe de survie du bras chirurgie montre que la survie
globale
a cinq ans est de l’ordre de 30 %. Ce r
esultat a
et
e
obtenu alors que 54 % des patients avaient
et
eop
er
es de
mani
ere suboptimale (lymphadenectomie inf
erieur
aD1).
R
etrospectivement, l’index de Maruyama a
et
ecalcul
e.
Cet index permet d’estimer la probabilit
e d’envahissement
des stations ganglionnaires de la classification japonaise,
a
partir de donn
ees cliniques et anatomopathologiques
simples. L’index moyen tr
es
elev
etrouv
e dans la population
de l’
etude am
ericaine signifie qu’une proportion impor-
tante, estim
ee
a 70 % des patients, a eu une r
esection
incompl
ete laissant en place du tissu ganglionnaire
m
etastatique [22]. La radiochimioth
erapie postop
eratoire
a donc d
emontr
e son efficacit
e dans la population des
patients op
er
es de mani
ere suboptimale d’un cancer de
l’estomac. Une
etude de registre r
ealis
ee au Canada
sur plus de 4 000 patients trait
es par chirurgie ou
chirurgie puis radiochimioth
erapie semble confirmer
308 HEPATO-GASTRO et Oncologie digestive
vol. 18 n83, mai-juin 2011
ossier th
ematiqueD
HEPATO
GASTRO
et Oncologie
digestive
Ad
enocarcinome
gastrique
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 26/05/2017.

l’int
er^
et de la radiochimioth
erapie postop
eratoire. Les
hazard ratio
etaient de 0,71, p= 0,000 7 et 0,66,
p<0,000 1 respectivement pour les stades III et IV (M0)
de [23].
‘‘ La radiochimioth
erapie postop
eratoire
ad
emontr
e son efficacit
e
dans la population des patients op
er
es
de mani
ere suboptimale d’un cancer
de l’estomac’’
Qu’en est-il chez les patients op
er
es avec un curage
ganglionnaire optimal ? Une
etude cor
eenne compara-
tive, prospective sur 990 patients mais non randomis
ee
apporte une partie de la r
eponse avec un niveau de preuve
faible. Dans ce travail, le traitement postop
eratoire
comportait une radiochimioth
erapie selon les m^
emes
modalit
es que dans l’
etude am
ericaine (45 Gy, 5 Fluoru-
racile bolus et acide folinique). Le groupe chirurgie seule
etait compos
e de patients s
electionn
es pour la radio-
chimioth
erapie dont l’entourage avait refus
e le traitement
postop
eratoire. [24]. Dans les deux groupes, l’analyse du
statut ganglionnaire a port
e sur plus de 25 ganglions chez
respectivement 85 et 87 % des patients. Le b
en
efice en
faveur du groupe radiochimioth
erapie a
et
e trouv
e pour la
survie globale
a cinq ans dans le groupe des stades IIIA
(61,6 vs 43,9 %, p= 0,001 3) et IIIB (40,8 vs 20,5 %,
p= 0,004 5) avec un hazard ratio respectivement de 0,60
(IC 95 % 0,43-0,83) et 0,53 (IC 95 % 0,34-0,84). Ces
r
esultats plaident en faveur d’un effet b
en
efique de la
radiochimioth
erapie dans la population des patients
op
er
es avec un curage ganglionnaire sup
erieur
a D1.
Cependant, ce traitement pr
esente des limites. Lazagne
R
ecemment, l’inefficacit
e de la radiochimioth
erapie post-
op
eratoire a
et
e sugg
er
ee pour les ad
enocarcinomes
a
cellules ind
ependantes [25]. Enfin, il est indispensable de
rappeler que la radiochimioth
erapie postop
eratoire ne
peut ^
etre r
ealis
ee que chez des patients en
etat g
en
eral
et nutritionnel satisfaisant. Dans les
etudes am
ericaine
et cor
eenne, les patients n’
etaient
eligibles que si
l’apport calorique quotidien
etait sup
erieur
a1500kcal.
Cette pr
ecaution doit ^
etre maintenue pour
eviter de
r
ealisercetypedetraitement
adespatientsd
enutris et
les exposer
a des complications s
ev
eres [26]. Cette
limite ne permet pas de connaı
ˆtrelafaisabilit
edela
radiochimioth
erapie postop
eratoire sur une population
de patients op
er
es d’un cancer de l’estomac. En effet,
dans l’
etude am
ericaine la randomisation
etait pratiqu
ee
en postop
eratoire chez des patients aptes
a recevoir le
traitement.
La radiochimioth
erapie pr
eop
eratoire pr
esente l’avantage
th
eorique d’^
etre r
ealisable chez tous les malades op
era-
bles d’un ad
enocarcinome de l’estomac. Cette strat
egie
pr
eop
eratoire a
et
e
evalu
ee dans un petit nombre d’
etudes
de phase II [27-29]. La dose totale de radioth
erapie utilis
ee
est de 45 Gy en
etalement classique, dans les trois
etudes. Les sch
emas de chimioth
erapie ont associ
edu
5 fluorouracile et du cisplatine plus ou moins paclitaxel
avec de mani
ere concomitante
a la radioth
erapie du 5FU en
perfusion continue associ
ee ou non
a du paclitaxel. La
faisabilit
edessch
emas
etudi
es
etait sup
erieure ou
egale
a80%.Uner
eponse compl
ete histologique a
et
e
constat
ee dans plus de 20 % des cas. Cependant, une
toxicit
e grade 4 est rapport
ee chez plus de 20 % des
patients. La progression m
etastatique sous la forme
d’une carcinose p
eriton
ealeestlaprincipalecausede
non-r
esection de la tumeur chez les patients trait
es par
radiochimioth
erpaie pr
eop
eratoire [30]. Cette option
th
erapeutique ne doit pas ^
etre utilis
ee en dehors d’une
etude clinique.
‘‘ La chimioth
erapie p
eriop
eratoire est
actuellement le traitement efficace le plus
s^
ur pour diminuer le risque de r
ecidive
postop
eratoire. En pratique on peut utiliser soit
trois cycles d’ECF (
epirubicine-cisplatine-5FU) ou
d’EOX (
epirubicine-oxaliplatine-capecitabine) soit
quatre cycles de LV5FU2 cisplatine avant et apr
es
la chirurgie. Les deux solutions se r
ealisent
sur 42 jours (trois cycles de 21 jours ou quatre
de 14 jours)’’
L’ad
enocarcinome de l’estomac
m
etastatique
En dehors de situations sp
ecifiques (h
emorragie, obstruc-
tion), la chirurgie n’est pas envisag
ee. La question reste
cependant non r
esolue dans quelques rares cas de
m
etastases h
epatiques facilement r
es
ecables parfaite-
ment stables sous chimioth
erapie.
La chimioth
erapie syst
emique doit ^
etre envisag
ee avec le
patient si son
etat g
en
eral le permet (activit
e au moins
50 % de la journ
ee). L’effet des poly-chimioth
erapies a
et
ed
emontr
e mais reste modeste avec des m
edianes de
survie dans les
etudes randomis
ees qui restent inf
erieures
a 12 mois. Il est indispensable d’int
egrer ce traitement
a
un projet personnel du patient, ce travail doit ^
etre fait en
consultation lors de la pr
esentation du plan personnalis
e
de soin. Les principaux protocoles de chimioth
erapie
recommand
es dans le th
esaurus national de canc
erologie
309
HEPATO-GASTRO et Oncologie digestive
vol. 18 n83, mai-juin 2011
ossier th
ematique Mise-au-pointD
HEPATO
GASTRO
et Oncologie
digestive
Ad
enocarcinome
gastrique
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 26/05/2017.
 6
6
 7
7
 8
8
1
/
8
100%