Le MSOME - TECHNIQUES

Le
p
e
t
it
gu
i
de
d
e
s
techniques
d
'
A
MP
Copyright 2012 – EKE – Le 10 mai 2013

Sommaire
L’IA ou IAD
La FIV
La FIV Don d'ovocytes
L’ICSI
L'IMSI
Le MSOME
Le PICSI
La MACS
La Fragmentation de l'ADN des spermatozoïdes
L'embryoscope
L'EmbryoGEN
Le blastocyste
Le Hatching

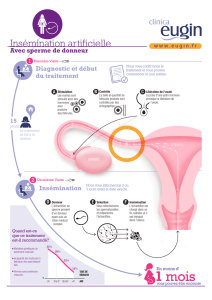
Insémination Artificielle
L’insémination artificielle est une technique simple.
Elle consiste à déposer les spermatozoïdes, préalablement
préparés en laboratoire,
dans
la
cavité utérine, au moment
de l'ovulation.
Nous parlons souvent d’une :
IAC – Insémination artificielle
avec sperme du conjoint
IAD – insémination artificielle
avec sperme du donneur

Insémination Artificielle
Cette technique comporte trois phases:
Un
processus de stimulation de l'ovulation
L'insémination peut parfois être réalisée sur un cycle spontané. Cependant plus fréquemment, les
médecins préfèrent aider les ovaires à fabriquer des ovocytes. Dans ce but, la femme recevra pendant la
première moitié du cycle un traitement inducteur de l’ovulation dont les effets seront suivis en effectuant
une échographie et des dosages hormonaux. On injectera ensuite à la femme de l'HCG (hormone
gonadotrope chorionique) en milieu de cycle pour déclencher l'ovulation. L'insémination sera en général
entreprise, 36 heures après le pic de LH ou l'injection d'HCG.
Un
processus de sélection des spermatozoïdes
Le jour de l‘insémination, le conjoint remet un échantillon de sperme au laboratoire. Ce sperme est traité
de manière à récupérer les spermatozoïdes mobiles et à les concentrer dans un volume réduit (IAC).
Pour IAD le sperme vient de la banque de sperme et est préparé de la manière que celui du conjoint.
Un
processus d'Insémination
L'insémination est un geste simple et indolore, qui est effectué sur une patiente allongée en position
gynécologique. Il consiste à introduire un fin cathéter, relié à la seringue contenant le sperme, à l'intérieur
de la cavité utérine pour y déposer environ un ml de sperme préparé au laboratoire (insémination intra-
utérine).
Après l'insémination, il suffit que la femme reste allongée 10 à 30 minutes et elle peut ensuite reprendre
une vie normale.
ATTENTION !
Pour les femmes de +38 ans le taux de réussite d’une IAD est très faible

Fécondation In Vitro
La Fécondation "In Vitro" est une technique complexe qui exige expérience et
technologie. Ce procédé consiste à féconder les ovocytes de la patiente, au laboratoire,
avec le sperme du conjoint, du compagnon ou du donneur. Les embryons obtenus au
moyen de cette fécondation sont alors transférés à l'utérus de la patiente.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
1
/
25
100%