1 Protection myocardique per ou post opératoire de la Tétralogie de

....................................................................................................................................................................................
Le cahier du CCM - janvier 2012 1
Présentation du mois
Prochainement
Les malades en insufsance cardiaque réfractaire au traitement
médical, représentent l’évolution naturelle de l’insufsance
cardiaque.
Les indications de transplantations sont extrêmement limitées ;
d’une part, compte tenu du nombre faible de donneurs, d’autre
part, compte tenu de la fréquence élevée de pathologies
associées (diabète, insufsance rénale, obésité, etc …) contre-
indiquant la transplantation cardiaque.
Depuis peu, les pompes d’assistance circulatoire électriques,
représentent une option réaliste pour traiter l’insufsance
cardiaque réfractaire et permettre à des malades de mener une
vie normale.
Parmi ces pompes, l’évolution a été extrêmement rapide ; nous
sommes passés de la pompe pulsatile bi ventriculaire, mimant le
cœur humain (JARVIK 7), aux pompes uni ventriculaire gauche,
pulsatile, type NOVACOR ou TCI, puis aux pompes à ux axial
continu, mono ventriculaire JARVIK 2000 et THORATEC.
L’avantage du JARVIK
2000 réside dans son
extrême simplicité, avec peu
d’électronique embarquée,
permettant d’avoir une abilité
très importante.
Aucune panne mécanique
n’a été, jusque ici, décelée
sur plusieurs centaines
d’implantations, au court et au long termes.
L’assistance circulatoire la plus longue a été de 8 ans, le malade
étant décédé d’un cancer.
La mise en place d’une prise électrique derrière l’oreille évite
toute infection chronique due à la sortie du système par voie
abdominale, et c’est le seul système qui présente cet avantage
sur tous les autres.
Le Centre Cardio-Thoracique, dèle à sa tradition d’innovation,
a débuté en Juillet 2011, un programme d’implantation
d’assistance circulatoire chronique, en alternative à la
transplantation cardiaque.
Nous avons implanté jusqu’ici deux patients qui vont bien, et
notre but est d’en implanter, selon les besoins de la région, 8 à
10 par an.
Permettez-moi, à l’occasion de cet éditorial, de vous présenter à
vous-même comme à ceux qui vous sont chers, tous mes vœux
pour l’Année 2012.
Professeur Gilles DREYFUS.
p 1
p 1 à 3
p 3 à 4
p 4
Edito du Pr. Gilles Dreyfus ......................................................................................................................................................................
Embryologie et anatomopathologie de l’anomalie d’Ebstein ................................................................................................................
Doute entre cardiomyopathie hypertrophique asymétrique et tumeur cardiaque ................................................................................
Dilatation de l’aorte ascendante : quand faut-il opérer ? ........................................................................................................................
19 janvier 2012
Protection myocardique per ou post
opératoire de la Tétralogie de Fallot.
P. Mauriat (Bordeaux)
n°39
jan. 2012
EDITO
16 février 2012
Endocardite infectieuse.
G. Habib (Marseille)
+ Embryologie et anatomopathologie de l’anomalie d’Ebstein*
Résumé de la séance précédente :
Embryologie
L’anomalie d’Ebstein est due à un arrêt dans le développement
normal de la tricuspide. Les différentes formes anatomiques
dépendent du stade auquel survient cet arrêt.
La valve tricuspide se forme à partir de l’entonnoir tricuspidien,
excavation de la partie postérieure du myocarde de l’anneau
primitif permettant d’établir la connexion atrioventriculaire droite
(Figure 1). L’entonnoir tricuspidien est également à l’origine de
la bande modératrice du ventricule droit et du pilier antérieur de
la tricuspide (la bande septale provenant de l’anneau primitif, et
la bande pariétale de la ventriculo-infundibular fold, c’est-à-dire
de la courbure interne). Cet entonnoir est composé de
+ L’assistance circulatoire mécanique permanente : une alternative réaliste ou non à la
transplantation cardiaque ?

....................................................................................................................................................................................
Le cahier du CCM - janvier 2012
2
3 parois : la paroi antérieure, libre dans la cavité ventriculaire
droite, dont proviendra le feuillet antérieur de la tricuspide ; la
paroi postéro-inférieure est celle du ventricule droit et donnera
le feuillet inférieur ; la paroi septale est représentée par le
septum interventriculaire et donnera le feuillet septal. La face
interne des 3 parois de l’entonnoir tricuspidien est tapissée
par le mésenchyme des bourgeons endocardiques du canal
atrioventriculaire. Les 3 feuillets tricuspides vont se former par
délamination à partir des parois de l’entonnoir tricuspidien.
Chronologiquement, le feuillet antérieur de la tricuspide apparaît
en premier (8ème semaine de vie intra-utérine), à partir de la
partie antérieure de l’entonnoir tricuspidien, par disparition
(apoptose) des cellules myocardiques de cette paroi. Le feuillet
inférieur apparaît immédiatement après par délamination à
partir du myocarde de la paroi postéro-inférieure (séparation
du mésenchyme des bourgeons et de la paroi du VD), puis en
dernier le feuillet septal (10 semaines de vie intra-utérine). La
délamination des feuillets inférieur et septal progresse de bas
en haut.
La délamination des feuillets se produit en même temps que la
formation des piliers à partir du myocarde ventriculaire, l’orice
de la valve tricuspide devient alors inférieur et l’orice primitif
devient la commissure antéroseptale.
Les arrêts du développement de la tricuspide au stade le plus
tardif correspondront aux anomalies d’Ebstein les moins sévères
anatomiquement : défaut de délamination du feuillet septal
seul. Les formes de survenue un peu plus précoce associent
un défaut de délamination des feuillets septal et inférieur, avec
atrialisation de l’inlet du ventricule droit. Les formes les plus
sévères découlent d’un arrêt du développement au stade de
l’entonnoir tricuspidien, au moment de la formation du feuillet
antérieur, alors que l’orice de la tricuspide est antérieur, dirigé
vers la chambre de chasse : anomalies sévères du feuillet
antérieur, pas de délamination des deux autres feuillets.
Anatomie
1. Ebstein : dénitionggggggggggggggggggggggggggggg
La dénition classique de l’anomalie d’Ebstein est l’insertion
basse de la tricuspide, le déplacement vers le bas (accolement)
de l’insertion proximale des feuillets tricuspidiens par défaut
de délamination. En réalité, cette dénition ne s’applique
qu’aux feuillets septal et inférieur de la tricuspide. L’insertion
proximale du feuillet antérieur est toujours normale, sur
l’anneau tricuspide, la « délamination » du feuillet antérieur
se faisant par disparition des cellules myocardiques de la
paroi antérieure de l’entonnoir tricuspidien, qui s’étend de la
ventriculo-infundibular fold en haut jusqu’à la future bande
modératrice en bas.
2. Feuillets inférieur et septalggggggggggggggggggggg
Leur insertion proximale est toujours déplacée vers le bas.
Leur point de déplacement maximal est représenté par la
commissure entre ces deux feuillets, correspondant au noyau
breux central ou croix du cœur. La discontinuité qui se produit
alors entre la croix du cœur déplacée vers le bas et l’anneau
atrioventriculaire explique la fréquence des anomalies des voies
de conduction associées, en particulier l’existence de voies
de conduction accessoires, très fréquentes dans l’Ebstein.
Le déplacement des feuillets inférieur et septal ne va jamais
au-delà de la jonction entre inlet (chambre d’admission) et
portion trabéculée (ou apex) du ventricule droit. Cette jonction
est souvent marquée dans cette anomalie par un éperon bro-
musculaire anormal, qui n’est autre que l’extrémité inférieure
de l’entonnoir tricuspidien. Ces anomalies d’insertion
proximale ont pour conséquences le déplacement vers le
bas (et dans les formes les plus sévères, vers l’avant) de
l’orice tricuspide effectif, à la jonction de l’inlet et de la partie
trabéculée du ventricule droit, mais aussi une dilatation souvent
majeure de l’oreillette droite, et de l’anneau tricuspide. L’inlet
peut se retrouver alors intégré à l’oreillette, c’est ce qu’on
appelle l’atrialisation de l’inlet du ventricule droit, avec une
paroi souvent amincie due à l’absence partielle de myocarde.
Le degré d’atrialisation dépend de l’étendue du défaut de
délamination (accolement) du feuillet inférieur de la tricuspide.
L’anneau fonctionnel de la tricuspide est
verticalisé, déplacé vers l’avant et vers le bas.
Les feuillets déplacés sont de taille très variable et souvent
dysplasiques, pouvant être réduits (surtout le feuillet septal) à
de petites excroissances en forme de chou-eur.
3. Feuillet antérieurgggggggggggggggggggggggggggggg
Au contraire des deux autres valves, l’insertion proximale
de la valve antérieure est presque toujours normale c’est-
à-dire non déplacée. Ce sont ses attaches distales qui
sont le plus souvent anormales, ainsi que sa structure elle-
même : elle est souvent trop large, parfois muscularisée,
avec une fusion des espaces interchordaux. Leung a
décrit trois types d’insertion distale de la valve antérieure,
reliés à la clinique c’est-à-dire aux conséquences sur le
fonctionnement de la valve tricuspide, fuite ou sténose :
- insertion focale, c’est-à-dire normale sur les piliers,
avec des commissures bien formées et un orice
inférieur libre – en général la valve ne fuit pas ;
- insertion discontinue avec de multiples attaches directes
à la paroi (« tethering») sans interposition de piliers, ou
bien fenestrations de la valve – c’est dans ces formes
que l’on trouve le plus souvent les fuites valvulaires ;
- insertion linéaire sur un éperon musculaire anormal à la
jonction inlet-apex du ventricule droit, le feuillet antérieur
est alors nommée « sail-like », tendu comme une voile de
bateau entre la bande pariétale en haut (insertion proximale
normale) et l’éperon musculaire anormal à la jonction inlet-
apex en bas - la valve peut alors fuir ou être sténosante.
Ce sont donc la taille et l’insertion distale du feuillet antérieur
qui vont déterminer la fonction de l’orice tricuspide effectif, et
la sévérité de la maladie. Ceci correspond à la classication
de l’équipe de Broussais, où les formes les plus sévères sont
celles où la mobilité de la valve antérieure est la plus réduite.
Dans les formes extrêmes d’Ebstein correspondant au type D
de la classication de Broussais, le feuillet antérieur est attaché
de façon linéaire sur l’éperon breux anormal et l’orice
Fig. 1

....................................................................................................................................................................................
Le cahier du CCM - janvier 2012 3
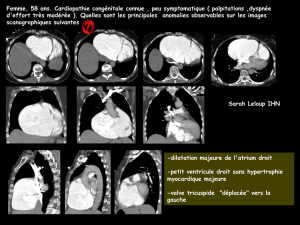
Il s’agit d’une patiente de 55 ans, asymptomatique mais porteuse
de facteurs de risque coronariens (hérédité coronarienne
précoce, dyslipidémie traitée par Crestor), adressée pour
réalisation d’une IRM adénosine, un scanner coronarien
n’ayant pas pu conclure du fait de calcications importantes.
à l’interrogatoire, la patiente fait mention d’une soeur porteuse
de cardiomyopathie hypertrophique.
A l’IRM, l’attention a été attirée par la présence d’une image
globalement arrondie, mais discrètement irrégulière semblant
appendue au niveau de la paroi antéro-septale. Cette image
inhabituelle est bien visible sur les coupes ciné « petit axe »
(g. n°1).
Deux diagnostics ont été évoqués : d’une part une
cardiomyopathie hypertrophique asymétrique de localisation
inhabituelle (formation irrégulière localisée non pas au niveau
de la paroi septale, mais au niveau de la paroi antéro-basale),
et d’autre part une tumeur cardiaque prolabant dans la cavité
ventriculaire gauche. L’utilisation des séquences IRM de type
«tagging» a permis de faire la différence.
Le tagging (ou tatouage) myocardique (g. n°2) permet,
comme le speckle tracking en échographie, de mesurer les
déformations myocardiques dans toutes les directions. Le
concept de tagging a été introduit en 1988 par Zerhouni et Axel.
Il s’agit d’appliquer des lignes ou des grilles de saturation dans
le plan de coupe au moment où survient l’onde R de l’ECG (n
de la diastole mécanique), an de pouvoir suivre la déformation
de ces lignes (d’hyposignal) en systole lors de la contraction
cardiaque. La persistance des motifs de tagging durant les 20 à
40 images décrivant
le cycle cardiaque
(résolution temporelle
de l’ordre de 30 ms)
permet d’analyser
les déplacements
myocardiques liés à
la contraction et à la
relaxation.
Dans le cas de
notre patiente, nous
constatons avec
les séquences de
«tagging», une
contractivité au
niveau de la zone
étudiée (g. n°3).
Nous avons conclu à
une cardiomyopathie
hypertrophique
asymétrique, plutôt
qu’à une tumeur
cardiaque. Nous
avons été confortés dans ce sens, du fait de
la présence d’un rehaussement tardif intra-myocardique focale,
après injection de Gadolinium, dans la zone de l’hypertrophie,
aspect en faveur d’une cardiomyopathie.
Par ailleurs, en réanalysant le scanner coronarien, plusieurs
faux tendons étaient visibles dont un volumineux reliant le
muscle papillaire antéro-supérieur et le septum. (g. n°4).
M.R.I
Cas cliniques du mois au C.C.M. :
* Références principales :
1. Leung MP, Baker EJ, Anderson RH, Züberbühler JR. Cineangiographic spectrum of Ebstein’s malformation : its relevance to clinical
presentation and outcome. J Am Coll Cardiol 1988 ; 11 : 154-161.
2. Carpentier A, Chauvaud S, Macé L, et al. A new reconstructive operation for Ebstein’s anomaly of the tricuspid valve. J Thorac Cardiovasc
Surg 1988 ; 96 : 92-101
3. Houyel L. Anomalie d’Ebstein : aspects anatomiques. Arch Mal Cœur 2002 ; 95 : 513-517.
inférieur est donc complètement oblitéré. Les feuillets antérieur
et inférieur sont fusionnés. On a alors une valve « unicuspide
», l’orice tricuspide effectif (dit en anneau de clé, « keyhole »)
centré sur la commissure antéroseptale est déplacé vers le haut
et vers l’avant, vers la chambre de chasse : ceci correspond à
l’orice antérieur primitif, au stade embryologique de l’entonnoir
tricuspidien. Cet orice peut être restrictif voire même atrétique.
D’autres formes extrêmes d’anomalies d’Ebstein peuvent
résulter en une absence complète de feuillets tricuspides
individualisables, aboutissant à un « unguarded tricuspid
orice» et éventuellement à une imperforation de l’orice
tricuspide déplacé dans ce cas très bas, au niveau de l’éperon
musculaire anormal séparant l’inlet de l’apex du ventricule droit.
Conclusion
L’anomalie d’Ebstein est due à une interruption du
développement normal de la valve tricuspide. Les différentes
formes anatomiques dépendent du moment de cette
interruption pendant la vie embryonnaire. Néanmoins, ces
différentes formes anatomiques auront un pronostic fonctionnel
très variable et l’adage qui veut qu’il n’y ait pas de parallélisme
anatomo-clinique dans l’anomalie d’Ebstein reste vrai malgré
l’évolution des connaissances embryologiques.
Lucile HOUYEL.
C.T.
Ciné
Ciné
Ciné Gado
Gado
Gado
Fig. 1
+ Doute entre cardiomyopathie hypertrophique asymétrique et tumeur cardiaque.
Fig. 2
Fig. 3

....................................................................................................................................................................................
Le cahier du CCM - janvier 2012
4
© 2012 - Centre Cardio-Thoracique de Monaco - Tous droits réservés
Direction de la publication :
L’équipe médicale du CCM.
Comité de rédaction du numéro : Lucile HOUYEL,
Gilles DREYFUS, Filippo CIVAIA, Philippe ROSSI, Nicolas
HUGUES, Laura IACUZIO, Clara ALEXANDRESCU.
Pour recevoir le Cahier du CCM :
Centre Cardio-Thoracique de Monaco
11 bis, avenue d’Ostende
BP223
MC98004 MONACO Cedex
Tél. +377 92 16 80 00
email : [email protected]
Site internet : www.ccm.mc
Scanner Imagerie par Résonance Magnétique Échographie Coronarographie
M.R.I
C.T. X.A.
E
+ Dilatation de l’aorte ascendante : quand faut-il opérer ?
Brèves
+ 19/01/2012 - Le CCM dispose désormais d’un
nouveau système d’imagerie endocoronaire : l’O.C.T.
(Optical Coherence Tomography).
E
Patient âgé de 64 ans, sportif,
porteur d’un anévrysme de l’aorte
ascendante à 52 mm adressé en
urgence pour douleur thoracique
avec suspicion clinique de dissec-
tion aortique
Echocardiographie transeso-
phagienne (g. 1, 2, 3 et 4) avec
visualisation d’un ap de dissec-
tion prolabant dans la chambre
de chasse du VG. Le diamètre de
l’aorte est à 54 mm. Le mouvement
du ap de dissection entre les sig-
moïdes aortique est responsable
d’une fuite aortique sévère asso-
ciée.
Un examen par scanner thora-
cique (g. 5 et 6) pour
évaluation de l’extension
de la dissection a mis en
évidence la présence du
ap au niveau du secteur
I de l’aorte sans atteinte de
la crosse aortique. Le dia-
mètre maximal de l’aorte
ascendante est mesuré à
52 mm
Le patient a bénécié d’un
remplacement complet
de la racine de l’aorte
avec réimplantation des
ostia coronaires avec des
suites opératoires très
simples.
On parle d’une dilatation de
l’aorte ascendante si le diamètre
de l’aorte dépasse 21 mm/m². Il est
important d’associer à cette déni-
tion la notion de perte de parallé-
lisme des parois de l’aorte thora-
cique.
Les causes de la dilatation :
1. La maladie anuloectasiante qui
concerne des patients âgés de
plus de 50 ans athéromateux
et surtout hypertendus sans
notion héréditaire. Dans 50 %
des cas, il s’agit d’ une atteinte
isolée des sinus Valsalva
2. Le Marfan
3. La bicuspidie aortique
Un anévrysme de l’aorte peut se
révéler d’emblée par une rupture
cataclysmique (60 % des patients
n’arrivent pas à l’hôpi-
tal) ou une ssuration
à traiter en extrême
urgence.
Lorsque l’anévrysme
est asymptomatique,
l’indication opératoire
sera posée à condi-
tion que son diamètre
atteigne ou dépasse
55 cm, ou bien qu’il
augmente rapidement
sur deux examens
successifs (plus de 5
mm/ année).
Clara ALEXANDRESCU, Filippo
CIVAIA, Gilles DREYFUS.
Fig. 4
C’est ce faisceau de faux tendons qui donne
cet aspect de cardiomyopathie hypertrophique
asymétrique, principalement au niveau antérieur
basal et moyen.
Laura IACUZIO, Philippe ROSSI,
Nicolas HUGUES, Filippo CIVAIA.
Fig. 1
Fig. 4
Fig. 2
Fig. 3
Fig. 5
Fig. 6
C.T.
1
/
4
100%







![III - 1 - Structure de [2-NH2-5-Cl-C5H3NH]H2PO4](http://s1.studylibfr.com/store/data/001350928_1-6336ead36171de9b56ffcacd7d3acd1d-300x300.png)

