Les outils du dépistage de l`infection par le VIH

Journal Identification = VIR Article Identification = 0501 Date: May 17, 2013 Time: 12:44 pm
revue
Virologie 2013, 17 (3) :171-81
Les outils du dépistage de l’infection par le VIH :
concepts, progrès et limites
Francis Barin1
Franc¸ois Simon2
1CHU Bretonneau,
université Franc¸ois-Rabelais,
Inserm U966,
centre national de référence du VIH,
laboratoire de virologie,
2, boulevard Tonnellé,
37044 Tours cedex,
France
2Hôpital Saint-Louis,
faculté de médecine Paris-Diderot,
laboratoire de virologie,
75010 Paris,
France
Résumé. En trois décennies, des progrès très importants ont été réalisés dans
le développement et la maîtrise des outils du diagnostic de l’infection VIH. La
connaissance de la cinétique des marqueurs virologiques de cette infection a per-
mis de disposer des bases conceptuelles sur lesquelles s’appuie ce diagnostic.
Associées aux aspects pratiques de faisabilité et de coût-efficacité, ces données
fondamentales font que le dépistage de l’infection VIH repose avant tout sur un
diagnostic sérologique. Les tests Elisa mixtes combinés de détection des anti-
corps anti-VIH et de l’antigène de capside p24 constituent désormais les outils à
utiliser en première intention pour un dépistage sensible et spécifique. Les tests
de diagnostic moléculaire sont des compléments pertinents dans certaines cir-
constances, telles que le diagnostic précoce de primo-infection ou le diagnostic
d’infection chez le nouveau-né. Les tests de diagnostic rapide constituent des
outils indispensables dans les pays à faibles ressources et offrent des possibilités
intéressantes afin de dépister des populations à risque entrant peu ou mal dans
le circuit sanitaire. Leur moindre sensibilité, notamment en début d’infection,
fait qu’ils ne peuvent se substituer aux tests Elisa classiques dès lors que ceux-ci
sont disponibles. La surveillance de l’efficacité des tests existants, qu’ils soient
sérologiques ou moléculaires, demeure indispensable du fait de la diversité du
VIH et de son évolution génétique et antigénique continue.
Mots clés : VIH, diagnostic, dépistage, immuno-essais, tests moléculaires
Abstract. The biological tools for an efficient diagnosis of HIV infection have
made major progresses during the three last decades. The dynamics of the viral
markers during natural infection is well known and provides a strong rationale for
the diagnostic strategy. The 4th generation enzyme immunoassays that allow the
simultaneous detection of the p24 capsid antigen and HIV antibodies must be used
as first-line diagnostic in priority. Nucleic acid testing are complementary tools,
particularly useful for the early diagnosis of primary infection and for diagnosis of
HIV infection in infants born to infected mothers. The rapid tests constitute major
tools for the HIV diagnosis in developing countries, but are also helpful in at-risk
populations than cannot be reached easily with classical assays in industrialized
countries. However, one must be aware of their lower sensitivity, especially in the
first weeks following infection. The growing diversity and the ongoing evolution
of HIV constitute a permanent challenge for the optimal efficacy of any diagnostic
tool.
Key words: HIV, diagnosis, serology, immunoassays, nucleic acid testing
Il y a un peu plus de 25 ans, les premiers tests de dépis-
tage de l’infection par le virus de l’immunodéficience
humaine (VIH) étaient mis à disposition deux ans après
l’identification du virus responsable de la pandémie la plus
Tirés à part : F. Barin
dramatique du xxesiècle [1]. Si l’isolement du virus par
culture cellulaire in vitro chez de nombreux patients a rapi-
dement permis de confirmer que le VIH était bien l’agent
étiologique du sida [2, 3], l’ampleur de l’épidémie et les
conséquences de l’infection pour tout individu contaminé,
à l’époque où aucune thérapeutique anti-virale n’était dis-
ponible, justifiaient de disposer en urgence de tests de
doi:10.1684/vir.2013.0501
Virologie, Vol 17, n◦3, mai-juin 2013 171
Pour citer cet article : Barin F, Simon F. Les outils du dépistage de l’infection par le VIH : concepts, progrès et limites. Virologie 2013; 17(3) : 171-81 doi:10.1684/vir.2013.0501
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

Journal Identification = VIR Article Identification = 0501 Date: May 17, 2013 Time: 12:44 pm
revue
dépistage de l’infection. Cette absolue nécessité était ren-
forcée par les évidences de la transmission du virus par
le sang et les dérivés plasmatiques [4-6], et donc par le
besoin de disposer d’outils de screening utilisables à large
échelle. La première approche fut de développer des tests
de dépistage des anticorps anti-VIH s’appuyant sur la tech-
nologie enzyme linked immunosorbent assay (Elisa) dont
la simplicité, l’efficacité et le faible coût avaient fait précé-
demment leur preuve dans le domaine des hépatites virales
A et B. Dès 1985, les tests de première génération deve-
naient disponibles et s’avéraient extrêmement utiles [7, 8].
Il est intéressant de se souvenir qu’à cette époque la signi-
fication de la présence d’anticorps anti-VIH était âprement
discutée : les anticorps détectés étaient-ils synonymes de
présence du virus, de contact avec le virus ou éventuelle-
ment de « guérison ». Il est devenu vite évident, du fait de la
permanence de la positivité des isolements du virus à partir
des cellules des patients en dépit de la présence d’anticorps,
que les anticorps anti-VIH signaient l’infection chronique et
que leur dépistage constituait la méthode de choix pour faire
le diagnostic d’infection VIH. Les deux décennies suivantes
ont vu l’accumulation de connaissances et d’exigences qui
ont porté très haut la qualité et la performance des tests de
dépistage de l’infection VIH, aussi bien en termes de sen-
sibilité, de spécificité que de praticabilité. L’objet de cette
revue est donc faire le point sur les concepts, les connais-
sances et les outils du dépistage, en partie au travers de leur
évolution depuis bientôt 30 ans, sans oublier de discuter
leurs limites et leurs indications. Pour les aspects pratiques
et de santé publique, il est recommandé de consulter les
documents intitulés « Dépistage de l’infection par le VIH
en France. Modalités de réalisation des tests de dépistage »
et « Dépistage de l’infection par le VIH en France. Stra-
tégies et dispositif de dépistage » sur le site de la Haute
Autorité de santé (HAS ; http://www.has-sante.fr).
Cinétique des marqueurs viraux
La cinétique des marqueurs viraux est clairement éta-
blie depuis environ 15 ans, période correspondant à
l’optimisation des outils dérivés des techniques immuno-
chimiques (Elisa de troisième génération) et moléculaires
(RT-PCR sensibles au seuil de 20-50 copies/mL). Le
schéma de cinétique d’apparition des différents marqueurs
correspond bien évidemment à un profil moyen basé sur
des analyses portant sur de nombreux patients (figure 1),
mais force est de constater que les variations de ciné-
tiques sont très limitées et que seuls des écarts modestes,
se chiffrant au maximum en jours, sont constatés entre les
cas individuels. L’étude la plus exhaustive est certaine-
ment celle publiée en 2003 par Fiebig et al. dans l’équipe
de M. Busch à San Francisco [9]. Cette étude rétrospec-
tive avait pu être réalisée du fait de la disponibilité de
10 0 20 30 60 2 4 6 8
jours années
ARN
Ag p24
Ac anti-Env
Ac anti-p24
Primo-infection Sida
Ly CD4+/mm3
Figure 1. Cinétique des marqueurs contribuant au dépistage de l’infection VIH. Les phases cliniques et la courbe du nombre de lymphocytes
CD4+(Ly CD4+) sont positionnées pour information complémentaire.
172 Virologie, Vol 17, n◦3, mai-juin 2013
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

Journal Identification = VIR Article Identification = 0501 Date: May 17, 2013 Time: 12:44 pm
revue
580 échantillons de sérums ou plasmas séquentiels collec-
tés au cours de primo-infections (PIH) ou séroconversions
identifiées chez 95 donneurs de plasma se présentant régu-
lièrement pour don par plasmaphérèse, la durée médiane
entre les prélèvements d’un même patient étant de quatre à
cinq jours. Les marqueurs viraux recherchés étaient l’ARN
viral par RT-PCR, l’antigène p24 (Ag P24) par Elisa,
et les anticorps anti-VIH par Elisa de seconde généra-
tion (modérément sensible, cf. infra), Elisa de troisième
génération (tests les plus sensibles) et western blot (test
analytique de confirmation, cf. infra). Il a été ainsi éta-
bli que l’ARN viral, l’Ag p24 et les anticorps anti-VIH
(Elisa de troisième génération) étaient détectés en médiane
respectivement, dix jours, 15 jours et 20 jours après la
contamination (tableau 1). Ce sont désormais ces délais
qui doivent être retenus pour répondre aux interrogations
concernant le délai de suivi après une exposition à risque
[10]. La charge virale (appréciée par la quantification de
l’ARN viral) et l’antigénémie p24 sont à leur maximum
au moment de la primo-infection et diminuent, voire dis-
parait pour l’Ag p24 du fait de la moindre sensibilité de la
technique, alors que la réponse anticorps se poursuit et per-
siste tout au long de l’infection (figure 1). Une classification
des différents stades définis par la cinétique d’apparition
des marqueurs viraux en début d’infection a été proposée
par Fiebig (tableau 1). Cette classification est désormais
largement utilisée dans bon nombre d’études physiopatho-
logiques ou virologiques s’intéressant à la primo-infection
[11].
Les tests Elisa : de la première
à la quatrième génération
Il était nécessaire avec les tests de première génération de
répondre très rapidement à l’urgence de disposer d’outils
de dépistage et de diagnostic. C’est donc vers des concepts
très simples et très classiques que se sont tournés cher-
cheurs et industriels. Ces tests de première génération
reposaient sur le principe des tests Elisa indirects dont
la phase solide était recouverte d’antigènes viraux issus
de virus semi-purifié produit par des lignées de lympho-
cytes T CD4+ chroniquement infectées par des souches
adaptées, notamment lignées productrices de la souche
initiale isolée à l’Institut Pasteur, dénommée BRU, LAI,
IIIB... [12]. Il est apparu très vite que ces tests de première
génération manquaient de sensibilité car les sérums de
certains patients, y compris au stade sida, demeuraient par-
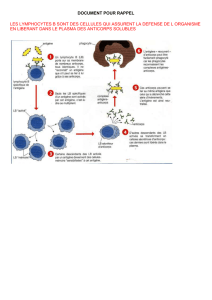
fois négatifs [7]. Au travers d’analyses immunochimiques,
telles que radioimmunoprécipitation (RIPA, figure 2A)
ou western blot (WB, figure 2B), il est très vite apparu
que les protéines virales n’étaient pas toutes également
immunogènes au cours de l’infection naturelle, et notam-
ment que les anticorps contre les protéines internes Gag
(p24–capside-, p17-matrice-) ou contre les enzymes virales
(p66/51–reverse transcriptase-, p34–intégrase-) n’étaient
pas constamment présents chez les patients infectés, y
compris au stade chronique, la diminution, voire la dis-
parition, de certains anticorps (anti-p24, anti-p17) étant
même considérée comme un marqueur d’évolution défa-
vorable [13, 14]. À l’opposé, tout patient infecté par le VIH
possédait systématiquement des anticorps contre les glyco-
protéines d’enveloppe, gp160 (précurseur Env) et gp120
(glycoprotéine de surface) sous forme native en RIPA,
et gp160 et gp41 (glycoprotéine transmembranaire) sous
forme réduite et dénaturée en WB [13, 15]. Ainsi, les
industriels du diagnostic se sont rapidement empressés de
développer les tests de seconde génération dont l’antigène
constitutif majeur était une protéine d’enveloppe, en géné-
ral recombinante (figure 3). Ces tests de seconde génération
avaient l’avantage d’être plus sensibles, mais également
plus spécifiques du fait de l’utilisation d’un antigène cible
purifié plus homogène. Le manque de sensibilité des tests
de première génération peut aussi être expliqué à la lumière
des données de structure obtenues plus récemment. En
Tableau 1 Délai d’apparition des différents marqueurs en début d’infection par le VIH-1.
Stade
(Fiebig stage)
ARN
viral
Ag
p24
Ac anti-VIH
(Elisa 2egen.)
Ac anti-VIH
(Elisa 3egen.)
Western blot Délai post-
infection (jours)
Durée du
stade (jours)
Phase muette 10
I+---- 105
II + + - - - 15 5
III + + - + - 20 3
IV + ±- + Pos. faiblea23 6
V+±± + Pos. (anti-p34 neg) 29 70
VI + ±+ + Pos. (anti-p34 pos) 99 ...
aPrésence d’anticorps anti-gp160 et/ou anti-p24.
Virologie, Vol 17, n◦3, mai-juin 2013 173
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

Journal Identification = VIR Article Identification = 0501 Date: May 17, 2013 Time: 12:44 pm
revue
A
B
- gp160
- gp120
- 66 RT
- 51 RT
- gp41
- 34 IN
- p24
- p17
- gp160
- gp120
- p55
- p24
- p17
Figure 2. Analyse immunochimique de la réponse anticorps anti-VIH-1 (sérums de patients infectés, prélevés au stade chronique de
l’infection).
A. Image représentative de radio-immunoprécipitation (RIPA) montrant la détection constante d’anticorps anti-gp160 et anti-gp120.
B. Image représentative de western blot (WB) montrant la détection constante d’anticorps anti-gp160 et anti-gp41.
effet, l’observation en microscopie électronique de parti-
cules virales purifiées suivie de la reconstruction d’images
en tomographie a clairement montré la faible densité de
spicules d’enveloppe à la surface du VIH-1 puisqu’on
estime que seulement environ 14 spicules seraient pré-
sents en moyenne en périphérie des virions [16]. On peut
ainsi penser que les tests de première génération étaient
peu performants pour détecter les anticorps antiprotéines
d’enveloppe, anticorps à détecter pourtant en priorité, du fait
d’une faible proportion des glycoprotéines d’intérêt dans
l’antigène utilisé. Les recherches fondamentales avaient
également permis d’identifier une région antigénique et
immunogène très conservée localisée dans l’ectodomaine
de la g41, constituée d’une boucle de cinq acides aminés
(AA) avec un pont disulfure à la base [17, 18]. Cette région
est appelée domaine ou épitope immunodominant (figure 3)
174 Virologie, Vol 17, n◦3, mai-juin 2013
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

Journal Identification = VIR Article Identification = 0501 Date: May 17, 2013 Time: 12:44 pm
revue
gp120 (GPSU) gp41 (GPTM)
IDE
1ère génération:
Virus purifié
2ème/3ème génération:
- Glycoprotéines purifiées
- Protéines recombinantes
- Peptides synthétiques
Figure 3. Composition antigénique des tests de dépistage des anticorps anti-VIH : de la première à la troisième génération.
GPSU : glycoprotéine de surface ; GPTM : glycoprotéine transmembranaire ; IDE : épitope immunodominant.
car tout patient infecté par le VIH développe des anticorps
contre cette région, quel que soit le type, groupe ou sous-
type de virus, et cela dès l’apparition de la séroconversion.
Cette particularité a donc permis de développer des tests de
dépistage de seconde génération dont l’antigène cible était
constitué de ce seul oligopeptide (moins de 20 AA) obtenu
par synthèse chimique. Les tests de troisième génération ont
par la suite gagné en sensibilité du fait de leur possibilité
de détecter les IgG et les IgM car reposant le plus souvent
sur une technologie de type « sandwich » (Ac détecté via la
capture sur une phase solide recouverte des antigènes cibles
et révélation par les mêmes antigènes marqués), et permet-
tant donc de réduire la durée de la « fenêtre sérologique »
[19]. Une étude réalisée récemment aux États-Unis à par-
tir de prélèvements séquentiels de patients identifiés dès la
primo-infection a permis d’objectiver le gain en termes de
précocité de détection entre les tests de première, deuxième
et troisième génération (figure 4, Pandori et al., présenté au
Workshop « Early and accurate detection of acute HIV
infection », Alexandria, VA, octobre 13-15, 2009).
L’amélioration des réactifs de dépistage s’est également
faite en parallèle grâce, d’une part, à l’accumulation des
connaissances sur la diversité du VIH et, d’autre part, à
l’introduction des tests de détection de l’Ag p24 pour le
diagnostic de primo-infection (PIH). L’identification du
VIH-2 en 1985 [20] suivie de son isolement en 1986 [21] a
immédiatement justifié le développement de réactifs mixtes
susceptibles de détecter efficacement aussi bien les Ac anti-
VIH-1 que les Ac anti-VIH-2 [22]. De fac¸on similaire,
l’identification du VIH-1 groupe O et les échecs de détec-
tion des anticorps correspondants du fait de la distance
génétique avec le VIH-1 groupe M ont justifié l’introduction
d’antigènes d’enveloppe du VIH-1 groupe O ou d’antigènes
du VIH-1 assurant la détection des anticorps anti-VIH-
1 groupe O par les tests de dépistage [23]. Les découvertes
plus récentes des variants rares des groupes N et P du VIH-
1 n’ont pas entraîné de modification de recommandation
10 0 20 30 60
jours
ARN
Ag p24
Ac anti-Env
Ac anti-p24
90
11
16
22
36
42
Elisa 1
ère
gen.
Elisa 2
nd
gen.
Elisa 3
ème
gen.
Ag p24
ARN VIH
TROD
Elisa 4
ème
gen.
(“combo“)
Figure 4. Délai de détection de l’ARN viral, de l’antigène p24 et
des anticorps anti-VIH selon la génération de tests Elisa (première,
deuxième, troisième). Les délais sont indiqués en jours. Le délai
estimé de positivité des tests de quatrième génération et des TROD
est indiqué à titre de comparaison.
selon Pandori et al. présenté au Workshop «Early and accurate
detection of acute HIV infection », Alexandria, VA, Octobre 13-15,
2009
de la composition des réactifs de dépistage [24-26]. Dès
1986, le développement et la disponibilité de tests Elisa de
détection de l’Ag p24 ont permis d’identifier très rapide-
ment l’intérêt majeur de ce marqueur pour le diagnostic de
la primo-infection [27]. C’est donc de fac¸on logique que les
industriels du diagnostic ont proposé des tests Elisa mixtes
(permettant la détection des anticorps anti-VIH-1 et anti-
VIH-2) combinés (permettant simultanément la détection
Virologie, Vol 17, n◦3, mai-juin 2013 175
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
1
/
11
100%