Echanges 63

N° 63 - Mars 2002 31
Complications des Cathéters Veineux
Centraux : prévention, traitement
J. PENGLOAN - Néphrologue - Hôpital Bretonneau - CHU - TOURS
Les principales complications des
Cathéters Veineux Centraux (CVC) sont
dominées par le taux élevé d’infections et
la fréquence des dysfonctionnements.
Dans cette présentation nous discu-
terons essentiellement des infections de
CVC.
FRÉQUENCE
DE L’INFECTION CHEZ LE
DIALYSÉ CHRONIQUE
La fréquence de l’infection est de 3 à 9 %
par an ; les taux de septicémie rapportés
dans la littérature sont de l’ordre de
0,93 %/mois/patient. La mortalité est
située entre 14 et 20 %. Elle est multipliée
par 2 lorsqu’il existe un antécédent de
septicémie. (Boelaert 1993 - Hoen 1997 -
Nielsen 1998 - Powe 1999)
Le risque de bactériémie à staphylocoque
doré chez un dialysé chronique est plus
de 330 fois supérieur à celui de la popu-
lation générale au Danemark (Nielsen
1998).
FRÉQUENCE
DES INFECTIONS LIÉES
AU CVC POUR
HÉMODIALYSE
Les données de la littérature rapportent
des taux d’infection de 3,9 à 5,5 bacté-
riémies pour 1000 jours/cathéter ; le taux
d’infection des CVC est nettement
supérieur à celui observé pour une fistule
artérioveineuse : un risque relatif de 7,64
(Hoen 1997) et une augmentation de
50 % du taux d’infection (Powe 1999) ont
été rapportés pour les CVC par rapport à
la fistule artérioveineuse. Le taux de
complication est très élevé de l’ordre de
40 à 44 % (Nielsen 1998 Marr 1998).
La mortalité est 4 fois plus élevée que
chez le sujet non dialysé.
L’infection liée au cathéter chez le dialysé
chronique est 2 fois sur 3 une infection à
staphylocoque et 2 fois sur 3 conduit à
l’ablation du cathéter.
SOURCES DE L’INFECTION
LIÉE AU CVC
Les germes responsables de l’infection du
CVC proviennent essentiellement :
- de la peau : mécanisme prédominant au
moment de l’insertion du cathéter.
L’infection se propage autour du cathéter
entraînant une tunnellite, une phlébite
etc…
- de l’environnement lors des manipu-
lations des connecteurs : mécanisme pré-
dominant lors de l’utilisation du cathéter.
L’infection est initialement endoluminale
et se propage à partir des germes intro-
duits par la lumière du cathéter.
La prévention du risque infectieux a bien
été étudiée par Mermel (2000) au cours
d’une méta-analyse.
Il en ressort que certaines mesures ont un
effet réel de prévention du risque infec-
tieux :
- l’asepsie cutanée au moment de la pose :
la teinture d’iode a un effet anti-infectieux
plus important que la Chorhexidine®et
même plus important que la Bétadine®.
Cependant la teinture d’iode est incom-
patible avec les silicones, matériau fré-
quemment rencontré dans les cathéters.
- le choix du site d’insertion : l’insertion
d’un CVC dans la veine sous-clavière s’ac-
compagne d’un risque infectieux moindre
que l’insertion dans la veine jugulaire
interne ou dans la veine fémorale ; cepen-
dant la pose d’un CVC dans la veine sous-
clavière doit être évité compte tenu du
risque important de sténoses qu’elle
entraîne.
- l’héparine lors du rinçage du cathéter a un
rôle préventif certain en réduisant les dépôts
de fibrine qui servent d’ancrage et de nutri-
ments pour les bactéries.
- la tunnellisation du cathéter en éloignant
l’orifice cutané du site d’insertion veineux a
un certain effet préventif.
- l’habillage chirurgical est un des facteurs le
plus important susceptible de prévenir l’in-
fection lors de la pose du cathéter ; ainsi il a
été montré une diminution statistiquement
significative (p = 0,02) du taux d’infection
de 0,5 /1000 jours/cathéter avec un habilla-
ge restreint (gants stériles et petit champ sté-
rile), à 0,08/1000 jours/cathéter si le cathé-
ter est posé avec un habillage chirurgical
(Infect. Control. Hosp. Epidemiol. 1994).
- le risque infectieux est lié au nombre de
manipulations, à la présence de personnel
non entraîné, au ratio personnel/patient : le
risque est augmenté si le ratio per-
sonnel/patient diminue de 1/l à l/2 (Infect.
Control. Hosp. Epidemiol. 1996).
Certaines mesures parfois préconisées n’ont
pas prouvé leur capacité de prévention de
l’infection :
- l’antibioprophylaxie lors de l’insertion du
cathéter
- les antibiotiques et les antiseptiques
locaux. Seule la Bétadine®crème appliquée
sur le site d’insertion pourrait avoir un effet
préventif. La Mupirocine®, antibiotique
utilisé dans le traitement du portage nasal
du Staphylocoque doré et parfois utilisé au
niveau des orifices cutanés est incompatible
avec le polyuréthane et peut entraîner une
résistance bactérienne.
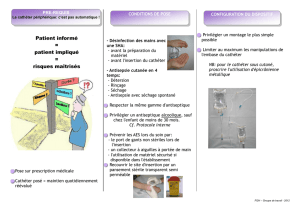
LES MÉCANISMES
DE L’INFECTION
ENDOLUMINALE
Fig.1 : Les étapes du développement de l’infection liée au cathéter

N° 63 - Mars 2002
32
L’infection endoluminale passe par
4 stades (Fig.1 page précédente) :
- introduction de la bactérie à l’intérieur
de la lumière du cathéter généralement
lors des manipulations des connecteurs
- l’adhésion de certaines bactéries :
certaines bactéries introduites ont des
capacités d’adhésion sur les matériaux
inertes comme les plastiques ; elles
acquièrent de nouvelles propriétés, secrè-
tent des adhésines qui leur permettent
d’adhérer aux matériaux, et deviennent
des bactéries à taux de croissance lent
vivant dans un milieu dénué ou pauvre en
nutriments ; pour se protéger, elles
secrètent un biofilm dans lequel elles
s’engainent et deviennent peu accessibles
aux traitements antibiotiques.
Chaque bactérie peut ainsi créer une
colonie visible en microscopie électro-
nique sous forme de “galette”. L’extension
se fait par essaimage d’une bactérie en
dehors de cette galette qui va créer une
nouvelle colonie dite “colonie fille” qui
sera elle-même à l’origine d’une nouvelle
galette et ainsi de suite pouvant aboutir à
un véritable tapis bactérien (Fig. 2
ci-dessous).
- à l’occasion de mouvements divers au
niveau de ces colonies, une bactérie peut
rejoindre le flux sanguin où elle retrou-
vera spontanément ses capacités patho-
gènes et sera à l’origine soit d’une septicé-
mie soit de localisations à distance sous
forme d’abcès, d’endocardite, d’arthrite,
etc…
La connection : c’est le moment crucial
de l’utilisation du CVC en hémodialyse,
au cours de laquelle une bactérie peut être
introduite dans la lumière du CVC et sera
à l’origine du développement d’une infec-
tion endoluminale puis d’une bactériémie
à point de départ cathéter. L’asepsie doit
être extrêmement rigoureuse au moment
de ces manœuvres.
TRAITEMENT
DE L’INFECTION
LIÉE AU CVC
Détection de la contamination endolu-
minale
Dans notre Unité d’Hémodialyse Chroni-
que nous avons émis l’hypothèse que la
détection précoce de la contamination
endoluminale permettrait de prévenir le
risque de bactériémie liée au CVC. La
culture du contenu du cathéter (héparine
contenue dans le cathéter et sang immé-
diatement aspiré) est faite une fois par
mois au moment des examens mensuels
avant dialyse. Le contenu de chaque
branche du cathéter est réparti dans
2 flacons d’hémoculture aérobie et anaé-
robie. Si la culture est positive dans une
ou deux branches, et en l’absence de
signes généraux, les hémocultures sont
répétées au début des 2 séances de dialyse
suivantes pour éliminer le risque de
souillure.
Si la positivité des cultures est confirmée
le traitement est débuté.
Le traitement est débuté immédiatement
en présence de signes généraux.
Traitement de l’infection endoluminale
du CVC
L’antibiothérapie doit être basée initiale-
ment sur une antibiothérapie à visée
antistaphylococcique. Les antibiotiques
doivent être choisis en fonction de leur
moindre risque de résistance bactérienne
et de leur facilité d’utilisation chez
l’hémodialysé chronique.
En cas de fièvre l’antibiothérapie doit être
instituée très tôt, immédiatement après
les hémocultures.
Le traitement de l’infection endoluminale
ou de la bactériémie liée au cathéter
repose sur l’association de trois trai-
tements :
- traitement du patient par antibiothé-
rapie générale : Céfazoline®500 mg,
Nétilmycine®2 mg/kg ; la moitié de
chaque antibiotique est passée dans
chaque branche du cathéter à la fin de
chaque séance de dialyse. La dose de
Nétilmycine®est adaptée en fonction des
résultats des dosages sériques.
- traitement du cathéter par verrou anti-
biotique en utilisant l’aminoside utilisé
(Nétilmycine®100 µg/ml dans l’héparine)
- traitement du biofilm avec un fibrinoly-
tique comme l’Urokinase®à 3 dialyses
successives après début de l’antibiothéra-
pie.
Le traitement antibiotique est éventuelle-
ment réajusté en fonction de l’antibio-
gramme.
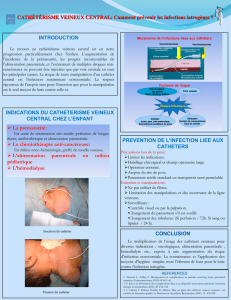
Fig.2 : Exemple de colonisation bactérienne d’un matériau inerte (2ème image : une “galette” à fort grossissement)

N° 63 - Mars 2002 33
La surveillance repose sur les cultures
faites pendant chaque séance de dialyse
puis une fois par semaine après négati-
vation des cultures. L’antibiothérapie est
poursuivie 2 semaines après la négati-
vation des cultures.
En cas de positivité persistante ou de
rechute après la fin de l’antibiothérapie, se
pose le problème du changement des
connecteurs ou de la pièce intermédiaire
des cathéters de Canaud. Si ces mesures
sont inefficaces le changement du cathéter
doit être envisagé.
En cas de persistance des signes généraux
malgré une antibiothérapie bien conduite
le cathéter doit être remplacé.
Résultats
Nous avons mené une étude prospective
concernant 36 cathéters totalisant
19 208 jours/cathéters. 9 contaminations
endoluminales ont été constatées : 6 sans
fièvre, 3 avec fièvre. 4 fois une seconde
contamination a été observée : 3 sans
fièvre, 1 avec fièvre. Le taux de coloni-
sation a été de 0,68/1000 jours/cathéter.
Le taux d’infection avec fièvre a été de
0, 21/1000 jours/cathéter. La probabilité
pour un cathéter de rester indemne
d’infection a été de 90 % à 12 mois. La
probabilité de ne pas être enlevé pour un
cathéter a été de 66 % à 36 mois, toutes
causes d’ablation du cathéter confondues.
Dans cette étude seul un cathéter a été
retiré pour une cause infectieuse.
Risques bactériologiques
On assiste à la diffusion de souches de
staphylocoques méthicilline-résistants et à
l’apparition d’entérocoques Vancomy-
cine-résistants. Ceci peut être lié à l’utili-
sation mal contrôlée des antibiotiques et à
l’insuffisance des mesures de lutte contre
la diffusion des staphylocoques méthicil-
line-résistants.
La stratégie de traitements des infections
dans un centre de dialyse doit faire appel
aux antibiotiques les plus anciens et doit
réserver les antibiotiques récents aux seuls
germes résistants.
La Vancomycine®est le dernier recours
pour traiter les staphylocoques méthicilli-
ne résistants. Elle ne doit donc pas être
utilisée en prophylaxie et doit être
réservée aux germes résistant aux autres
antibiotiques après antibiogramme.
PRÉVENTION
DES INFECTIONS LIÉES
AU CVC : L’AVENIR
De nouvelles méthodes de prévention de
l’infection endoluminale du CVC sont en
cours d’étude :
- le développement de solutions de
remplissage du cathéter à base d’antisep-
tiques comme le Citrate ou la
Taurolidine®. L’intérêt de ces solutions est
de ne pas avoir d’effet antibiotique et
donc de ne pas induire de résistance des
staphylocoques ou des bactéries de
l’environnement. Le risque de ces solu-
tions est de modifier l’environnement
bactériologique et peut-être de faciliter
l’émergence de germes inhabituels ou de
levures. Leur efficacité est en cours
d’évaluation.
- les connecteurs sous-cutanés peuvent
être une solution, en particulier chez les
patients faisant des infections à répétition
malgré les mesures d’asepsie. Le système le
plus connu actuellement est le système
Dialock®.
- un nouveau design des connecteurs
réduisant le risque d’introduction des
germes est espéré.
Dans tous les cas c’est le respect rigoureux
des règles d’asepsie durant toutes les
procédures de connections et de
déconnections qui est le plus susceptible
de réduire le risque infectieux.
CONCLUSION
L’infection reste la seconde cause de
mortalité chez l’hémodialysé chronique.
L’infection liée au cathéter met la vie des
patients en jeu. L’application stricte des
règles d’hygiène universelles reste la
mesure la plus efficace pour prévenir
l’infection liée au cathéter. La détection
et le traitement précoce des contamina-
tions endoluminales des CVC est une
mesure supplémentaire qui contribue à
améliorer la durée de survie des cathéters
veineux centraux pour hémodialyse.
1
/
3
100%