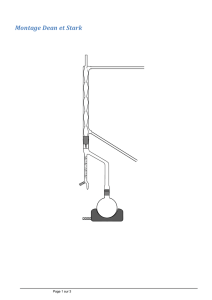
Enoncé TP N°5 - CPGE Brizeux

!"#$%&'()*# +!#,-.# /01234(%56(7'&(7#89:.589:;#
#
1/5$
!"#$%&#'#()!(*+,+-.!+/$#0(#,+)-1(*#
!
/2345678#'#<(#=)1#>(#?(#+!#(@1#>(#2(11%(#(7#A)B%(#0C(@1D%&E&?31&F7#>C)7#(@1(%#3?&>(#?3%=F*40&G)(#H3%#)7#30?FF0#
H%&23&%(#I#0C3&>(#>C)7#2F713J(#K(375L13%M#H)&@#>(#H)%&E&(%#0(#H%F>)&1#F=1(7)#H3%#>&@1&0031&F7#E%3?1&F77D(N#
#
+9 0:;;<4=#46#5:;=7>;4=#?4#=<5@A76<#
-:BC:=<#
.57?4#
D5<67E@4#
>FD57DF#
G@6D;HIH:F#
.5<6D64#?4#
2@6JF4#
."!)#
!:F@K;4#
LD==4#B:FD7A4#
M>NB:FOIP#
;9O9.#
PQO:8#
::;O:;#
:P8O89#
R8O:Q#
04;=76<#
:O9QR#
9OS:9#
9OSS;#
#
9OS;P#
!4BC<AD6@A4#
?Q<2@FF767:;#M%-P#
::S#
::P#
:8;#
#
:::#
)<5@A76<#46#
A4BDAE@4=#
"F%%F@&EO#
H%FBFG)(#>(#
J%3B(@#
=%T0)%(@N#/#
237&H)0(%#
3B(?#>(@#J371@#
(1#>(@#
0)7(11(@N#
U7E03223=0(N#
#
#
,F?&E#H3%#&7V3031&F7O#
?F713?1#3B(?#03#H(3)#
(1#H3%#&7J(@1&F7N#!()1#
?3)@(%#@F27F0(7?(#
(1#B(%1&J(N#/#
237&H)0(%#3B(?#>(@#
J371@#(1#>(@#0)7(11(@N#
U7E03223=0(N#
#
#!()1#?3)@(%#
@F27F0(7?(#(1#
B(%1&J(N#/#
237&H)0(%#
3B(?#>(@#J371@#
(1#>(@#
0)7(11(@N#
U7E03223=0(N#
#
"F%%F@&EN#/#
237&H)0(%#
3B(?#>(@#J371@#
(1#>(@#
0)7(11(@N#
#
,F?&E#H3%#&7V3031&F7O#
?F713?1#3B(?#03#H(3)#
(1#H3%#&7J(@1&F7N#
!()1#?3)@(%#
@F27F0(7?(#(1#
B(%1&J(N#/#237&H)0(%#
3B(?#>(@#J371@#(1#>(@#
0)7(11(@N#
U7E03223=0(N#
#
#
Remarque!:!L'acide!acétique!glacial!ne!signifie!pas!qu'il!est!à!0°C,!mais!qu'il!est!pur!à!99,5!%.!Il!est!surnommé!
"glacial"!car!il!a!tendance!à!cristalliser!à!des!températures!inférieures!à!17!°C.!
!
++9 "A7;57C4#><;<ADF#
#
W7#>D@&%(#@471VD1&@(%#0C3?D131(#>(#=)140(O#)7#(@1(%#I#0CF>()%#?3%3?1D%&@1&G)(#>(#=3737(#F)#>(#HF22(N#U0#(@1#
)1&0&@D# ?F22(# 3>>&1&E# 30&2(713&%(# >37@# 0(@# @)?%(%&(@O# 0(@# ?%X2(@# J03?D(@O# 0(@# E%F23J(@O# (1# (@1# 1%F)BD#
731)%(00(2(71#>37@#?(%13&7@#E%)&1@#?F22(#0(@#HF22(@N#
W7# @(# H%FHF@(# HF)%# 0CF=1(7&%# >C(EE(?1)(%# @;4# 4=6<A7875D67:;# ?4# ,7=5R4A#(71%(# 0C3?&>(# 3?D1&G)(O# )7# %D3?1&E#
?F22(%?&30#=F7#23%?VDO#(1#0(#=)1375:5F0N#
#
O
OH +HO
APTS
toluène
O
O
+H2O
acétate de butyle

!"#$%&'()*# +!#,-.# /01234(%56(7'&(7#89:.589:;#
#
2/5$
+++9 LD;7C@FD67:;##
-:;=7>;4=#'##
S <CF%J37&@31&F7#0F%@#>C)7#+!#>(#?V&2&(#F%J37&G)(#(@1#H%&2F%>&30(#(1#H(%2(1#>(#E3&%(#03#>&EED%(7?(#(71%(#
0(@# ?37>&>31@# 3)*# ?F7?F)%@N# /B371# >(# ?F22(7?(%# 03# 237&H)031&F7O# 7F# 4=6# :2F7>D6:7A4# ?4# F7A4#
7;6<>ADF4B4;6# FQ<;:;5<9# <(@# 1(2H@# >C311(71(# >(B%F71# Y1%(# (*H0F&1D@# 3)# 2&()*# Z371&?&H31&F7# >(@#
H%F?V3&7(@# D13H(@# >)# H%F1F?F0(O# %D>3?1&F7# >)# ?F2H1(5%(7>)O# H%DH3%31&F7# >(@# ?30?)0@# HF)%# 0(#
%(7>(2(71[\N##
S U0# BF)@# (@1# >(237>D# >CY1%(# H3%1&?)0&X%(2(71# B&J&0371@# (7# ?(# G)&# ?F7?(%7(# 03# =<5@A76<N# <(@# H%F>)&1@#
>F&B(71#Y1%(#237&H)0D@#3B(?#0(#BD6<A74F#?4#CA:64567:;#3>3H1DN#]F)@#B(&00(%('#I#?(#G)(#BF1%(#H3&003@@(#
@F&1#(7#H(%237(7?(#CA:CA4#46#274;#AD;><4N#
#
I9 )J;6RK=4#
S K37@#)7#=300F7#>(#8.9#2<#2)7&#>C)7#3HH3%(&0#K(375L13%M# 3)G)(0#3# D1D#E&*D#)7# %DE%&JD%371O#&71%F>)&%(#
@)??(@@&B(2(71#9O8.#2F0#>(#=)1375:5F0O#9O8.#2F0#>C3?&>(#3?D1&G)(#J03?&30#(arrondir!au!mL!supérieur!en!
acide!et!au!mL!inférieur!en!alcool,!de!manière!à!avoir!l'alcool!en!léger!défaut)O#^9#2<#>(#1F0)X7(#(1#9O.#J#
>C3?&>(#para51F0)X7(@)0EF7&G)(N#
S _(2H0&%#0(#1)=(#>D?371()%#>(#1F0)X7(#`)@G)CI#@3#H3%1&(#@)HD%&()%(N#
S !F%1(%#0(#2D037J(#%(E0)*#@F)@#3J&131&F7N#
#
T9 !AD764B4;6#?4#FD#A<D567:;#
S a)37>#0C(@1D%&E&?31&F7#(@1#1(%2&7D(O#%(E%F&>&%#0(#=300F7#H)&@#B(%@(%#@F7#?F71(7)#>37@#)7#(%0(72(4(%N#
S /`F)1(%#8.#2<#>C)7(#@F0)1&F7#@31)%D(#>(#?3%=F731(#>(#@F>&)2#3E&7#>(#HF%1(%#0(#H6#B(%@#PN##
S /H%X@# ?(@@31&F7# >(# 0C(EE(%B(@?(7?(O# &71%F>)&%(# 0(# 2&0&()# %D3?1&F77(0# >37@# 0C32HF)0(# I# >D?371(%# (1#
%D?)HD%(%#03#HV3@(#F%J37&G)(N#
S <3B(%# 03# HV3@(# F%J37&G)(# 3B(?# 8.# 2<# >C)7(# @F0)1&F7# @31)%D(# >(# ?V0F%)%(# >(# @F>&)2# H)&@# @D?V(%# @)%#
@)0E31(#>(#23J7D@&)2#37V4>%(N#
#
U9 "@A7875D67:;#?@#CA:?@76#?4#=J;6RK=4#
S K&@1&00(%#I#03#H%(@@&F7#312F@HVD%&G)(#(7#?30F%&E)J(371#03#?F0F77(N#
S _(?)(&00&%#0C(@1(%#>37@#)7#(%0(72(4(%#H%FH%(O#@(?O#H%D303=0(2(71#H(@D#(1#2)7&#>C)7#=F)?VF7N#
S !(@(%#0(#H%F>)&1#F=1(7)#(1#7F1(%#@F7#3@H(?1N#
#
V9 (WDF@D67:;#?4#FD#C@A46<#?4#FQ4=64A#:264;@#
S KD1(%2&7(%#03#1(2HD%31)%(#>CD=)00&1&F7#>(#0C(@1(%#I#03#H%(@@&F7#312F@HVD%&G)(N#
S b(@)%(%#@F7#&7>&?(#>(#%DE%3?1&F7N#
#
#
#
##

!"#$%&'()*# +!#,-.# /01234(%56(7'&(7#89:.589:;#
#
3/5$
+X9 Y@4=67:;=#
I9 c3&%(#)7#@?VD23#377F1D#>)#2F713J(#K(375L13%M#(1#>)#2F713J(#>(#>&@1&0031&F7#E%3?1&F77D(N#
T9 <F%@# >(# 03# %D3?1&F7# >C(@1D%&E&?31&F7O# HF)%G)F&# ?V3)EE(515F7# 0(# 2&0&()# %D3?1&F77(0#d# a)(0# (@1# 0(# %e0(# >(#
0C3?&>(# para51F0)X7(@)0EF7&G)(#d# a)(0# (@1# 0f3B3713J(# >f)1&0&@(%#0f/!+L# 3)# 0&()# >f3?&>(# @)0E)%&G)(#
?F7?(71%D#d#
U9 a)(0#(@1#0(#%e0(#>)#1F0)X7(#d#g*H0&G)(%#0(#?VF&*#>)#2F713J(#K(375L13%M#(7#@C3HH)4371#@)%#0(#>&3J%322(#
=&73&%(#(3)51F0)X7(N#/#G)(00(#1(2HD%31)%(#>F&15F7#HF%1(%#0(#2&0&()#%D3?1&F77(0#d#"F22(71#@3&15F7#G)(#03#
%D3?1&F7#(@1#1(%2&7D(#d#
#
V9 a)(0# (@1# 0C&71D%Y1# >)# 03B3J(# >(# 03# HV3@(# F%J37&G)(# 3B(?# 03# @F0)1&F7# @31)%D(# >(# ?3%=F731(# >(# @F>&)2#d#
!F)%G)FC(EE(?1)(515F7#H3@#>&%(?1(2(71#0(#03B3J(#>37@#0C32HF)0(#I#>D?371(%#d#a)(00(#(@1#03#731)%(#>)#
>DJ3J(2(71#J3'()*#F=@(%BD#d#!F)%G)Ff)1&0&@(515F7#H3@#)7(#@F0)1&F7#>(#@F)>(#HF)%#%D30&@(%#0(#2Y2(#
03B3J(#d#
&9 a)(0# (@1# 0C&71D%Y1# >)# 03B3J(# >(# 03# HV3@(# F%J37&G)(# 3B(?# 03# @F0)1&F7# @31)%D(# >(# ?V0F%)%(# >(# @F>&)2#d#
"F22(71#@C3HH(00(5(00(#?(11(#D13H(#d#
Z9 KD1(%2&7(%#0(#%(7>(2(71#>(#03#@471VX@(N#
[9 gB30)(%#03#H)%(1D#>)#H%F>)&1#@471VD1&@D#J%h?(#3)*#%D@)0131@#>(@#2(@)%(@#(EE(?1)D(@N#
\9 !%FHF@(%#)7#2D?37&@2(#%D3?1&F77(0#HF)%#03#%D3?1&F7#>C(@1D%&E&?31&F7#%D30&@D(N#
]9 U71(%H%D1(%#0(@#@H(?1%(@#_b,#:6#(1#U_#>(#0C3?D131(#>(#=)140(#>F77D@#>37@#0CD7F7?DN#
#
Figure!1!:!Spectre!IR!de!l'acétate!de!butyle!

!"#$%&'()*# +!#,-.# /01234(%56(7'&(7#89:.589:;#
#
4/5$
#
Figure!2!:!Spectre!RMN!1H!de!l'acétate!de!butyle!(CDCl3,!90!MHz)!
#
Annexes&:&données&spectroscopiques&
#
Figure!1!:!Table!RMN!1H!en!ppm!non!exhaustive!pour!différents!protons!en!fonction!de!leur!environnement!
#
#
Figure!2!:!Table!IR!
1O#86#
@O#^6#
2#
Q6#
1#
^6#

!"#$%&'()*# +!#,-.# /01234(%56(7'&(7#89:.589:;#
#
5/5$
#
G7FD;#?4=#5:BC<64;54=#46#5DCD576<=#4^C<A7B4;6DF4=#B:27F7=<4=#?D;=#54#!"#'#
• b(11%(#(7#A)B%(#>(@#%XJ0(@#>(#@D?)%&1D#3>DG)31(@#(Réaliser)N#
• b(11%(#(7#A)B%(#)7(#(@1D%&E&?31&F7#I#0C3&>(#>C)7#2F713J(#K(375L13%M#(7#`)@1&E&371#@F7#&71D%Y1N#(Réaliser!
et!analyser)N#
• b(11%(# (7# A)B%(# )7(# (*1%3?1&F7# 0&G)&>(50&G)&>(# (1# )7# 03B3J(# (7# `)@1&E&371# @F7# &71D%Y1# ZRéaliser! et!
analyser\N#
• b(11%(# (7# A)B%(# 0(# @D?V3J(# >C)7# 0&G)&>(# (1# DB3HF%(%# 0(# @F0B371# %D@&>)(0# I# 0CDB3HF%31()%# %F131&E#
(Réaliser)N#
• b(11%(#(7#A)B%(#)7(#>&@1&0031&F7#E%3?1&F77D(#(Réaliser)N#
• KD1(%2&7(%#0(#%(7>(2(71#>C)7(#@471VX@(#(Réaliser!et!valider)N#
• b(@)%(%#)7#&7>&?(#>(#%DE%3?1&F7O#(*H0F&1(%#0(#%D@)0131#(Réaliser!et!valider)N#
• "F7E&%2(%#)7(#@1%)?1)%(#I#0C3&>(#>(#>F77D(@#@H(?1%F@?FH&G)(@#(Valider)N#
• _D@)2(%# @3# >D23%?V(# (1# @(@# %D@)0131@# I# 0CD?%&1# >(# E3iF7# ?03&%(# (1# ?F2H0X1(# (7# E3&@371# 3HH3%3j1%(# 0(@#
HF&71@#?0D@#>)#%3&@F77(2(71#ZCommuniquer\N#
#
#
#
#
1
/
5
100%