Remodelage des grosses et petites artères dans l`hypertension

Mini-revue
Sang Thrombose Vaisseaux 2004 ;
16, n° 2 : 81–9
Remodelage des grosses et petites artères
dans l’hypertension artérielle
Pierre Boutouyrie, Stéphane Laurent
Service de pharmacologie, hôpital européen Georges Pompidou, 20, rue Leblanc, 75908 Paris Cedex 15
Correspondance et tirés à part :
Pierre Boutouyrie
Le remodelage vasculaire correspond à toute modification de
structure et de fonction artérielle au cours de processus physio-
logiques et pathologiques. Les modifications adaptatives sur le
court terme peuvent s’accompagner de conséquences patholo-
giques sur le long terme. Au cours de l’hypertension artérielle,
les conséquences sont différentes selon que l’on s’intéresse aux
petites artères de résistances ou aux artères de conduction. Les
artères de résistances subissent trois types de phénomènes :
1) un remodelage concentrique dit eutrophique, c’est-à-dire
une réorganisation de la même quantité de tissus autour d’un
diamètre plus petit ; 2) une raréfaction du lit artériolaire, c’est-
à-dire une densité artériolaire diminuée par unité pondérale de
tissu perfusé ; 3) une atteinte précoce de la fonction endothé-
liale, avec diminution de la biodisponibilité du monoxyde
d’azote (NO). La conséquence globale est une augmentation
des résistances périphériques, une altération des capacités de
vasodilatation et une ischémie tissulaire en condition critique de
perfusion. Les méthodes d’exploration de ces différentes com-
posantes sont insuffisantes pour les proposer en routine.
L’atteinte des grosses artères est dominée par l’hypertrophie
excentrique, l’augmentation de rigidité et la perte de com-
pliance. Cette augmentation de rigidité dépend du territoire
artériel. Elle est importante pour l’aorte, modérée pour les
artères élastiques, paradoxalement diminuée pour les artères
musculaires, reflétant les effets cumulés de l’hypertrophie mus-
culaire lisse vasculaire (prédominant en périphérie), et les
modifications de matrice extracellulaire (prédominant pour les
artères élastiques). La valeur pronostique péjorative de l’hyper-
trophie et de la rigidification sont maintenant bien établies. Ces
deux lésions constituent à proprement parler l’atteinte de l’ar-
tère en tant qu’organe cible.
Mots clés : hypertension artérielle, remodelage, athérosclérose, rigidité
artérielle, épaisseur intima média.
STV, n° 2, vol. 16, février 2004 81
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

Ces dernières années, le remodelage artériel a
émergé comme un concept clef de la physiopa-
thologie de l’hypertension artérielle et de son
retentissement. En effet, le système artériel est
par définition un acteur essentiel et primordial dans la
pathogénèse des complications infracliniques et cliniques
de l’hypertension. Le terme remodelage recouvre une réa-
lité complexe. Au sens premier, remodelage avait un sens
très restrictif, correspondant à la réorganisation d’une
même quantité du tissu artériel autour d’un diamètre diffé-
rent. Aujourd’hui, le sens est beaucoup plus large, et dési-
gne tout phénomène survenant au niveau de la paroi arté-
rielle (de l’artériole aux artères de gros calibre), englobant
toutes les modifications structurales et fonctionnelles des
artères, observé au cours de processus pathologiques ou
physiologiques. Le remodelage artériel implique au moins
4 processus cellulaires :
– croissance ;
– migration cellulaire ;
– production ou dégradation de la matrice extracellulaire ;
– apoptose (mort programmée).
Ces processus dépendent d’interactions dynamiques entre
facteurs de croissance produits localement, substances va-
soactives, et stimulus hémodynamiques [1]. Ce type de
remodelage peut ainsi s’observer sur tous les sites vasculai-
res, qu’il s’agisse d’artérioles ou de gros troncs artériels, et
non seulement au cours de l’hypertension mais aussi de
l’insuffisance cardiaque, de l’athérosclérose, et de la resté-
nose après angioplastie.
Plus spécifiquement, au cours de l’hypertension, le remo-
delage consiste en un épaississement de la paroi artérielle
(de l’intima-média, c’est-à-dire les couches interne et
moyenne de la paroi), que l’on suppose adaptatif et destiné
à maintenir constante la contrainte pariétale. Le concept de
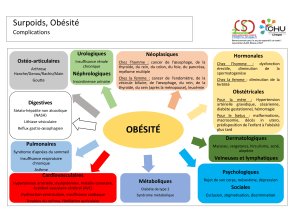
remodelage artériel (figure 1) permet d’aborder, au plan
physiopathologique, le problème du retentissement fonc-
tionnel et structural de l’hypertension sur le système arté-
riel [2, 3].
Les propriétés fonctionnelles doivent être envisagées en
fonction du calibre de l’artère :
– fonction de conduction du sang ;
– fonction d’amortissement de la pulsatilité artérielle pour
les artères de gros calibre ;
– fonction de distribution du débit sanguin et de résistance à
l’écoulement pour les petites artères et artérioles.
Les propriétés structurales sont définies par :
– hypertrophie, eutrophie et hypotrophie : augmentation ou
diminution de la masse artérielle ;
– excentrique ou concentrique : augmentation ou diminu-
tion du calibre interne.
Remodelage artériel
au cours de l’hypertension
Artères de conduction et de compliance
Elles présentent une structure concentrique avec, de dedans
à en dehors, l’intima, la média et enfin l’adventice. La
média (couche moyenne) est la couche la plus impliquée
dans les phénomènes de remodelage de l’hypertension. La
média des artères élastiques présente une apposition
concentrique de lames élastiques circulaires. Entre chacune
d’elles se trouvent des cellules musculaires lisses, des fibres
de collagène, des microfibrilles d’élastine et des glycosami-
noglycanes de la substance fondamentale (figure 2). L’en-
semble constitue les « unités lamellaires » [4]. La
contrainte circonférentielle, calculée selon l’équation de
Lamé (rh = P.R/h, avec P = pression, R = rayon et
h = épaisseur ; équation dérivée de la loi de Laplace :
tension = P.R), supportée par chaque unité lamellaire est
relativement constante d’une artère à l’autre.
L’hypertension entraîne une augmentation de l’épaisseur
de la média (h) qui permet de maintenir constante la
contrainte circonférentielle malgré l’augmentation de la
pression intraluminale.Au cours de l’hypertension, le nom-
bre d’unités lamellaires reste fixe et l’augmentation de
l’épaisseur pariétale est obtenue grâce aux modifications
des cellules musculaires lisses et de la matrice extracellu-
laire. Les effets de l’hypertension diffèrent selon les terri-
toires artériels. Les grosses artères élastiques (comme la
AFEDCB
Définition du remodelage artériel
Pression Flux Lésion
Figure 1. Différents types de remodelage artériels, observés
en pathologie. Le vaisseau A représente le remodelage hyper-
trophique, tel qu’il peut être observé dans l’hypertension
artérielle. B représente le remodelage eutrophique (impli-
quant une réduction structurale de la lumière artérielle), C
(hypotrophique) et D (hypertrophique excentrique) représen-
tent l’adaptation à une diminution ou à une augmentation du
flux artériel chronique. E et F représentent les remodelages
de l’athérosclérose : E, l’hyperplasie intimale (resténose post-
angioplastie), F, l’athérosclérose avérée (d’après [1]).
STV, n° 2, vol. 16, février 2004
82
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

carotide primitive) présentent une hypertrophie excentri-
que, alors que les territoires musculaires (comme l’artère
radiale) sont l’objet d’un remodelage « eutrophique in-
terne », c’est-à-dire que le calibre de l’artère est réduit, avec
augmentation de l’épaisseur pariétale, mais sans augmenta-
tion de la surface de section pariétale [6].
Chez l’homme, le développement récent des techniques
d’échotracking de haute résolution et de la mesure automa-
tique de la vélocité de l’onde de pouls permettent des
mesures non invasives du diamètre de l’épaisseur du com-
plexe intima-media, (l’intima et la média sont impossibles à
distinguer au plan échographique) et de la rigidité artérielle
de grandes séries de patients. Il a été permis de définir les
caractéristiques géométriques des artères de gros et moyen
calibres dans de multiples conditions physiologiques et
pathologiques [7-9].
L’âge et la pression artérielle sont les deux principaux
déterminants du remodelage artériel. Ainsi, à âge égal, le
diamètre interne de l’artère carotide commune et celui de
l’aorte thoracique et abdominale sont plus grands chez le
sujet atteint d’hypertension essentielle permanente que
chez le sujet normotendu [10], tandis que celui d’artères
plus musculaires et distales, comme les artères fémorale
commune, humérale et radiale, reste inchangé [8]. Nous
avons récemment mis en évidence le rôle majeur des
contraintes pulsatiles dans l’épaississement de l’artère ca-
rotide primitive [11, 12]. En effet, la pression pulsée locale
est le plus puissant déterminant de l’épaisseur intima-
média (EIM) et de la dilatation.
L’épaisseur de l’intima-média est accrue chez l’hyper-
tendu, par comparaison à celle du normotendu de même
âge, tendant à normaliser la contrainte circonférentielle (cf
supra). Il est cependant à noter que la normalisation de la
contrainte est totale pour les artères de petit calibre, comme
l’artère radiale, mais qu’elle reste incomplète pour les
artères élastiques de gros calibre comme l’artère carotide.
Artères résistives de petit calibre
Les artères résistives sont définies par leur diamètre
interne : < 500 µm. La comparaison des divers modèles
d’hypertension permet de conclure que l’hyperplasie (aug-
mentation du nombre des cellules musculaires lisses) pré-
domine lorsque la masse vasculaire est augmentée, tandis
que ni l’hypertrophie ni l’hyperplasie ne sont observées
lors du remodelage, qui ne constitue qu’un réarrangement
d’une même quantité de tissu autour d’une lumière plus
petite [6].
Chez l’homme, les modifications géométriques des artério-
les du tissu sous-cutané peuvent s’étudier au travers de
vaisseaux isolés de biopsie de graisse sous-cutanée de la
fesse. Chez l’hypertendu, un remodelage pur est observé
(réduction de la lumière artérielle sans augmentation de la
section pariétale). L’étude ultrastructurale montre qu’il n’y
a ni hypertrophie ni hyperplasie cellulaire, mais réorganisa-
tion d’une même quantité de matériau autour d’une plus
petite lumière.
Raréfaction capillaire
L’autre hypothèse avancée pour expliquer l’augmentation
chronique, fixée des résistances périphériques dans l’hyper-
tension artérielle est la raréfaction artériolaire et capillaire.
L’observation princeps a été réalisée sur des modèles ani-
maux hypertendus, soit génétiques, soit secondaires. Elle
implique à la fois une moindre densité artériolo-capillaire
et une disparition de réseaux existants. Les phénomènes
d’apoptose sont au premier plan de la physiopathologie de
la raréfaction vasculaire.
Les conséquences sont multiples : augmentation fixée des
résistances, rapport perfusion/masse tissulaire défavorable,
source d’ischémie, augmentation des ondes de réflexion.
Chez l’homme hypertendu, de tels phénomènes existent,
avec un niveau de preuve moindre que chez l’animal, mais a
pu être démontré au niveau de la vascularisation digitale, et
du tissu sous-cutané graisseux. S’ajoute à cette raréfaction
du lit artériolaire, une modification de la géométrie des
bifurcations, dont l’angle tend à augmenter, ce qui génère
une augmentation des ondes de réflexion.
Coll
Coll
EL
EL
SMC
SMC
D
D
D
Ox
Ox
Figure 2. Organisation tridimensionnelle de la paroi arté-
rielle. (EL : élastine ; Coll : collagène ; SMC : cellules muscu-
laires lisses ; D : desmosomes ; Ox : Fibres Oxytalans) [5].
STV, n° 2, vol. 16, février 2004 83
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

Conséquences fonctionnelles
du remodelage artériel
au cours de l’hypertension
Artères de conduction et de compliance
Au cours de l’hypertension essentielle, les deux consé-
quences fonctionnelles majeures du remodelage artériel
sont :
– à court et moyen termes : la préservation des propriétés
élastiques de la paroi artérielle ;
– à long terme : la potentialisation de l’athérosclérose.
Préservation des propriétés élastiques
de la paroi artérielle
Les propriétés élastiques des gros troncs artériels jouent un
rôle fondamental dans le couplage des activités du cœur et
des vaisseaux et l’altération des artères de conduction
conditionne l’atteinte des organes cibles : cœur, cerveau,
œil et rein.
Au cours de l’hypertension, l’augmentation de la rigidité
des gros troncs artériels contribue à l’augmentation de la
pression pulsée. Cette hyperpulsatilité est un facteur de
développement de l’hypertrophie ventriculaire gauche [13]
et de l’augmentation de l’épaisseur intima-media des artè-
res de gros calibre et artérioles [10, 11, 14]. Un véritable
cercle vicieux est ainsi réalisé (figure 3). Le remodelage des
petites artères de résistance contribue à l’augmentation des
résistances périphériques, et donc de la pression artérielle
moyenne. En retour, la rigidité artérielle augmente au pro-
rata de l’augmentation de pression, et contribue à l’aug-
mentation de la pression pulsée centrale, facteur de remo-
delage des grosses artères et d’hypertrophie ventriculaire
gauche.
L’hypertrophie ventriculaire gauche est associée à une aug-
mentation de la morbidité et de la mortalité cardiovasculai-
res [15], et le remodelage hypertrophique des gros troncs
artériels favorise l’athérosclérose, source de complications
cérébrovasculaires, coronaires et artérielles périphériques
[20]. Dans ce tableau d’auto-aggravation des lésions au
cours de l’hypertension artérielle, il existe deux dogmes à la
vie dure : l’hypertrophie pariétale des artères de conduction
est assimilée à une augmentation de rigidité artérielle, et
l’hypertension est un vieillissement accéléré.
Ces deux dogmes sont faux.
L’hypertrophie de l’intima-média n’augmente pas la rigi-
dité du matériau constituant la paroi (module élastique de
Young) au cours de l’hypertension artérielle essentielle. Il
existe une autorégulation de la compliance artérielle au
cours de l’hypertension essentielle, grâce aux modifica-
tions structurales du tissu artériel compensant la perte de
compliance liée à l’augmentation de la pression [9].
Le remodelage artériel de l’hypertendu s’oppose en tout
point à celui observé au cours du vieillissement normal [10]
et de l’insuffisance rénale chronique [17], au cours desquels
l’hypertrophie artérielle s’accompagne d’une augmenta-
tion de la rigidité du vaisseau dans son ensemble, et du
matériau constitutif (figure 4).
Potentialisation de l’athérosclérose
L’hypertrophie pariétale est un facteur largement reconnu
d’athérosclérose.
Les plaques carotides d’athérosclérose sont plus fréquentes
chez les sujets dont l’épaisseur de l’intima-média caroti-
dienne est augmentée, tous autres facteurs de risque pris en
compte [18] (figure 5).
Les anomalies hémodynamiques de l’hypertension favori-
sent à leur tour les complications de la plaque d’athérome :
fissure, rupture et hémorragie, à l’origine d’une cascade
d’événements biochimiques conduisant à la thrombose ar-
térielle et à l’ischémie viscérale. La très grande complexité
des relations entre facteurs mécaniques et processus de
développement de l’athérosclérose pourrait expliquer le
trop modeste impact du traitement de l’hypertension sur les
complications de l’athérosclérose que l’on constate en pra-
tique clinique.
PA
PAM Pression Pulsée
Résistances
artériolaires Rigidité des
gros troncs
artériels
Remodelage des
gros troncs artériels
HVG
Remodelage des artérioles
Vasoconstriction
X
Figure 3. Pathogenèse du remodelage artériel et artériolaire
dans l’hypertension : les composants moyen (PAM) et pulsé
de la pression artérielle (PA) sont chacun des facteurs de
remodelage des artérioles, des gros troncs artériels (GTA) et
du ventricule gauche (hypertrophie ventriculaire gauche -
HVG). La vasoconstriction artériolaire, secondaire à l’aug-
mentation du tonus vasomoteur, augmente les résistances
périphériques, facteur d’hypertension. Le remodelage artériel
est un facteur « structural » de l’augmentation des résistan-
ces périphériques, à l’origine d’un véritable cercle vicieux. Le
remodelage des GTA n’entraîne pas d’augmentation de la
rigidité artérielle, au cours de l’hypertension essentielle.
L’augmentation de la rigidité artérielle est due essentielle-
ment à l’augmentation de la pression artérielle.
STV, n° 2, vol. 16, février 2004
84
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

Conséquences de l’augmentation
de la rigidité artérielle
L’augmentation de la rigidité artérielle est la conséquence
indirecte du vieillissement et de l’hypertension. La pression
pulsée, considérée comme un index de rigidité artérielle est
un marqueur de risque cardiovasculaire indépendant de la
pression moyenne. Dans ce contexte, il était intéressant de
tester si la rigidité des grosses artères était un facteur de
risque de mortalité totale et cardiovasculaire.
Nous avons suivi à l’hôpital Broussais pendant 9 ans une
cohorte de 1 980 patients hypertendus essentiels chez qui la
rigidité aortique a été évaluée initialement par la vitesse de
l’onde de pouls (VOP) [19-21]. Le résultat principal de ce
travail est que la vitesse de l’onde de pouls prédit la morta-
lité totale et la mortalité cardiovasculaire indépendamment
de l’âge, et de tous les facteurs de risques classiques. Sa
valeur prédictive est supérieure à celle de la pression pulsée
mesurée au bras. La rigidité artérielle est donc un marqueur
de risque de mortalité totale et cardiovasculaire, mais aussi
de morbidité chez l’hypertendu essentiel. L’augmentation
de risque de mortalité (toute cause et cardiovasculaire) est
d’environ 60 % pour une déviation standard de VOP
(4,5 m/s) avant ajustement, et de 40 % après ajustement sur
les autres facteurs de risque (figure 6).
Nous avons pu démontrer que la valeur prédictive de la
rigidité artérielle était comparable à celle donnée par le
score de Framigham [19], et que la combinaison des deux
informations améliorait la prédiction du risque, notamment
chez les sujets considérés à faible risque (figure 7). Dans
cette catégorie de patients (risque absolu à 10 ans < 12 %),
les patients avec les artères les plus rigides ont un risque
relatif de 5,80 de développer une cardiopathie ischémique
pendant le suivi. Nous avons plus récemment démontré que
la rigidité prédisait la survenue d’accidents vasculaires
fatals [20].
Artères résistives de petit calibre
L’augmentation du rapport « média/lumière » a plusieurs
conséquences fonctionnelles, les 3 premières étant délétè-
res et la 4
e
plutôt compensatrice :
1. Augmentation structurale des résistances vasculaires
périphériques.
Au cours de l’hypertension, le tonus vasoconstricteur est
augmenté. L’origine en est variable, d’un malade à l’autre,
et associe à l’évidence plusieurs facteurs causaux : aug-
mentation du tonus sympathique, augmentation de la réac-
tivité vasculaire par rétention sodée, activation du système
Normotendus
Hypertendus
Module élastique (kPa.10-3)
Contrainte circonférentielle (kPa)
0 150
jeune
moyen
âgé
0
4
P< 0,01
jeune
moyen
âgé
Augmentation rigidité
Figure 4. Relation entre la contrainte circonférentielle et la
rigidité (module élastique) de l’artère carotide primitive, chez
le normotendu et l’hypertendu. Dans les deux populations, le
vieillissement s’accompagne d’une augmentation de rigidité.
Chez l’hypertendu, il existe une augmentation de contrainte
circonférentielle, avec une augmentation de rigidité propor-
tionnelle, indiquant que les propriétés mécaniques du maté-
riau ne sont pas modifiées. Seuls les hypertendus jeunes ont
une augmentation de rigidité artérielle, sans augmentation de
la contrainte circonférentielle, indiquant une altération intrin-
sèque des propriétés élastiques de la paroi artérielle (d’après
Bussy et al. [10]).
Figure 5. Valeur prédictive de l’épaisseur intima-média de l’artère carotide primitive sur la
survenue de nouvelles plaques lors d’un suivi longitudinal de 4 ans (d’après Zureik et al.
[18]).
EIM carotidienne en prédiction du risque
de développement de plaque 1 010 patients âgés de 59 à 73 ans
Quartile 1 Quartile 2-3 Quartile 4
EIM < 0,56 mm 0,56-0,73 mm > 0,74 mm
n 226 561 223
Plaque, % 8,4 19,3 26
Ajust. Age et sexe OR 1 2,66 (1,58-4,46) 3,67 (2,09-6,44)
Ajust. Multivarié OR
1
1 2,48 (1,47-4,18) 3,20 (1,80-5,67)
Ajust. Multivarié OR
2
1 2,43 (1,44-4,11) 2,86 (1,60-5,11)
1
Ajusté pour l’âge, le sexe, tabac, hypertension, diabète, cholestérol, histoire de maladie coronaire.
2
Ajustement complet + présence plaques carotidiennes à l’inclusion.
STV, n° 2, vol. 16, février 2004 85
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.
 6
6
 7
7
 8
8
 9
9
1
/
9
100%