Pharmacogénomique en clinique : où en sommes

32e journée annuelle de pharmacothérapie
Centre d’information pharmaceutique
Hôpital du Sacré-Cœur de Montréal
Vendredi 24 mars 2017
Pharmacogénomique en clinique :
où en sommes-nous ?
Simon de Denus
pharmacien

1
Pharmacogénomique en clinique :
où en sommes-nous?
Simon de Denus, pharmacien, MSc (Pharm), PhD
Titulaire de la Chaire Beaulieu-Saucier en pharmacogénomique de
l’Université de Montréal
Professeur agrégé, Faculté de Pharmacie, Université de Montréal
Co-directeur du groupe en insuffisance cardiaque, Institut de
cardiologie de Montréal
Plan de la présentation
• Définition
• Généralités
• Exemples sélectionnés
• PGx et données probantes
• Conclusion

2
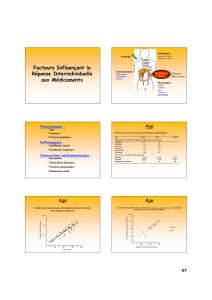
Pharmacogénétique/génomique
• Définition:
– L’étude de la relation entre les variations génétiques et
la variabilité dans les effets des médicaments.
Roden DM, et al. Ann Intern Med. 2006;145:749-57.
Pharmacogénomique
La pharmacogénomique – Génétique complexe
de Denus S, Phillips MS, Tardif JC. Pharmacogenomics.
R Brugada, ed. Spinger;2010:273-287.
ex: CYP2C19
ex: VKORC1
ex: HLA-B*5701
ex: facteurs de risque
génétiques d’une maladie

3
et répondeurs
“toxiques”
Potentiel de la pharmacogénomique
Patients avec un diagnostic donné
1
2
Répondeurs sans
prédisposition à un
effet indésirable
Non-répondeurs,
hyper-répondeurs
Traiter avec autre Rx
ou autre dose
Rx/dose habituels
Bientôt dans une clinique ou une
pharmacie près de chez vous!

4
Attitudes face à la PGx
0% 20% 40% 60% 80% 100%
Greffés
IC
Sains
% réponse
Oui
Non
Ne sait pas
Envisageriez-vous de vous prêter à un test pharmacogénomique visant
à examiner vos gènes si ce test pouvait vous indiquer qu’un
médicament en particulier pourrait être efficace pour vous?
Lachance K, et al. Pharmacogenomics J. 2014 Jul 1. doi:
10.1038/tpj.2014.29. [Epub ahead of print]
Accès aux résultats des tests PGx
0%
20%
40%
60%
80%
100%
% réponse
Sains
IC
Greffés
Lesquels parmi les professionnels de la santé suivants devraient
avoir accès à vos renseignements pharmacogénomiques?
Lachance K, et al. Pharmacogenomics J. 2015 Feb;15(1):13-9.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
1
/
32
100%