La culture prolongée : résultats de la co

Journée SMR
mt Médecine de la Reproduction, Gynécologie Endocrinologie 2012 ; 14 (4) : 311-8
La culture prolongée :
résultats de la co-culture embryonnaire
sur des cellules endométriales humaines
Résumé de la Journée thématique de la SMR sur le dialogue
blastocyste-endomètre
Prolonged culture: results for embryo co-culture on human endometrial cells
Juan Felipe Velez de la
Calle1
Nicolas Chevalier2
1Laboratoire Glasgow, Unité de
Fécondation in vitro, Clinique Pasteur,
34, rue du moulin à Poudre, 29200 Brest,
France
2Centre AMP Saint Roch, 43, rue du
Faubourg St-Jaumes, 34090 Montpellier,
France
Résumé. Les résultats de la fécondation in vitro en matière de taux de grossesses, restent encore
perfectibles. La culture prolongée jusqu’au stade du blastocyste, s’avère être une alternative très
intéressante pour améliorer lesdits résultats. En effet, le blastocyste, ultime stade cellulaire avant
la nidation, permet une meilleure sélection de l’embryon apte à la nidation. Par ailleurs, grâce
à l’obtention des blastocystes, nous pouvons mettre en pratique le transfert d’un seul embryon
(SET : Single Embryo Transfert) pour diminuer un effet péjoratif de l’assistance médicale à la
procréation (AMP) qui est celui de grossesses multiples. L’utilisation de la co-culture, en lieu
et place des milieux séquentiels, donne un bien meilleur rendement non seulement sur le
taux de grossesses exprimé en pourcentage de grossesses cliniques, mais sur leur évolutivité
et le nombre d’enfants nés à la maison. L’utilisation de cellules endométriales de la patiente
(étude Endocell) ou d’une donneuse pour constituer le support de cette culture, s’avère très
prometteuse.
Mots clés : blastocyste, culture prolongée, co-culture, cellule endométriale
Abstract. Results in IVF pregnancy rates are still perfectible. Prolonged culture to the blastocyst
stage proves to be a very interesting alternative to improve such results. Indeed, the blastocyst,
ultimate cell stage before implantation, allows us a better selection of embryos suitable for
nidation. In addition, by obtaining blastocysts, we can put into practice the transfer of a single
embryo (SET : Single Embryo Transfer) to reduce the not wished effect of AMP that is multiple
pregnancies. The use of Co-Culture, instead of sequential environments, gives us a much better
performance not only on the pregnancy rate expressed as a percentage of clinical pregnan-
cies, but their scalability and the baby take home rate. The use of endometrial cells from the
patient (Endocell trial from Genevrier Labs) or from a donor as a support of this culture is very
promising.
Key words: blastocyst, prolonged culture, co-culture, endometrial cell
Depuis des nombreuses années,
plusieurs auteurs [1, 2] ont
démontré en fécondation in vitro
(FIV), la supériorité en termes de
taux d’implantation et taux de gros-
sesses de la culture prolongée. Cette
technique permet l’obtention d’un ou
plusieurs blastocystes, comparée au
transfert effectué le plus fréquemment
à J2 ou J3 (13 à 17 % de transfert de
blastocystes vs 85 % de transfert à J2
ou J3 : rapport activité AMP 2010 de
l’ABM).
Ces études, comme le tableau 1
ci-dessous les résume [3], cherchent
à déterminer le moment idéal du
transfert et du type d’embryon à trans-
férer en vue d’obtenir une grossesse.
Comme on peut l’apprécier, ces tra-
vaux sont -pour la plupart- de nature
prospective et randomisée. La majo-
rité d’entre eux concluent à une
différence statistique significative en
faveur de la culture prolongée. Sans
vouloir rentrer dans des débats, ceux
dont les résultats ne vont pas dans le
même sens, montrent des chiffres en
termes de taux de grossesses très bas
par rapport aux moyennes observées
en routine dans les centres de FIV,
doi:10.1684/mte.2012.0436
médecine thérapeutique
Médecine
de la Reproduction
Gynécologie
Endocrinologie
Tirés à part : J.F. Velez de la Calle
311
Pour citer cet article : Velez de la Calle JF, Chevalier N. La culture prolongée : résultats de la co-culture embryonnaire sur des cellules endométriales humaines.
mt Médecine de la Reproduction, Gynécologie Endocrinologie 2012 ; 14 (4) : 311-8 doi:10.1684/mte.2012.0436
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

Journée SMR
Tableau 1. Études propectives comparant les taux de grossesses observés entre les transferts à J2-3 vs J5.
Auteur Étude D2/3 vs D5/6 p
Gardner DK, 1998 Prospectif, randomisé 30,1 % – 50,5 % <0,01
Patton PE, 1999 Prospective – don d’ovocyte 22%–52% <0,05
Coskun S, 2000 Prospective Randomized 21%–25% NS
Huisman GJ, 2000 Prospective 14,4 % – 15,5 % NS
Milki AA, 2000 Rétrospectif 20%–47% <0,001
Balaban B, 2001 Prospective 5,9%–15% <0,001
Langley MT, 2001 Retrospective – Oocyte donation 40,4 % – 54,1 % <0,05
Karaki RZ, 2002 Prospective Randomized 13 %–26 % <0,01
Levron J, 2002 Prospective Randomized 38.7 % – 20.2 % NS
Rienzi L, 2002 Prospective Randomized 35%–38% NS
Utsunomiya T, 2002 Prospective Randomized 11,7 % – 9,2 % NS
Van der Auwera I, 2002 Prospective Randomized 29%–46% <0,05
Wilson M, 2002 Retrospective 27%–43% <0,005
Emiliani S, 2003 Prospective Randomized 31,4 % – 29,4 % NS
Estes SJ, 2003 Retrospective 21%–23% NS
Frattarelli JL, 2003 Prospective Randomized 26,1 % – 43,4 % <0,05
Hreinsson J, 2004 Prospective Randomized 20.9 % – 21,1 % NS
Levitas E, 2004 Prospective Randomized 6 % – 21,2 % <0,01
Papanikolaou EG, 2005 Prospective Randomized 20,6 % – 37,3 % <0,001
Guerif F, 2009 Prospective 29,6 % – 43,6 % <0,01
traduisant probablement une culture embryonnaire et/ou
une méthodologie insuffisante.
Ces résultats, globalement très encourageants,
impliquent quelques éléments «pratiques »de l’assistance
médicale à la procréation (AMP) dans le cadre de la FIV.
En effet, le transfert au stade blastocyste nous permet
d’effectuer une assez fine et bien meilleure évaluation
de la qualité embryonnaire, évaluation qui reste jusqu’à
maintenant essentiellement morphologique. D’autant
plus que, si la culture prolongée est «poussée »un jour
de plus (J6), on peut assister à l’éclosion du blastocyste et
ainsi choisir sur les critères les plus fiables, l’embryon à
transférer.
Par ailleurs, le replacement de l’embryon dans l’utérus
à ce stade, peut être considéré comme étant encore plus
«physiologique »avec un environnement plus approprié
pour sa nidation car, à ce stade, l’embryon se trouve au
niveau de la muqueuse utérine, contrairement à l’embryon
de J2 ou J3 qui normalement est en transit au niveau de
la trompe. Or, nous savons que les conditions physico-
chimiques dans ces différents organes, ne sont pas les
mêmes – taux d’oxygène dans les trompes de 8 % vs 2%
dans l’utérus [4].
Par ailleurs, l’imprégnation en progestérone étant plus
importante (à distance de la ponction ovocytaire), elle
permet une contractilité utérine moindre et diminue les
éventuelles contractions post-transfert qui ont déjà été sus-
pectées comme étant délétères pour l’implantation car
l’embryon peut être rejeté par un simple effet mécanique
[5]. De plus, le transfert ayant lieu à distance de ladite
ponction d’ovocytes, les effets péjoratifs du phénomène
inflammatoire sous-jacent à la stimulation ovarienne sont
également diminués en favorisant par la même occasion
l’implantation [6-8].
L’autre avantage de la culture prolongée -et pas des
moindres-, est la probabilité de la mise en place du Single
Embryo Transfert (SET). En effet, à partir du moment où
nous disposons d’embryons avec un très bon potentiel
implantatoire, nous pouvons envisager le transfert d’un
seul embryon pour éviter les grossesses multiples qui
constituent un risque majeur et indésirable de l’AMP.
Par ailleurs, bien que nos méthodes de stimulation ova-
rienne s’améliorent sans cesse, que les indications soit
de mieux en mieux posées et que la culture embryon-
naire ainsi que toutes les techniques du laboratoire se
portent pour le mieux, on pourrait penser que les taux de
312 mt Médecine de la Reproduction, Gynécologie Endocrinologie, vol. 14, n◦4, octobre-novembre-décembre 2012
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

180
160
140
120
100
80
60
40
20
0
1986-1990
Taux de grossesses triples
N°/100 000 accouchements
1991-1995 2001-2005
1996-2000
Angleterre et pays de Galles Etats-Unis Finlande
Figure 1.
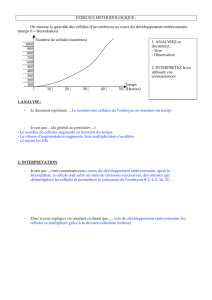
grossesses multiples iraient en diminuant comme le
montre la figure 1 [9] pour les grossesses triples. Cepen-
dant, au lieu de diminuer, les grossesses gémellaires
augmentent dans des pays comme les Etats-Unis et restent
assez élevées dans d’autres pays [9b] (figure 2). Compte
tenu des effets délétères de ce type de grossesse (grande
prématurité, complications obstétricales, etc.), des pays
comme la Belgique et la Suède se sont dotés d’une légis-
lation où le SET est obligatoire. Aujourd’hui en France,
l’arrêté sur le guide des bonnes pratiques prône de cher-
cher à diminuer le nombre d’embryons transférés (1 à 2).
Finalement, l’utilisation du SET permet aussi d’avoir
un taux de congélation embryonnaire plus élevé avec, par
conséquent, un meilleur taux de grossesses en cumulé.
Il faut citer finalement une meilleure cryoconservation
(congélation lente ou par vitrification), dans le contexte
des blastocystes comparé à celle des embryons de J2 ou
J3.
La culture prolongée
Avant la mise en place des milieux séquentiels cen-
sés apporter les différents «nutriments »à l’embryon pour
combler ses besoins métaboliques au jour le jour, on uti-
lisait entre autres (tableau 2) [3], des co-cultures faisant
appel aux cellules dites «Vero »en provenance de reins
de singes [10]. Pour des raisons évidentes concernant le
principe de précaution, elles ne furent plus du tout utili-
sées et toutes les équipes se sont cantonnées à l’utilisation
des milieux séquentiels. A signaler, l’arrivée sur le marché
d’un milieu de culture prolongée dit total, le Global [11]
et d’un autre tout récent, le CSCM [12] qui peuvent être
40
35
25
20
15
10
5
0
1970-
1979
1980-
1989
1990-
1999
2000-
2008
30
Taux de grossesses multiples/1000 accouchements
Décennies
Angleterre et pays de Galles Etats-Unis Australie
République tchèque Finlande
Figure 2.
employés dès la fécondation jusqu’au stade blastocyste,
donc, de manière non séquentielle.
Depuis, des progrès notoires ont été accomplis en
matière d’utilisation des cellules endométriales en tant
que support «idéal »pour nous permettre d’obtenir des
blastocystes avec un très haut potentiel implantatoire [13].
Dans le cadre des journées thématiques de notre
société, nous nous sommes intéressés à la culture pro-
longée sous forme de co-cultures, lesquelles semblent
aujourd’hui déterminantes pour la réussite de la FIV avec
l’obtention d’un très bon taux de grossesses. Ainsi, avec le
support des laboratoires Genévrier, nous avons organisé
fin 2010, un colloque sur la culture prolongée. Lors dudit
colloque, nous avons cherché à intégrer et à analyser, tous
les paramètres pouvant avoir une influence sur le résultat
final : «le blastocyste ». Dans cet article, nous voulons faire
le point sur cette journée thématique en apportant égale-
ment les différents progrès observés en la matière depuis
deux ans.
Les types de co-culture prolongée
Au moment de la réalisation de cette journée théma-
tique, deux méthodes de co-cultures existent actuellement
mt Médecine de la Reproduction, Gynécologie Endocrinologie, vol. 14, n◦4, octobre-novembre-décembre 2012 313
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

Journée SMR
Tableau 2. Différents types de supports employés dans le cadre des co-cultures embryonnaires.
Auteur,
Années
Contrôles Co-cultures
Origine cellulaire
%B %G %I %B %G %I
Cumulus
Saito, 1994 15,0 33,0
Quinn, 1996 31,0
Carrell, 1999 39,4 20,6 49,2 29,9
Fibroblastes Wetzels, 1998 30,0 18,0 27,0 17,0
Granulosa Plachot, 1993 3,0 6,3 30,0 5,9
Trompe bovine Wiemer, 1993 29,3 33,0 11,0 58,5 55,0 18,0
Trompe humaine
Yeung,1992 46,0 51,0
Bongso, 1992 21,4 10,4 37,0 31,0
Yeung, 1996 12,8 3,1 19,3 9,5
Weichselbaum, 2002 24,0 56,6
Trompe-endomètre Bongso, 1994 41,0 63,0
Endomètre
Desai, 1994 29,0 69,0
Jayot, 1995 8,0 21,0
Liu, 1999 18,2 51,8
Barmat, 1999 25,0 13,0 29,0 15,0
Menezo, 1990 3,0 61,0
Van Blerkom, 1993 38,5 45,6
Cellules Vero
Schillaci, 1994 10,0 19,0 68,0 50,0
Magli, 1995 37,5 19,0 7,0 38,0 18,0 10,0
Turner, 1996 46,0 77,0
D’Estaing, 2001 41,6 39,5 23,7 31,6 38,6 15,1
Cellules hépatiques de rat Hu, 1997 28,0 34,0
Cancer de l’ovaire Ben-Chetrir, 1996 23,0 33,0 39,0
en France qui font appel au même support cellulaire, celui
des cellules endométriales.
L’un d’entre eux, fait appel aux cellules de la même
patiente (étude Endocell), qui seront prélevées et conge-
lées lors d’un cycle précédant la ponction ovocytaire et
le transfert d’embryon, puis décongelées pour servir de
support à la culture embryonnaire dès J3. En résumé, une
biopsie endométriale est effectuée au préalable (≥1 mois).
Un système de transport des cellules endométriales est
adressé au laboratoire qui se chargera de la vérification
de la qualité du prélèvement et procédera à la congé-
lation de la biopsie. Lorsque la patiente aura son cycle
de stimulation suivant, le laboratoire du centre «mère »
(Genévrier) procède à leur décongélation lors du déclen-
chement de l’ovulation pour l’isolement et la culture des
cellules endométriales qui permettront la production d’un
tapis cellulaire en monocouches. Ce tapis sera transporté
au laboratoire d’AMP où la co-culture embryonnaire aura
lieu dès J2.
Pour valider cette méthode, il a été mis en place une
étude prospective randomisée entre co-culture autologue
endomètre-embryon avec un transfert à J5 comparée à une
culture traditionnelle avec un transfert à J3. Les objectifs
de l’étude étaient de comparer la technique Endocell®àla
technique de référence la plus utilisée en France (milieux
séquentiels), de promouvoir la culture de blastocystes
grâce la co-culture embryon–endomètre Endocell®et de
fournir des données scientifiques à J5 avec Endocell®.
Cette étude devait inclure 720 patientes et montrait une
différence de 15 % entre les 2 bras. Cette étude clinique
314 mt Médecine de la Reproduction, Gynécologie Endocrinologie, vol. 14, n◦4, octobre-novembre-décembre 2012
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

Tableau 3. Résultats du don d’ovocytes :
comparaison J3 versus J5 (janvier 2008 - septembre 2010)
J3 J5
Nombre total de cycles 1,949 978
Nombre total de transferts (%) 1,842 (97,2) 891 (91,1)
Taux de grossesses cliniques/transfert 50,0 60,5
Taux de fausses couches spontanées 17,0 14,8
Taux de Grossesses gémellaire 30,3 32,7
Taux d’implantations 33,4 45,0
menée depuis 2008 auprès de 230 femmes a permis de
démontrer que le pourcentage de grossesses cliniques
par transfert est de 50,7 % dans le groupe SCBT (Single
Cocultured Blastocyst Transfer/Groupe Endocell®), signi-
ficativement supérieur comparé à 33,0 % dans le groupe
contrôle SET (Single Embryo Transfer/Group à J3) ; p
= 0,02.
L’autre méthodologie, concerne des cellules de don-
neuses qui seront utilisées essentiellement dans des
programmes de dons d’ovocytes en parallèle avec la ponc-
tion d’ovocytes et la culture ultérieure des embryons.
Brièvement, la biopsie endométriale de la donneuse récu-
pérée est finement découpée et soumise à une digestion
enzymatique à 37◦C, suivie d’une sédimentation par gra-
vité qui permettra une adhésion cellulaire et l’obtention
d’une fraction riche en cellules épithéliales qui seront
mises en culture et serviront dès le départ de la culture
jusqu’à l’obtention du blastocyste.
Le tableau 3 ci-dessus montre les résultats obtenus à
l’IVI (Valence-Espagne) où la co-culture est comparée à la
méthode classique de transfert à J2-J3 sur une population
dédiée au don d’ovocytes.
Sans conteste et de la même manière que pour la
méthode Endocell, la co-culture embryonnaire et le trans-
fert de blastocystes, permettent d’obtenir un taux de
grossesses supérieur et statistiquement significatif.
Les «préalables complémentaires »
de la culture prolongée
Afin d’optimiser les résultats en matière de culture pro-
longée, les challenges de la Biologie de la Reproduction
sont importants et concernent essentiellement une amélio-
ration de la méthode de la culture embryonnaire en faisant
appel par exemple aux baisses de tensions et consom-
mation en O2 (cf. différences de tension entre la trompe
et l’utérus), aux analyses de micro-fluides (indicateurs
métaboliques) qui pourraient permettre l’identification
de biomarqueurs fiables, à la capacité d’implantation
de l’embryon à transférer (aujourd’hui, nous disposons
uniquement des paramètres morphologiques), en faisant
appel à des sciences telles que la transcriptomique, la
protéomique, la métabolomique.
Il faut citer également des techniques récentes dans
les laboratoires de Biologie de la Reproduction, où la
culture prolongée fut validée, voire, améliorée en termes
d’efficacité, grâce à l’utilisation de l’Intracytoplasmic Mor-
phologically Selected Sperm Injection (IMSI). En effet,
cette technique [14] qui permet de choisir le gamète mâle
avec un très fort grossissement, trouve tout son intérêt
lorsque la culture prolongée y est ajoutée. Ainsi, certains
auteurs ont constaté un ratio blastocystes/embryons supé-
rieur lorsque l’IMSI est utilisé au lieu de l’ICSI. Par ailleurs,
leurs observations concluent à des résultats montrant un
taux de malformations néonatales inférieur vs ICSI [15-
18].
Toutes ces variables, inconnues pour la plupart d’entre
elles, semble-t-il, peuvent être réunies en faisant appel à
la co-culture embryonnaire. En effet, le blastocyste obtenu
à l’aide de cette méthode de culture, semble «mieux
équipé »pour la nidation.
Pour ce qui est des progrès cliniques permettant
d’optimiser la culture prolongée, il faut tout d’abord
s’intéresser à la stimulation ovarienne et à son éventuel
impact sur la qualité ovocytaire et ultérieurement sur la
qualité embryonnaire.
En effet, depuis quelques années, les progrès de la sti-
mulation ovarienne se sont portés sur l’amélioration de
la stimulation des patientes (adaptation plus précise des
doses de FSH au départ), le confort pendant ladite stimula-
tion (Mild stimulation, protocoles antagonistes, réduction
du risque d’hyperstimulation, etc.), et la fac¸on de contrôler
davantage le taux des grossesses multiples (modification
de la politique de transfert avec le SET, amélioration des
techniques de cryoconservation avec l’avènement de la
vitrification, etc.).
La question reste donc posée : quel est l’impact de la
stimulation ovarienne sur la qualité embryonnaire ?
Sur ce point, les cliniciens doivent rester modestes car
la qualité ovocytaire (modification de la structure de la
chromatine, empreinte parentale, phosphorylation cen-
trosomes, etc.) est prédéterminée avant le début de la
stimulation. Cependant, certaines questions sont encore
en suspens sur l’impact des produits utilisés au cours de
la stimulation et la manière de les utiliser, sur la qualité
ovocytaire et par conséquent embryonnaire.
L’équipe de B. Fauser [19] a démontré qu’une
stimulation «légère »comparée à une stimulation
conventionnelle permet d’obtenir un nombre propor-
tionnellement plus important d’embryons euploïdes. De
même, dans une étude récente [20], la diminution des
doses de FSH conduit à un nombre total plus élevé de blas-
tocystes présentant moins d’anomalies chromosomiques.
Même si les résultats en AMP sont quasi identiques
sur un grand nombre de patientes quelle que soit la FSH
mt Médecine de la Reproduction, Gynécologie Endocrinologie, vol. 14, n◦4, octobre-novembre-décembre 2012 315
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.
 6
6
 7
7
 8
8
1
/
8
100%