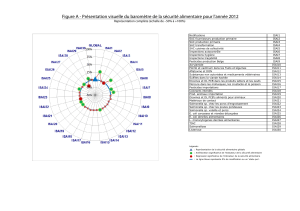
famille des Enterobacteriaceae

15/01/17
1
Les entérobactéries
ou
famille des
Enterobacteriaceae
DFGSP3 – 2016/2017
Pr Hélène MARCHANDIN
Habitat, mode de vie!
Commensales / mutualistes de l’homme +/- des animaux !
! ! !Tube digestif +++ nom!
Rôle utile : effet de barrière!
Bactéries isolées dans l’environnement
plantes, sol, eau
2!
Pathogènes :
• opportunistes mutualistes
• spécifiques (jamais mutualistes) :
ex : agents de la peste, de la typhoïde, …

15/01/17
2
Pouvoir pathogène!
Infections intestinales!
Infections urinaires!
Infections nosocomiales!
Infections respiratoires, de plaies, ...!
Infections chroniques
Bioterrorisme
Résistance aux antibiotiques multirésistance 3!
Caractères définissant les
entérobactéries!
Bacilles à Gram négatif, non sporulés!
Mobiles (flagelles péritriches), + rarement immobiles!
Aérobies-anaérobies facultatifs!
Culture sur milieu ordinaire!
4!

15/01/17
3
Dépourvus d’oxydase (-)
Possèdent une catalase (+)
Nitrate réductase + : nitrates nitrites
Fermentent le glucose
(avec ou sans production de gaz)
5!
Les principaux représentants!
P. mirabilis!Proteus!
S. marcescens! S Serratia!
E. aerogenes, E. cloacae! E Enterobacter!
K. pneumoniae! K Klebsiella!
Y. pestis, Y. enterocolitica!Yersinia!
S. dysenteriae!Shigella!
S. enterica!Salmonella!
E. coli!Escherichia!
Espèces principales!Genres!
> 80% des infections humaines
Autres genres: Citrobacter, Morganella, Providencia, …
(au total > 40 genres et 200 espèces) 6!

15/01/17
4
Caractères différenciant les espèces!
• Fermentation des sucres!
• Production de métabolites particuliers !
Indole (IND), H2S, acétoïne (VP), ...!
• Contenu enzymatique !
β
-galactosidase (ONPG), décarboxylases (LDC,ODC),
gélatinase (GEL), …!
7!
Identification par détermination du profil métabolique!
Ex : API 20E
!
Acidification du milieu et virage de l’indicateur coloré de pH
8!
ou détermination du profil protéique!
IDENTIFICATION D’ESPECE
Spectrométrie de masse
Technique MALDI-TOF Matrix Assisted Laser Desorption Ionization-time of flight
Identification des bactéries par analyse de leurs protéines totales

15/01/17
5
Définition de sérotypes au sein
d’une espèce!
Basée sur structure antigénique
des entérobactéries
• Ag les + utilisés : !
O : Ag de paroi toujours présents (LPS)!
H : Ag flagellaires!
Ag O!
LPS!9!
K : Ag de capsule
• Nombreux variants sur chaque Ag!
• Chaque variant Ag est reconnu par un antisérum
spécifique!
10!
IDENTIFICATION DE
SÉROTYPE ou SÉROVAR
Ex : E. coli sérotype 0157:H7
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
1
/
34
100%