1 - Bibliothèque et Archives Canada
publicité

ISABELLE CHOU INFLUENCE DES OESTROGENES ET DES FACTEURS DE CROISSANCE DÉRIVÉS DES OSTÉOBLASTES(M-3) SUR LES EFFETS DE L'ADRLAMYCINE SUR LES CELLULES DU CANCER DU SEIN (MCF-7). Mémoire présenté a [a facdté des études supérieures de I'Université Laval pour I'obtention du grade de maître ès science (M.Sc) FACULTE DE MEDECINE Biologie cellulaire et molécuiaire UNIVERSITE LAVAL AOUT 1997 O Isabelle Choki, 1997 1*1 National Library ofCanada Bibliothèque nationale du Canada Acquisitions and BibliographicServices Acquisitions et senrices bibliographiques 395 Wellington Street Ottawa ON K I A O N 4 395, rue Wellington Ottawa ON K1A ON4 Canada Canada The author has granted a nonexclusive licence dowing the National Library of Canada to reproduce, loan, distribute or seIl copies of this thesis in microfom, paper or electronic formats. L'auteur a accorde une licence non exclusive permettant à la Bibliothèque nationale du Canada de reproduire, prêter, distribuer ou vendre des copies de cette thèse sous la forme de microfiche/nlm, de reproduction sur papier ou sur format électronique. The author retains ownership of the copyright in this thesis. Neither the thesis nor substantial extracts fkom it may be printed or otherwise reproduced without the author's permission. L'auteur conserve la propriété du droit d'auteur qui protège cette thèse. Ni la thèse ni des extraits substantiels de celle-ci ne doivent être imprimés ou autrement reproduits sans son auto~ïsatim. Les femmes atteintes de métastases généralisées à partir du cancer du sein, présentent un très mauvais pronostic. Cependant les patientes soufhnt uniquement de métastases osseuses présentent une meilleure réponse au traitement chimiothérapeutique et par conséquent ont un pronostic favorable. Nous avons évalué la capacité des cellules phhotypiquement semblables aux ostéoblastes humains ( MG-63) et du milieu conditionné (CM) des cellules MG63 a influencer les effets cytotoxiques de l'adriamycine, I'un des agents chimiotherapeutiques les plus utilisés dans le traitement des cancers, sur des cellules du cancer du sein ( MCF-7), possédant le récepteur des oestrogènes (ER+) et répondant am oestrogènes. Nous avons constaté que l'oestradiol (E2; 100nM) diminue le nombre des cellules MCF-7 à la phase Gl/GO et augmente leur nombre dans les phases S et G2/M du cycle cellulaire, stimulant ainsi leur prolifération. E2 n'affecte ni la croissance ni la distribution des cellules MG43 dans les phases du cycle cellulaire. L'Adfiamycine (100nM) inhibe la croissance des cellules MCF-7 et MG-63 et bloque les deux lignées cellulaires dans la phase G2/M. De plus, elle augmente le nombre des cellules MCF-7 dans la phase G1/GO du cycle cellulaire en présence de E2. L'adnamycine (100nM) n'induit pas i'apoptose des cellules MCF-7 ni des cellules MG43, tel que démontré par la cytométrie en flux et l'analyse de I'ADN sur gel d'agarose simple. L'IGF 1 exogène augmente la prolifération des cellules MCF-7 tandis que le TGFPl l'bhî'be; contrairement B l'IN 1, le MG-63 CM et le TGFBI potentialisent l'effet cytostatique de l'adriamycine sur les cellules MCF-7. Ces résultats suggèrent que les facteurs de croissance dérÏvés des ostéoblastes, tel que le TGFP 1, peuvent augmenter l'effet cytostatique de I'adriamycine sur les cellules MCF-7 (ER+). Ainsi, ceci peut expliquer le pronostic favorable des patientes ayant le cancer du sein (ER+) avec seulement des métastases osseuses. Isabelle Choki AVANT-PROPOS Les travaux relatifs à cette étude ont été réalisés dans L e laboratoire d'Endocrinologie moléculaire du Centre Hospitalier de l'Université laval. Je voudrais remercier particulièrement mon directeur de recherche, le Docteur Michael Koutsilieris pour la confiance qu'il m'a témoignée et I'exceUent support scientifique qu'il m'a accordé tout au long de la réalisation de mon travail de recherche. Je le remercie aussi pour les conseils qu'il m'a prodigués au cours de mes études de maîtrise et pour sa disponibilité sans faille. Je désire aussi souligner le travail de M. Carlos Reyes-Moreno pour sa précieuse aide techaique. Je remercie également Pascal Koupaki et Léonie Quenum qui m'ont permis de poursuivre mes études; et Alain Saint-Cyr pour tout son support. Pour terminer, je dédie ce travail à toutes les femmes qui ont soufFert et qui so&ent de cancer du sein. Sespère qu'un jour ce mal sera définitivement enrayé. TABLE DES MATIERES PAGES I P RESUME.................................................................................i AVANT-PROPOS................................................................... .-. IU TABLE DES MATERES ...................................................... ..iv .. LISTE DES ABRÉVIATIONS .................................................vu CHAPITRE 1 INTRODUCTION.. ................................................................ -2 1 INTERET DE NOTRE ETUDE ............................................. 3 2 LA BIOLOGIE DU CANCER DU SEIN................................ 4 2.1 LES FACTEURS DE PRONOSTIC................................ 4 2.1.1 LES RÉCEPTEURS DES OESTROGENES ET DE LA PROGESTÉRONE................................... -4 2.1.2 D'AUTRES RÉCEPTEURS ET FACTEURS DE CROISSANCE............ . ...............................-6 2.1-3 L'AcTIwTÉ PROLIFÉRATIVE DES CELLULES TUMORALES........................................................ 6 2.2 LE DIAGNOSTIC DU CANCER DU SEIN........................ 7 3 LE CANCER DU SEIN &TASTATIQUE.. ........................ -7 3.1 LES &TASTASES OSSEUSES..........................................9 4 LE TRAITEMENT DU CANCER DU SEIN............................... 10 4.1 MASTECTOMIE ET TRAITEMENT CONSERVATEUR DU SEIN-.............. . . ........*...............*..**....-......*...*..*... 10 4.2 TRAITEMENTS ADJUVANTS....................................... 10 4.2.3 L'ADMAMYCINE:AGENT DE C ~ O T H É R A P E.........L 2 5 LE TRAITEMENT DU CANCER DU SEIN &TASTATIQUE ..........14 6 L'APOPTOSE......-...........................................................................-15 6.1 LES CARACTERISTIQUES MORPHOLOGIQUES ET BIOCHIMIQUES DE L'APOPTOSE......-...... . ............. 17 7 PROBLÉMATIQUE, OBJECTIFS ET STRATÉGIES EXPERIMENTALES........................................................................... 19 I CHAPITRE II LES FACTEURS DE CROISSANCE PRODUITS PAR LES OSTÉOBLASTESPOTENTLALISENT L'EFFET CYTOSTATIQUE DE L'ADEUAMYCINE SUR LES CELLULES DU CANCER DU SEIN HUMAIN.......................................22 # RÉSUME (en français)............................................................................23 Article: Osteoblast-derived growth factors enhance adriamycin-cytostasisof MCF-7 human breast cancer ........................................................................24 ceus. in vitro............... . CONCLUSION.....................................................................................65 ADN Acide désoxyribonucléique ADR Adrïamycine ARN Acide ribonucléique ARNm ARN messager MG63 CM Milieu conditionné des cellules MG-63 E2 17P-estradid EGF Epidermal growth factor ER- Estrogen receptor negative ER+ Estrogen receptor positive ETBCG Early Breast, Cancer Trialist, Collaborative group IGF 1 Insulin-like growth factor, type 1 PTH Parathyroid hormone TAM Tarnoxifene TGF Transfomiing growth factor TUNEL TdT-mediated digoxigenin-dUTP nick end labeling TNF Tumor necrosis factor CHAPITRE I INTRODUCTION 3 1. INTÉRET DE NOTRE ÉTUDE Notre intérêt p9ur cette étude repose sur des données cliniques très révélatrices. En effet, les femmes atteintes de métastases généralisées a partir du cancer du sein présentent un très mauvais pronostic. Cependant, des études ont montré que le site préférentiel des cellules métastatiques du cancer du sein est Pos et que les patientes souflkant du cancer mammaire (ER+) et ne présentant que des métastases osseuses semblent avoir un pronostic plus favorable que les patientes qui souffrent de métastases hépatiques et pulmonaires. Nous avons voulu déterminer la capacité des cellules semblables aux ostéoblastes humains (cellules MG-63), du milieu conditionné des cellules MG43 (MG-63 CM), et la capacité des facteurs de croissance dérivés des ostéoblastes, tels que I'IGF 1, et le TGFPI, a duencer la cytotoxicité de I'adriamycine sur les cellules du cancer du sein (MCF-7 ER+), in vitro. Nos résultats ont montré que le CM et le TGFBI augmentent l'effet cytostatique de I'ADR sur les cellules MCF-7. Du fait que la matrice osseuse est la seconde source de TGFBl après les plaquettes, il est concevable que l'augmentation de I'effet cytostatique de l'adnamycine médiée par le tissu hôte (l'os) puisse expliquer le pronostic favorable qui accompagne les patientes ayant le cancer du sein (ER+) et qui ont développe uniquement les métastases osseuses. Afin de permettre une meilleure compréhension des objectifs de notre étude, nous allons tout d'abord expliquer brièvement ce qu'est le cancer du sein en insistant sur le cancer du sein métastatique et les Herents traitements utilisés avant de présentar les quelques résultats que nous avons obtenus. 2. LA BIOLOGIE DU CANCER DU SEIN Les tumeurs malignes du cancer du sein sont, soit des carcinomes, développes à partir de Pépithelium des canaux galactophores ou des lobules; soit des sarcomes, nés de tissu conjonctif commun ou spécialisé, de tissu adipeux, vasculaire, nerveux, etc... En outre, il existe, d'autres localisations mammaires de processus tumoraux: lymphomes malins, mélanomes malins, métastases diverses. La valeur diagnostique et pronostique de la cytologie du cancer du sein fait référence aux carcinomes qui représentent 98% des tumeurs malignes du sein (1). 2.1 LES FACTEURS DE PRONOSTIC DU CANCER DU SEIN Un facteur de pronostic est une caractéristique de la tumeur ou de l'individu qui la porte et est en relation statistique avec la probabilité de surMe de la personne atteinte. Cette évaluation pronostique n'a de valeur que dans un groupe de sujets, mais en aucun cas pour un individu donné. Parmi les facteurs de pronostic les plus révélateurs, nous pouvons citer: LES RÉCEPTEURS PROGESTÉRONE. 2.1.1 DES OESTROGENES ET DE Ces facteurs ont deux intérêts, l'un pronostique et l'autre thérapeutique puisque la présence de récepteurs hormonaux est le garant d'une bonne efficacité de I'hoxmonothérapie. LA Ces récepteurs nucléaires appartiennent à une s u p e r f d e qui regroupe les récepteurs des androgènes, des glucocorticoïdes, des minéralocorticoïdes, des homones thyroïdiennes, de la vitamine D et de I'acide rétinoïque. Chaque récepteur est divisé en trois régions et six domaines (de A à F). La région E contient le site de liaison spécifique du stéroïde («~l&md binding domain»), sa structure quaternaire se modine lors de la liaison du ligand, démasquant dans le domaine C le site de liaison à l'ADN (CcDNA binding dom-). Celui-ci comporte une structure en doigt de zinc permettant la reconnaissance par le complexe homone-récepteur d'une séquence spécifique de l'ADN (<hormone responsive element>>) (2,3,4). Le récepteur existe sous une forme libre (4s) et sous une forme liée à des protéines (8s) qui bloquent le domaine de liaison à I'ADN et sont e1iminées lors de la liaison à l'hormone. Les récepteurs des oestrogènes sont retrouvés dans plusieurs types de tissus : ovaires, testicules, prostate, utéms, os, coeur, sein. En plus du récepteur " alpha" des oestrogènes , il a été prouvé récemment qu' il existe dans les tissus du rat, l'expression d' ARN messager d'un sous-type de récepteurs d'oestrogènes appelé recepteur "bêta" (B). Ce nouveau récepteur aurait une homologie d'environ 55% avec le récepteur "alpha". La signification biologique de l'existence de deux sous-types de récepteurs ci' oestrogènes reste a être élucidé. Cette existence pourrait expliquer les actions sélectives des oestrogènes dans les différents tissus cibles. Toutefois, 1' expression de 1' ARN messager de ce nouveau récepteur n'a pas encore été détectée dans les glandes mammaires,ni dans P os (3,4). Panni les facteurs impliqués dans le développement et la croissance du cancer du sein, les oestrogènes sont reconnus pour jouer un rôle prépondérant. La voie qui conduit à la prolifération cellulaire et a l'augmentation de volume de la tumeur, est le récepteur des oestrogènes. En effet, l'oestradiol doit se lier à son récepteur afin d'exercer son action. La fixation de l'oestradiol au récepteur entraine le changement de conformation du récepteur. Le complexe ligandrécepteur se lie à certains génes de la cellule cancéreuse qui contiennent les éléments de réponse aux oestrogènes (estmgen responsive element). Cette liaison déclenche les mécanismes qui conduisent à la division cellulaire et à la multiplication des cellules cancéreuses. La présence de ces récepteurs permet de combattre le cancer du sein en utilisant des anti-oestrogènes. Ces recepteurs ont une valeur pronostique moderée à côté de I'envahissement ganglionnaire et de la taille tumorale. Tous les auteurs s'accordent pour considérer que la négativité des deux récepteurs est un facteur de pronostic péjoratif. D'autres auteurs ont montré que des patientes souflkmt de tumeurs (Et+)avaient des métastases trois fois plus Wquents que les patientes présentant des tumeurs (ER-), (5) 2.1.2 D'AUTRES RÉCEPTEURS ET FACTEURS DE CROISSANCE Les récepteurs de la prolactine et des androgènes sont des facteurs prédictifs peu utilisés en pratique. Certains facteurs de croissance (EGF, IGF 1, TGF et leurs récepteurs), Les protéases, la cathepsine D, les activateurs du plasminogène, les oncogènes (c-myc. c-fos, c-myb), la protéine p53 sont activement étudiés. La liste n'est pas exhaustive. Aucun n'est actuellement utilisé en pratique car les phases d'évaluation clinique ne sont pas terminées. 2.1.3 L'ACTIVITÉ TUMORALES PROLIFERATIVE DES CELLULES Le pourcentage des cellules dans la phase S et la ploïdie sont des marqueurs efficaces du pronostic. L'homme, conune les espèces animales, a deux jeux de chromosomes identiques: les cellules de l'homme sont diploïdes (2x); mais dans le cas de cellules cancéreuses, on peut observer des cellules polyploïdes, tétraploïdes avec quatre copies de chaque chromosome (2). 7 2.2 DIAGNOSTIC DU CANCER DU SEIN Pour poser le diagnostic du cancer du sein, trois types d'examens sont nécessaires: clinique, fadioIogique et cytologique. Les données de ces trois examens doivent être associées dans le cadre du triplet concordant pour améliorer le diagnostic d'une lésion mammaire. En effet, les études statistiques montrent qu'un diagnostic de cancer, porté simultanément par Ies trois méthodes, triplet concordanf est exact dans 99 à 100% des cas. Ainsi, dans un triplet concordant, la cytologie fournit un diagnostic de certitude autorisant une décision thérapeutique. Dans le cas de triplet discordant, la vérification histologique s'impose. Le cytodiagnostic de malignité a plus de poids que les autres domees, étant donné sa valeur prédictive pour un cancer, soit 99 à 100%) (1). 3. LE CANCER DU SEIN METASTATIQUE La mortalité du cancer du sein est essentiellement liée aux métastases souvent précoces et silencieuses, précédant le traitement de la tumeur primitive. Certaines cellules du cancer mammaire expriment fortement des protéases capables de participer à la dégradation des structures avoisinantes et a la dissémination. Le développement des métastases est un processus complexe qui implique la cellule tumorale et l'hôte (1' organe). La cellule tumorale qui appdt dans un tissu (le sein dans le cas présent) se multiplie. Ces cellules forment une masse de cellules. Cette tumeur est encore "bénigne". Pour que cette tumeur progresse vers la malignité, les cellules néoplasiques doivent d'abord quitterl'endothélium et envahir les espaces vasculaires etlou lymphatiques. Toutes les cellules à phenotype maligne n'ont pas la capacité de subir le processus métastatique. Une fois dans la circulation, peu de cellules survivent au transport vers d'autres organes. Les cellules les plus agressives, qui ont survécu au transport, sont arrêtées dans la microcirculation. Bien que des facteurs mécaniques peuvent contribuer au processus metastatique, les molécules d'adhésion telles que les glycoprotéines de la f a d l e des intégrines semblent jouer un rôle important dans I'etablissement de sites micrornétastatiques. Ltangiogenèse, un autre phénomène biologique, joue également un rôle très important dans les métastases. En effet, c'est grâce à I'angiogenèse que des cellules ou des flots tumoraux peuvent migrer et croître (6). Cerîains facteurs de croissance présents dans la matrice extracellulaire sont angiogeniques. Dans un nombre non négligeables de tumeurs, il y a une corrélation entre I'angiogenèse d'une part et le potentiel métastatique d'autre part. L'invasion de sites métastatiques requiert la dissolution de la membrane basale. Ce processus est facilité par la production d'enzymes de dégradation par la cellule tumorale (protéases: cathepsines et métalloprotéinases). Des facteurs locaux, produits par les tissus dans lesquels les cellules tumorales s'arrêtent, peuvent promouvoir la croissance de nouveaux sites métastatiques. Il s'est avéré, par observation clinique, que le site préférentiel pour le développement de métastases à partir du cancer du sein soit l'os (7,8,9). Cependant, les fâcteurs qui attirent les cellules du cancer du sein dans l'os et les poussent à proliférer restent à être identifiés. 3.1. LES METASTASES OSSEUSES Les métastases osseuses sont une complication fréquente des cancers du sein avancés. Les études autopsiques révèlent jusqu'à 70% de métastases osseuses comparées aux 30% de métastases pulmonaires ou hépatiques. Si la maladie metastatique est limitée au squelette, la sunie peut être longue ( médiane a 2 ans) avec 20% de sUIMvants au delà de 5 ans. Les métastases osseuses des cancers du sein sont très souvent ostéolytiques, rarement ostéocondensantes ou mixtes. La destruction de la matrice osseuse est le résultat d'une augmentation de la résorption osseuse par les ostéoclastes. Les cellules tumorales sécrètent des cytokines ( TNFa et B, TGFa et P, interleukines, prostaglandines) qui stimulent l'activité, le recrutement et la diEérenciation des ostéoclastes (10). Les substances libérées par la résorption de la matrice (ostéocalcine, peptides, facteurs de croissance) pourraient être chimiotactiques pour les cellules tumorales et pourraient stimuler leur prolifération. Il existerait un autoentretien réciproque dans le tissu osseux, entre la destruction osseuse et la croissance tumorale. Parmi les manifestations cliniques des métastases osseuses, la douleur est le symptôme le plus fiéquent et est habituellement localisée à l'endroit où la métastase s'est installée. En plus de la douleur, on peut observer des fi-actures pathologiques, une compression de la moëlle épinière et une hypercaicémie (1 1)- IO 4. LE TRAITEMENT DU CANCER DU SEIN La règle est d'évaluer le n s q ~ evital a court terme et de déterminer le traitement adéquat pour chaque malade (6). 4.1 MASTECTOMIE ET TRAITEMENT CONSERVATEUR DU CANCER DU SEIN Lorsque la glande mammaire est envahie et représente un danger pour la suMe de la patiente, il est plus qu'indispensable d'avoir recours B la mastectomie qui consiste à ôter tout le sein atteint. Cependant dans certains cas, il est possible de pratiquer une exérèse régionale. La conservation doit pouvoir se faire avec des résultats esthétiques satisfaisants et complétée avec des traitements adjuvants (6,16) 4.2 TRAITEMENTS ADJUVANTS Pour guérir le cancer du sein, en plus de la chirurgie, on fait appel a la radiothérapie, à lliormonothérapie, a la chimiothérapie ou encore à la combinaison d'une ou de plusieurs de ces modalités thérapeutiques. s'agit d'un complément indispensable à la chirurgie limitée. En effet, après un traitement conservateur, I'absence de radiothérapie s'accompagne d'un taux élevé de rechutes locales dans tous les essais thérapeutiques. Son effet sur la survie globale est d'environ 12% mais non significatif (0.1%). L'hormonothérapie adjuvante du cancer du sein fait appel à l'administration d'antioestrogènes, tel que le tmoxiEene (TAM) et à la castration. Il existe trois méthodes de castration: la castration radiothérapeutique, chirurgicale, et l'utilisation des analogues de la luteinizing hormone-releasing hormone (LHRH)- Le tamosene est généralement un traitement de première Ligne à cause de sa tolérance et de sa faible toxicité. C'est un antioestrogène non stéroidien qui agit principalement par l'intermédiaire de récepteurs hormonaux. Il est égaiement doué d'un effet antitumod propre. Son utilisation chez les patientes ménopausées ne posent pas de problèmes aussi bien chez les sujets ER (+) que ER (-). Mais avant la ménopause, on observe beaucoup d'effets secondaires, tel que le développement du cancer de l'utérus. D'autres antioestrogenes , tel que le EM 800, sont en train d'être étudies au laboratoire d'endocrinologie du centre de recherche de luniversité Laval (C.H.U.L) par le groupe du Docteur Femand Labrie. La méthode de choix est la castration chirurgicale réalisée par coeliochirurgie. Les analogues de la LH-RH sont employés dans les cas où l'on souhaite une castration temporaire chez la femme jeune. Cependant, aucun essai thérapeutique n'a montré une équivalence éventuelle entre une castration temporaire et la castration dé£înitive. La castration entraine, après quinze ans, une réduction du risque de rechute de 10.6% dans le groupe castré par rapport au groupe non castré (6). 4.2.3 L'ADEUAMYCINE: AGENT DE CHIMIOTHÉRAPIE La méta-analyse publiée par IEBCTCG* donne des résultats globaux à 10 ans en terme de différence de suMe sans récidive de 8.4% et de 6.3% pour la mortalité en faveur de la polychimiotherapie adjuvante (6). Le protocole 4 AC (adriamycine, cyclophosphamide) est recommandé dans les indications courantes de traitement adjuvant. Les polychimiothérapies longues sont plus efncaces que les polychimiothérapies pré- ou peropéraîoires courtes. L'effet sur la survie sans récidive est acquis dans les cinq premières années alors que l'effet sur la mortalité se poursuit pendant les dix d e s d'études. L'adnamycine (ADR) est l'un des agents chimiothérapeutiques les plus souvent utilises dans le traitement des cancers (18,19). En effet, I'adriamycine est un antibiotique de la famille des anthracyclines (molécules dirigées contre les cellules qui prolifeent trop vite). La toxicité de cet agent sur les cellules tumorales serait mediée par plusieurs mécanismes: -intercalation d'adriamycine dans l'ADN entrainant l'inhibition de la biosynthèse de cet ADN, -Interférence avec la topoisornérase II et induction de cassures double-brin de l'ADN, -génération de radicaux libres, -altération de la fonction membranaire, -induction de la différenciation, -interférence avec le déroulement de l'ADN, -initiation de mort cellulaire apoptotique. L'explication possible pour toutes ces actions contradictoires serait que les différentes voies peuvent medier l'arrêt de la croissance et la mort cellulaire dans les lignées cellulaires tumorales spécifiques selon le profil biochimique du tissu particulier et selon les conditions expérimentales telles que la concentration d'adnamycine et le temps d'exposition. L'adn'amycine induit des cassures simple ou double brin de l'ADN associées à une protéine. Cette action a Lieu à des concentrations de l'ordre de 0.5 à 2.5pMol (20,2 1). La protéine associée aux cassures serait la topoisomérase II et le dommage serait catalysé par l'enzyme elle-même. La topoisomérase II est un cible commun pour beaucoup d'agents anticancéreux. Cette enzyme retirerait les noeuds qui résultent de certaines modifications de la superstructure de la double hélice. La suppression de l'enchevêtrement résulte du passage d'une hélice au travers de l'autre par coupure double brin. Lors de la coupure du brin de l'ADN, l'enzyme fotme avec le brin un complexe de clivage. Ltadriamycine, à des concentrations cytotoxiques et cliniques, stabilise le complexe de clivage. A des doses plus fortes, I'adriamycine inhibe complètement I'activité de passage du brui mais une fois le produit enlevé de l'ADN, on n'observe plus cette inhibition due à la topoisomérase II. Bien que l'adriamycuie soit Pun des agents cytotoxiques les plus utilisés, son utilisation est limitée du fait de nombreux effets secondaires (nausées, vomissements, dépression de la moelle osseuse, problème cardiaque, alopécie, etc..). Du fait de ces effets secondaires, les doses d'adriamycine sont déterminées suivant les antécédents de la patiente; et la malade doit rapporter toute indisposition à son médecin traitant. On essaie d'améliorer le bien-être des patientes en leur donnant d'autres médications qui permettent d'éviter les effets non désirables. Dans notre étude, nous avons choisi les doses de: -1 00 n M comme dose pharmacologique, - 10 ph4 comme dose supra-pharmacologique 5. LE TRAITEMENT DU CANCER DU SEIN MÉTASTATIQUE Le traitement du cancer du sein métastatique est palliatif, la place de la chirurgie n'est pas à négliger mais reste f ~ b l dans e cette situation. La radiothérapie au contraire est omniprésente et son effet palliatif est utilisé ponctuellement dans de nombreuses circonstances. Cependant c'est l'hormonothérapie et la chimiothérapie qui représentent véritablement la base du traitement du cancer du sein métastatique: toutes deux ont la capacité de prolonger (modestement) la survie et le pouvoir d'atténuer les symptômes qui handicapent la vie des malades. Pour chaque patiente se pose le choix du traitement systémique à employer. On peut indifféremment utiliser successivement I'hormonothérapie et la chimiothérapie, sans que la suMe des patientes en soit affectée. Le choix de la chimiothérapie se fera en fonction de I'état de la malade, des antécédents pathologiques, de l'urgence thérapeutique, de la toxicité des différentes drogues et de la connaissance personnelle que l'on a des protocoles utilisés (17). 6. APOPTOSE Ii est connu que tous Ies traitements anticancéreux, incluant la radiothérapie entraînent la mort des cellules cancéreuses par apoptose. L'apoptose, ou la mort programmée cellulaire est un processus physiologique important dans le développement normal et I'homéostasie des organismes multicellulaires. Il est codé par un programme endogène, conservé à travers Pévolution des métazoaires, résultant halement au suicide cellulaire. Lorsque les voies menant à l'apoptose sont dérangées, cela peut entraîner des conséquences graves telles que plusieurs maladies humaines incluant le syndrome d'immunodéfiscience, des maladies neurodégénératives, et le cancer (1 l,l2). Contrairement Papoptose, la nécrose est due à un échec général de régulation homéostatique suite a une blessure. Les cellules nécrotiques meurent par groupes et on observe une perte de l'intégrité de la membrane cellulaire et une réponse innammatoire très significative. Le processus de nécrose n'a pas besoin d'énergie, ni de synthèse de protéine et d'acide nucléique pour se dérouler. L'apparition et la croissance d'une tumeur résultent d'un déséquilibre entre la prolifération cellulaire et l'apoptose. La nécrose et l'apoptose sont les principales causes de la perte cellulaire. Des foyers de nécrose sont observés au centre des tumeurs peu vascularisées. L'apoptose spontanée des cellules tumorales est observée dans les tumeurs solides de toute taille, en périphérie aussi bien qu'en leur centre. Cette apoptose spontanée peut être amplifiée par la thérapeutique, par exemple par la privation hormonale dans les tumeurs homono-dépendantes. L'apoptose serait une réponse régulatrice active de cellules stimulables par un stimulus inducteur spécifique. Par exemple, une large variété d'agents cytotoxiques sélectionnés induisent l'apoptose seulement dans des cellules qui ont des voies de régulation appropriées. La plupart des traitements utilises contre le cancer peuvent induire l'apoptose des cellules tumorales. Les mécanismes d'induction dépendent des cellules traitées et du type de traitement utilisé. La première voie d'induction de la mort cellulaire programmée débuterait avec I'activation d'oncogènes non spécinques (c-myc. c-fos. c m ) . Au niveau des points de contrôle, cette voie d'activation est orientée vers I'apoptose en réponse aux signaux extracellulaires qui modulent leur activité (signaux inhibiteurs ou absence de signal). Les molécules classiques impliquées dans le cycle cellulaire, en particulier c-mye, c-fos, puis la protéine p53 sont activées. La cellule est cependant incapable de compléter le cycle cellulaire, probablement du fait de l'absence de signal mitogénique et meurt par apoptose. Un arrêt en G1 et surtout en G2 est une autre réponse observée dans les cellules tumorales traitées par un agent cytotoxique. Cet arrêt est interprété comme un moyen, pour la cellule traitée, de gagner du temps afin de réparer ses lésions avant de progresser plus loin dans le cycle cellulaire. Si elle n'en est pas capable, elle entre en apoptose à distance de l'arrêt en G1 ou en G2. La protéine p53 jouerait le rôle de point de contrôle avant le passage de la cellule de la phase G1 à la phase S du cycle cellulaire. Si I'ADN est altéré, la p53 inhiberait la progression daos le cycle cellulaire pour permettre à la cellule de réparer ses lésions. Si les réparations sont insufnsantes, la p53 orienterait le métabolisme cellulaire vers l'apoptose. La seconde voie d'induction est celle de la mort en interphase. L'apoptose est observée très rapidement dans les cellules tumorales traitées, moins d'une heure après le début du traitement. Le nombre de cellules apoptotiques est alors supérieur au nombre de cellules dans une phase donnée du cycle cellulaire. Tout se passe comme si la cellule était préprogrammée pour l'activation de la phase kale de I'apoptose, probablement l'activation d'une endonucléase. Les inhibiteurs de la synthèse des macromolécules n'ont aucune influence sur cette voie d'induction. Un changement du programme génétique de la cellule au cours d'un processus de différenciation, ou de signaux adressés à la cellule, peut moditier la sensibilité cellulaire à l'induction de I'apoptose. L'inhibition du processus apoptotique est quant à elle contrôlée par d'autres gènes tels que le bcl-2 (13). Le gène bel-2 apparait comme un nouveau type d'oncogène dont l'activation contribue au développement tumoral en inhibant la mort cellulaire. La protéine bcl-2 est exprimée au niveau de la membrane interne des mitochondries mais les mécanismes biochimiques de régulation de I'apoptose par cette même protéine ne sont pas encore connus. Son expression peut inhiber Papoptose et dans ce cas la cellule ne meurt ni ne prolifere. LES CARACTERISTIQUES BIOCHIMIQUES DE L'APOPTOSE 7.1 MORPHOLOGIQUES ET La membrane d'une cellule apoptotique garde son intégrité, la cellule rétrécit et forme finalement des corps apoptotiques. Aucune réponse inflammatoire n'est observée, les lysosomes sont intactes et la chromatine est compactee en masses unifonnément denses. Finalement la cellule est phagocytée par des cellules normales adjacentes ou par quelques macrophages. Les critères biochimiques sont induits par des stimuli physiologiques. Il s'agit d'un processus fortement regulé avec des étapes de synthèse et d'activation et qui nécessite de l'énergie. Ce processus requiert également la synthèse macromoleculaire et la transcription génique de novo. L'aspect biochimique principal est la hgmentation intemucléosornale de l'ADN (1 80 à 200 pb) résultant de l'activation d'endonucléases (1 4). Les femmes atteintes de métastases généralisées à partir du cancer du sein présentent un très mauvais pronostic. Cependant, des études ont montré que le site préférentiel des cellules métastatiques du cancer du sein est l'os et que les patientes qui ne soufEent que des métastases osseuses, développées a partir du cancer du sein semblent présenter un meilleur pronostic. L'utilisation de MDR, l'un des agents chimiothérapeutiques les plus utilisés dans le traitement des cancers constitue un paramètre déterminant dans la survie de ces femmes. Alors, nous avons voulu déterminer si l'environnement osseux modifiait les effets de I'adriamyciue sur les celIules métastatiques du cancer du sein, et le rôle des oestrogenes dans ce phénomène. Afin de déterminer si I'enviromement osseux modifiait la réponse au traitement à I'adriamyciue des cellules du cancer du sein (MCF-7), nous nous sommes fixés deux principaux objectifs. Tout d'abord, nous avons évalué les effets des facteurs de croissance dérivés des ostéoblastes humains sur les cellules cancéreuses du sein en présence ou en absence d'oestradiol. Dans un deuxième temps, nous avons étudié les effets des facteurs de croissance dérivés des ostéoblastes humains sur la cytotoxicité exercée par l'adnamycine sur les cellules du cancer du sein. Pour mener à bien notre étude, nous avons utilisé, comme modèle d'étude in vitro, les cellules de cancer du sein et les cellules humaines MG-63, une lignée provenant d'un ostéosarcome. La lignée ceMaire des MCF-7 a été établie a partir d'une patiente so&ant de cancer du sein. Ces cellules possèdent des récepteurs des oestrogènes et représentent un modèle in vitro très intéressant pour I'étude de la biologie du cancer du sein hormono-dépendant. Les cellules MG63 appartiennent à une lignée cellulaire humaine de type ostéoblastique, denvee d'un ostéosarcome. Quelques caractéristiques lui confeent Ie phénotype ostéoblastique permettant ainsi son utilisation comme modèle in vitro. En effet, ces cellules produisent des phosphatases alcaiines, de l'ostéocalcine et expriment le récepteur de la PTH. La production de I'AMPc est augmentée lorsque ces celiules sont stimulées par la PTH.Elles expriment également le récepteur de la vitamine D3, et les récepteurs des oestrogènes, augmentent l'expression de l'ostéocalcine en réponse aux oestrogènes et lorsque ces cellules sont cultivées sur des gels de collagène, l'expression du collagène de type I est stimulée. De plus, les lignées cellulaires MG63 et MCF-7 ont été utilisées de manière satifaisante dans la mise au point d'un système tridimensionnel de gel de collagène de type 1. Ce système permet de mettre en évidence la réaction de l'os dans les métastases osseuses, in vitro. Pour étudier les effets des facteurs de croissance, du CM des cellules MG-63 et de I'adriamycine sur les deux lignées cellulaires, nous avons eu recours à l'essai d'exclusion par te bleu de trypan, à la cytométrie en flux, à l'extrait et à l'analyse de L'ADN sur gel d'agarose, et à l'essai de détection de Papoptose dit de TLTNEL. La première étape de notre démarche expérimentale avait pour but de connaître les effets de I'adriamycine sur la prolifération et la croissance des deux lignées cellulaires par la méthode dexclusion par le bleu de trypan. Nous avons eu quelque réponses mais cette méthode ne nous a pas permis de déterminer l'effet cytotoxique de I'adriamycine sur les différentes cellules étudiées. Alors nous avons utilise la cytométne en flux, méthode plus sensible qui permet de mettre en évidence la distri%ution des cellules dans le cycle cellulaire. Nous n'avons pas pu voir des fragments d'ADN caractéristiques de I'apoptose avec I'andyse de I'ADN sur gel d'agarose, ni avec la méthode dite de tunnel. Ensuite, nous avons étudié les effets du CM, de TGFPl et de IGF I sur les cellules MCF-7. Nous avons choisi particulièrement ces deux facteurs de croissance parce que ce sont des facteurs qui sont abondamment produits par l'os. En effet, après les plaquettes, l'os est la deuxième source de production de TGFB 1. Les détails concernant les méthodes utilisées et les résultats des étapes de notre démarche expérimentale sont présentés dans le chapitre suivant. CHAPITRE IL LES FACTEURS DE CROISSANCE PRODUITS PAR LES OSTEOBLASTES POTENTIALISENT L'EFFET CYTOSTATIQUE DE L'ADRIAMYCINE SUR LES CELLULES DU CANCER DU SEIN HUMAIN Les rapports cliniques montrent que les patientes so&ant seulement de métastases osseuses développées a partir de cancer du sein homonodépendant (ER+) semblent avoir une progression plus lente et un meilleur pronostic. Nous avons déterminé la capacité des cellules MG63 et de leur CM à influencer la cytotoxicité de l'ADR sur les cellules MCF-7 (ER+) du cancer du sein. Le I7a-oestradiol (E2; 100nM) diminuait la distribution des cellules MCF-7 au niveau des phases Gl/Gû et augmentait celle-ci dans les phases S et G2/M du cycle cellulaire, stimulant ainsi la croissance des cellules MCF-7. E2 n'affecte ni la croissance ni la distribution des MG-63 dans le cycle ceildaire. L'adriamycine (100nM) inhibait la croissance des cellules MG-63et MCF-7 et les arrêtait à la phase G2/M du cycle cellulaire. Mais en présence doestradio1 (lOOnM), I'adriamycine augmente le nombre de cellules dans la phases GUGO du cycle cellulaire. L'adnamycine n'induit pas I'apoptose des cellules MCF-7 ni des cellules MG63, comme démontré par la cytornétrie en flux et par l'analyse de l'ADN sur un gel d'agarose simple. Contrairement à I'IGF 1, le TGFPl et le milieu conditionné des M G 4 3 inhibaient la croissance des cellules MCF-7. Le milieu conditionné et le TGFP1 augmentaient l'effet cytostatique de l'adrirnycine sur les cellules MCF-7. Ces résultats suggèrent que les facteurs de croissance dérivés des MG-63, tel le TGFBl peuvent augmenter l'effet cytostatique exercé par l'adriamycîne sur les cellules MCF-7 (ER+). D'une manière concevable, ces résultats peuvent expliquer le pronostic favorable des patientes souffrant de métastases localisées uniquement au niveau de l'os. OSTEOBLAST-DERIVED GROWTH FACTORS ENHANCE ADRIAMYCIN-CYTOSTASIS OF MCF7 HUMAN BREAST CANCER CELLS, IN VITRO. Isabeiïe CHOKl (l), Antigone SOURLA (l), Carlos REYES MORENO (l),and Michael KOUTSILIERIS (1,2) (1) Molecular Endocrinology Laboratory, Research Center, Pavillon C.H.U.L-C.H.U.Q, Laval University, 2705 Boul. Laurier, Ste. Foy, Quebec, G l V 4G2, Canada, and (2) Department of Physiology, Medical School of Athens, National and Kapodistrian University, 75 Micras Asias, Goudi, Athens 115 27, Greece. Address correspondence to Michael Koutsilieris, MD, Ph.D, Molecular Endocrinology Laboratory, Research Center, CHUL-CHUQ, Ste Foy, G1V 4G2, Quebec, Canada. Phone: (418) 654 2296; Fax: (418) 654 2761; e-mail: michael.koutsü[email protected]. Key Words: Breast cancer, bone metastasis, adriamycin, apoptosis, cytostasis. ABSTRACT Bone ody metastasis in patients with estrogen receptor (ER)-positive breast cancer reported to have a favorable response to chemotherapy, a favorable prognosis, and an "indolent7' course. Therefore, we assessed the ability of MG43 osteoblast-like human osteosarcorna celis (MG-63 cells) and MG-63 conditioned media (CM) to influence adriamycin-cytotoxicity of ER-positive MCF-7 human breast cancer cells. 17P-estradiol (E2; 100 nM) increased the distribution at S and G2M phases in the cell cycle and stimulated the growth of MCF-7 cells. E2 did not affect the growth and phase distribution of the MG63 cells. Adriamyein (100 nM) inhiiited the growth and arrested the MCF-7 cells supplemented with or without lOOnM of estradiol [(-E2) and (+E2) MCF-7 cultures] at G 2 N phase in the ce11 cycle. In addition, adriamycin (100 u M ) uicreased the distribution at GVGO phase in the ceU cycle of (+E2) the MCF-7 cultures. Adriamycin (100 nM) did not induce apoptosis of MCF-7 cells as assessed by flow cytometry and analysis of DNA fragmentation on simple agarose gel. Exogenous insulin-like growth factor 1 (IGF 1) stimulated while transfomiing growth factor beta 1 (TGFP 1) and MG63 CM inhibited the growth of MCF-7 cells. Furthennore,The MG-63 CM and TGFB 1 enhanced while IGF 1 reversed the adriamycin (100 nM)cytostasis of MCF-7 cells. These data suggest that osteoblastic CM contained growth factors, such as TGFB I capable of enhancing adnamycui-cytostasis, in vitro. Conceivably, these osteoblast-derived "enhancers" of chemotherapycytostasis c m explain the favorable prognosis and "indolent" course of ERpositive breast cancer patients with bone only metastasis. INTRODUCTION Breast cancer is the most common malignant tumor and the second leading cause of tumor-related death in women. One third of women with breast cancer is expected to develop metastasis and eventually to die fiom disease progression at the sites of metastases (1). Although metastasis cm develop in any organ, bone, Iiver and lung are the most fiequent sites of metastasis, excluding lymph nodes, and bone is the most common fkst site of metastases fiom breast cancer (2). The specific factors which result in the hi& fiequency of skeletal metastasis in breast cancer are yet to be defined (2,3). The type of metastatic lesions in bone c m be lytic, blastic and mixed (4). The blastic lesions are associated with tumor-derived growth factors for osteoblasts, an osteoblast-mediated mechanism (4) and Iytic lesions with either an osteoclast-mediated or tumor-mediated bone resorption (46). Among the local moddators involved in the local reaction of bone metastasis, overexpression of urokuiase type plasminogen activator @PA) and its receptor (uPA.R) is thought to activate plasminogen to plasmin, which in its tum, activates ma& metalloproteases dereguiating directly bone rnatrix deposition (7) or acting via limited hydrolysis of insulin-Iike growth factorbinding proteins (IGFE3Ps) and latent-transforming growth factor beta 1 (latent-TGFB1). The increased bioavailability of growth factors in association with a deregulated metaUoproteases/metalloprotase inhi'bitors activity possibly mediate the pathophysiology of the lytic and the bIastic bone metastases (4-9). Because estrogen receptor (ER) positive breast cancer patients with bone only metastases reported to have a favorable response to chemotherapy, "good" prognosis and an "indolent" course compared with that of patients with liver and lung metastases (10-12), we assessed the ability of the MG-63 osteoblast-like human osteosarcoma cells, MG-63 conditioned media (MG63 CM), and osteoblast-related growth factors such as IGF I and TGFB 1 to influence adriarnycin-cytotoxicityof ER-positive MCF-7 human breast cancer ceus, in vitro. We documented that adriamycin (100 nM) arrested the progression of the MCF-7 breast cancer cells at G2M phase in the cell cycle without producing apoptosis. In addition, adnamycin (100nM) arrested at Gl/Gû phase in the ceIl cycle the MCF-7cells only when supplemented with 100 n M of estradio1 (E2). Furthemore, MG-63 osteoblast-iike ceus, MG63CM and TGFB1 enhanced whîle IGF 1reduced the adriamycin (100 nM)-cytostasis of MCF-7 cells. Therefore, it's conceivable that osteoblast-derived "enhancers" of adriamycin-cytostasis potentiate favorable response to cytotoxic chemotherapy, thereby resulting in favorable prognosis and "indolent"course of ER-positive breast cancer patients with bone only metastases . MATERIALS AND METHODS Ce11 lines and ceil culture assays MG63 osteoblast-derïved human osteosarcoma ceUs and PC-3 human prostate cancer cells were obtained h m the Amencan Type Ce11 Culture (ATCC, Bethesda, MD). In our study, the PC-3 cens were used as positive controls for the analysis of adriamycin-apoptosis "DNA fragmentation" on simple agarose gel and three-dimensional type 1 collagen system. MCF-7 human breast cancer ceIls were obtained fiom Dr. Claude Labrie, CHüL, Laval University, Quebec, Canada. The MG-63, PC-3 and MCF-7 cells were grown in 75-cm2 culture flasks using Dulbecco's rnodified Eagle's medium/F12 @MEME-12, GIBCO/BRL, Gaithersburg, MD) containhg 5% calf senun (CS) and 100 nM of l7B-estradiol (ES; Sigma, St. Louis, MI) depending on the experiment. The M G 6 3 and MCF-7 cens were plated at a ceU density of 10,000 cells in 24-well plates and grown with DMEM/F-12 phenol red-fiee medium containing 5% of CS pretreated with dextran coated charcoal (CS-DCC). The MCF-7 human breast cancer cells contain estrogen receptor (ER), thereby representing a reliable in vitro mode1 for sîudying the molecular events associated with response to chemotherapy of ER-positive breast cancer cells ( 13,14 and ref. therein). MG-63 human osteosarcoma cells are well-characterized osteoblast-like osteosarcoma cells that express alkaline phosphatase, osteocalcin, parathyroid hormone receptor (PTHR), increase CAMPproduction in response to PTH, express vitamin D3 receptor, estrogen receptor (ER), increase osteocalcin expression in response to estrogen, and enhance expression of type 1 coUagen when cdtured on collagen gels (15,16 and ref. therein). The MG-63, PC-3 and MCF-7 ce11 lines were successfully used in the development of a three-dimensional type 1 collagen gel system which produced for the fust t h e the morphological evidence of the local bone reaction (local and lytic reaction), in vitro (1 7,18). Cytotoxicity assays The number of alive (A) and dead @) ceus was analyzed by ttypan blue exclusion MG-63, and MCF-7 cultures exposed to 100 nM and 10 ph4 of adriamycin (Sigma, St. Louis) for 6 hr, 24 hr and 48 hr. The MG43 and MCF-7 cells were plated at lO,OOO ceUs/well and cultured with DMEM/F-12 phenol red-fiee containing 5% CS- DCC treated for 24 hr in presence or absence of 100 nM of 17P-estradiol ( 3 2 ) for 24 hr. Then cells were washed with senun-fkee medium and cultured with DMEM/F-12 phenol red-fiee medium containing 5% CS-DCC supplemented with or without 100 nM E2. The media contained also 100 nM or 10 pM of adriarnycin depending on the experiments. The dive (A) versus dead @) ceUs ratio was computed ( A D ) and compared with that of adriarnycin-kee cultures. The AîD ratio was calculated by dividing the mean values which refereed to the number of alive cells vs that of dead MCF-7 cells, as were computed by triplicated determinations. Detection of apoptosis on simple agarose gel Apoptosis was assessed by detecting DNA ladders of multiples of 180 base pairs "DNA fragmentationt' on simple agarose gel electrophoresis of total cellular DNA (19). In bnef, DNA was extracted fiom MG-63, PC-3 and MCF-7 cells which were detached by ûypsin, pooled and lysed in 5 mM Tris (pH 7.4), 5 m M EDTA, and 0.5% Triton X-100for 2 hr on ice. The lysate was centrifùged at 27,000~g for 20 min. The supernatant was incubated with 200 p g / d proteinase K for 1 hr at 5 0 ' ~ and extracted with phenol/chloroform; then DNA was precipitated overnight at - 2 0 ' ~ in 2 volumes of ethanol and 0.13 M NaCl with 20 ug of glycogen. After treatment with 1 m g / d boiled bovine pancreatic RNase A for 1 hr at 50°c, the DNA was loaded (15 pg) onto a 2% horizontal agarose gel containing 0.3 pg!d ethidium bromide and run in ixTBE (Tns/Borate/EDTA) b e e r at 4.0 V/crn. Gels were photographed under UV light with Polaroid 57 type film (19). Phase distribution in the ceil cycle and detection of apoptosis by fîow cytometry The indices of cell cycle and apoptosis were assessed by flow cytomev analyzing DNA content in propidium iodide (PI) stained cells with a counter EPICS 753 pulse cytometer (Coulter counter, Hideah, FL) (20). In brief, adriamycin treated and adnamycin-fkee (control) MCF-7 and MG63 cells were cdected (3.0-7.5~100,000ceus) and resuspended wiîh 150 pl of icecold 1X PBS. Then ceUs were k e d with 350 pl of absolute ethanol and incubated on ice for 30 min. M e r centrifûgation, ceils were resuspended with 300 pl of 1X PBS containing 50 p g M PI and 1 m g h l RNase A. Then cells were incubated at 3 7 O ~for 30 min and analysed on EPICS 753 pulse cytometer. The MG-63 and MCF-7 cells were exposed to 100 n M and 10 p M of adnamycin for 6,24, and 48 hr cultured with DMEM/F-12 phenol red-f?ee media supplemented by 5% CS-DCC and 100 n M E2, depending on the experiment. We analyzed apoptosis (hypodiploid ceils; <G1) and computed the % of apoptotic cells and phase distribution of MG63 and MCF-7 cells into the cell cycle (20). Results were expressed as % of cens in GUGO, S, G2/M phase in the cell cycle, and as % of the total cells at apoptosis (<Gl). The eff'ts of IGF 1, TGFP 1, M G 6 3 CM on the growth of MCF-7 cells and against adriamyein-cytostasis Because IGF I and TGFP 1 are very important autocrine and paracrine factors of bone pathophysiology (7-9), we analyze the ability of recombinant human IGF-I and TGFB 1 (R&D Systems) to innuence adrïamycin-cytotoxicity of MCF-7, as assessed by the alive (A) vs dead @) cens (ND) ratio in monolayer cultures. MG63 conditioned media (CM) prepared using confluent M G 6 3 cell cultures which were grown in 225-cm2 culture flasks using DMEME-12 without CS. CMs were collected every 48 hr, pooied together and centrifuged at 3,000 rpm for 3 min. The supernatant was then filtered over protein filters ~ Ï t hcut-off molecular weight (MW) of 15,000 ddtons (Amicon Inc., MA, USA). Increasing dose of CM containing nom 1 ngM up to 100 p g l d ( h a 1 concentration in culture-well) were tested in MCF-7 cells assessing ceU growth (number of ceîls); and then 50 pghd (maximum bioactivity) of MG63 CM was andyzed for its putative action against or for adrïamycincytotoxicity in MCF-7 ceus. Three-dimensional type 1 coiiagen gel system (3-D system) Collagen was prepared in our laboratov using native type 1 collagen extracted from rat tail tendons (17). We used this type I collagen in an aqueous solution containing 0.002 M acetic acid in a final concentration of 1.5 mglrnl. Three-dimensional gels of native collagen type I were prepared in 24-weU plates by rapidly mùang MG-63, MCF-7 tells, or both ce11 types with type I collagen in a b a l concenîration of 106 celldml of collage* gel. The collagen gels were let for 30 min at 3 7 ' ~ and then incubated in a hurnidined CO2 uicubator using 1 ml of DMENUF-12 containing 5% CS and 100 n M ofE2 (17,18). In addition, we prepared collagen gels containing mixed cell populations of 0 . 5 ~ 1 0of~ MG-63 and 0 . 5 ~ 1 0of~ MCF-7 ceUs (final concentration 106 ceLIs/ml of gel). Both the MG-63 and MCF-7 celIs were homogeneously dispersed into the type 1 collagen gel (1 7,18). After 24 hr, we changed culture media and added 100 nM of adriamycin for 48 hr. Control coflagen gels were cdtured without adriamycin under identical experimental conditions. Control collagen gels were cultured without adnamycin containing only MG-63 cells, only MCF-7 cells, and mixed MCF-7 and MG-63 cells]. Detection of adriamycin-a poptosis and adriamycin-cytostasis in 3-D system After 48 hr exposure to 100 nM of adnamycin coUagen gels underwent fixation with phosphate buffered fonnalin 10% for 4 hr and then were routinely processed and embedded in paraffin blocs. Serial sections were of 5 pm were cut and stained with the classic trichrome-Masson techniques as described previously ( 17,18) or processed for TdT-mediated nick end labeling method for detection of apoptosis (TIMEL assay). The sections consecutive to those stained with the TUNEL assay (ONCOR, Inc., USA; TdT-mediated nick end labeling)] were stained wiîh standard hematoxylin/eosin to evduate histologicd featwes of apoptosis, ïncluding ceIl shrinkage, chromaiin condensation, and apoptotic body formation. Cytostasis was assessed by counting the number of MCF-7 and MG-63 cells in 5 serial sections of 3-D system before and after adriamycin exposure. RESULTS 1. Adriamycin cytotoxicity of MCF-7 ceUs in monolayer cultures. Exposure to 100 nM and 10 pM of adriamycin for 48 hr remarkably decreased the number of MCF-7 cells as compared with that of adnarnycin~ e cultures e (controls). This was suggestive of a potent cytostatic andor cytotoxic action (Fig. 1; upper panel). It is noteworthy that 100 n M of E2 resulted in higher number of MCF-7 cells growing in adriamycin-fiee (control) cultures as compared with that of adnamycin-free cultures rnaintained in E2-fkee media (Fig. 1; upper panel). The number of dead MCF-7 cells did not ùicrease sigdcantly d e r the exposure to pharmacological (100 nM) and suprapharmacological (10 pM) doses of adriamycin for 24 hr and 48 hr as assessed by trypan blue exclusion [(-E2) MCF-7 cultures; control = 400 70 ; adriamycin (100 nM) = 540 + 110; Adriamycin (10 pM) = 430 + 80; Number of dead MCF-7 cells; X + SE] and [(+E2) MCF-7 cultures; control = 520 2 100 ;adnamyein (100 nM) = 530 t 105;adriamycin (10 pMj = 440 90; Number of dead MCF-7 ceUs (X + SE)]. These data suggested that adnamycin did not produced or apoptosis in MCF-7 cells. + + Because the analysis of adriamycin-cytotoxicity cannot be assessed without taking into consideration the number of alive cells in each culture, cytostasis probably decreases cytotoxicity, we computed the alive (A) vs dead @) cells ratio of MCF-7 cultures incubated with and without adriamycin in the presence and absence of 100 nM o f E2. Adriamycin decreased A/D ratio of MCF-7 cells. In (-E2) MCF-7 cultures the A D ratio was decreased kom 28.9 (controls; adriamycin-free) down to 18.95 (IO0 n M ofadriamycin) and to 12.5 (10 p M of a b y c i n ) . In (+E2) MCF-7 cultures the A/D ratio was decreased fiom 42.8 (controls; adriarnycin-&ee) down to 20.5 (100 n M of adriamycin) and to 12.5 (1 0 pM of adriamycin) (Fig. 2). To c o h the adnamycin-cytotoxicity, we analyzed adriamycin-fkee vs adnamycin-treated MCF-7 cells using flow cytornetry 1% distribution of MCF-7 cells in GUGO; S; G2M phase in the ce11 cycle, and % of hypodiploid cells (<G1= DNA fragmentation)J .The MCF-7 cultures were supplemented with or without 100 n M of EL. E2 (100 nM) signincantly changed the phase distribution in the ceU cycle of the MCF-7 cells. This included a decrease in the distribution of MCF-7 cells at Gl/GO phase and an increase of that at S phase in the cell cycle (Table 1). These changes apparently resulted in the increased number (Fig. 1 ) and the increased AD ratio (Fig.2) of (+E2) MCF-7 cultures, as compared with that of (-E2) MCF-7 cultures (Fig. 1; upper panel). In addition, few apoptotic/necrotic cells were detected in MCF-7 cultures in either (-E2) or (+E2) culture conditions [<G1 = 1-3%] (Table 1). These data corroborated the results of trypan blue exclusion which detected similar number of dead cells in either experimental conditions [(-E2); controls = 400 f 70 and (+E2); controls = 520 i1001.Therefore, the increased number (Fig. 1) and increased A/D ratio of (+E2) MCF-7 cells (Fig. 2) were the result of an enhanced rate of proiiferation produced by the 100 n M of E2 in MCF-7 cultures (Table 1). However, exposure to adnamycin changed the phase distribution of the MCF7 cells in a tirnedependent (6 vs 24 vs 48 hr) and dose-dependent (100 nM vs 10 CrM) manner. Indeed, 6 hr exposure to 100 nM and 10 p M of adriamycin produced Little change in the phase distn'bution of MCF-7 cells and no evidence of apoptosis in either (-E2) or (+E2) MCF-7 cultures (data not shown). In contrast, 24 hr and more evidently 48 hr exposure to 100 n M of adriamycin increased the distribution of MCF-7 ceIls at G2/M phase and decreased that at S phase in the cell cycle. Adriamycin did not produce apoptosis of MCF-7 cells (Table 2 vs Table 1 and Fig. 3). Notably, adriamycin (100 nM) increased dso the distribution at Gl/Gû phase in the ce11 cycle but ody of (+E2) MCF-7 cells (Table 2). Suprapharmacological dose (10 CLM) of adriamycin did not produce apoptosis of MCF-7 cells but increased the distribution of MCF-7 cells at the G2/M phase and surprisingly at S phase in the ceII cycle (Table 3 vs Table). Supplementation of MCF-7 cultures with 100 nM of E2 did not influence adnamycin (1O C1M)-cyîostasis (Fig. 1;upper panel). The failure of adnamycin (100 n M and 10 pM) to induce apoptosis of MCF-7 cells was confïmed by the analysis of DNA fragmentation on simple agarose gel using as positive control for adriarnycin-apoptosis the DNA fragmentation of PC-3 human prostate cancer cells (Fig. 4). Consequently, adriarnycincytostasis rather adriarnycin-apoptosis mediated the reduction of the ce11 number a . A/D ratio of MCF-7 cultures (Fig. 1,2). In addition, these data suggested that different molecular pathways possibly mediated pharmacological (100 nM) and suprapharmacological (10 pM) adriamycincytostasis of MCF-7. 2. The effects of M G 6 3 CM, IGF I, TGFB 1 on the growth of MCF-7 ceiis and adriamycin-cytostasis. Increasing doses of MG-63 CM (0.5 up to 100 pg/ml; final protein concentration) inhiited the growth of MCF-7 cells. Fifty (50)&ml of MG63 CM produced maximum inhibition resulting in 25% reduction of the number of the MCF-7 cells grown in monolayer cultures (data not show). In addition, 50pg/mi of MG-63 CM decreased the ratio of both the (-E2) and (+E2) MCF-7 cultures mg. 2). Fifty 50 n&nI of IGF 1 and 25 ng/ml of TGFP 1 increased and decreased the A/D ratio of MCF-7 ceus, respectively [(-E2) MCF-7 cultures; control = 28.9; plus IGF I =30.5; plus TGFBL =22.5] and [(+E2) MCF-7 cultures; control 42.8; plus IGF 1 4 4 . 5 ; plus TGFP 1= 21 -51 (Fig. 2). Moreover, exogenous IGF I increased the distribution of (-E2) MCF-7 cells at the S and G2/M phases in the ceIl cycle , at the expenses of GVGO phase (Table 1). Exogenous TGFPL arrested (+E2) MCF-7 ceils at the Gl/GO phase and decreased the distribution at S and G2M phase in the ce11 cycle (Table 1). These data were in concert with what is known about the role of these growth factors in the biology breast cancer (21-23) and our results assessing the N D ratio of MCF-7 cells (Fig. 2). Therefore, exogenous IGF 1 produced E2-like changes in MCF-7 cells regarding îhe phase distribution in the ce11 cycle and TGFPl reversed the E2-mediated changes in the ce11 cycle of MCF-7 cells. Conceivably, differential expression of IGF I (up regulation) and TGFB1 (down regulation) possibly mediate at least in part ER function in the MCF-7 cells. In addition, 50 p g / d of MG63 CM and 25 ng/ml of TGFP 1 enhanced adriamycin (100 nMJ-cytostasis of both (-E2) and (+E2) MCF-7 cultures wMe 50 n g b l of IGF I partially reversed the adnamycin (100 nM)-cytostasis of (-E2) MCF-7 cultures; [(-E2) MCF-7 cultures: A/D ratio; control = 28.9 ; adriamycin (100 nM)= 18.95 ;adriamycin (100 nMJ plus MG-63 CM = 15.0 ;adnamycin (100 nM) plus TGFB 1 = 13.9 ;adriamycin (100 nM) plus IGF 1 = 22.5 ;adriamycin (100 nM) plus MG-63 CM + IGF I + TGFP 1 = 13-61 and [(+E2) MCF-7 cultures: N D ratio; control = 42.8 ;adriamycin (100 nM) = 22.5 ; adriarnycia (100 nM) plus MG-63 CM = 16.8 ;adriamycin (100 nM) plus TGFPI = 15.8 ; adnamycin (100 nM) plus IGF I = 18.8 ; adnamycin (100 nM) plus MG-63 CM + IGF I + TGFj31 = 13-11. Under identical experimental conditions, MG-63 CM, IGF I and TGFSI partially reversed the supraphamiacologicd dose of adriamycin (10 pMJcytostasis of MCF-7 cultures [(-E2) cultures: A/D ratio; control = 28.9 ; adnamycin (10 pM) = 12.6 ; adriamycin (10 pM) plus MG63 CM = 14.8 ; adn'amycin (10 CrM) plus TGFP 1 = p; adnarnycin (1 0 CLM) plus IGF 1= 17.6 ;adriamycin (10 pMJ plus MG-63 CM + IGF 1 + TGFP 1 = 18-21and [(+E2) cultures: A/D ratio; control = 42.7 ;adriamycin (10 CLM) = 12.6 ; adriarnycin (10 CiM) plus MG963 CM = 14.8 ;adriamycin (10 pM) plus TGFB1 = 17.8; adriamycin (10 pM) plus IGF I = 15.2 ;adriamycin (10 CLM) plus MG-63 CM + IGF 1 + TGFPl = 16.61 (Fig. 2). 3. M G 6 3 osteoblast-like cells enhance adriamycin-cytostasis of MCF-7 c e k in 3-D system. One hundred (100 nM) of E2 had a marginal effect on the growth of MG63 cells in monolayer cultures (Fig. 1; lower panel). Exposure to adriamycin (100 nM) decreased the number of MG63 (Fig. 1; lower panel) and arrested MG-63 cens at G2/M phase in the celI cycle of both the (422) and (+E2) MG43 cultures. In addition, MG-63 ceUs were apparently resistant to 100 nM of adriamycin-apoptosis as assessed by flow cytometry and DNA fiagmentation on simple agarose gel (Table 4 and Figs. 43). Suprapharmocological dose of adriamycin (10 pM) produced apoptosis of MG-63 cells and increased the number of MG-63 ceUs at the S phase in the ce11 cycle as it did in MCF-7 cells (Table 4). E2 supplementation increased both adriamycine (100 nM)-cytostasis and adriarnycin (10 CLM)-apoptosis of MG-63 cells (Table 4). The M G 4 3 and MCF-7 cells were resistant to pharmacological dose (100nM) of adriamycin-apoptosis in 3-D system as documented by the TUNEL assay [Fig. 6 , panel A =MG-63, panel B = MCF-7 cells, and panel C = PC-3 "positive control"]. However, MG-63 and MCF-7 were sensitive to the adriamycin (100 nM)-cytostasis, as documented by a decreasing number of both ce11 type growing in 3-D system, as compared with that of adriamycin-f?ee 3-D gel systern (Fig. 7). Coculture of MG-63 with MCF-7 cells inhibited the growth of both the cell types grown in the 3-D system, suggestive of cell-cd interactions inhi'biting the growth of MCF-7 and mainly MG-63 cefIs as cornpared with those ceus growing in 3-D systems contauiing one single ceU type (Fig. 7). This was in concert with a recent report which documented the existence of MCF-7 breast cancer-derived specinc intiI'bitors of protein nature (MW =700 up to 4,000 D) for osteoblasts, including MG-63 ceus (25). In addition, coculture of MCF-7 with MG-63 cells increased adriamycin-cytostasis of MCF-7 in 3-D system (Fig. 7). DISCUSSION The ability of various neoplasms to metastasize selectively înto specific organs depends on metastatic properties of tumor subclones, stochastic elements that interfere with the metastatic process, and local interactions with the host tissue (4,26, and ref. therein). Because (ER)-positive breast cancer patients with bone only metastases reported to have favorable prognosis and "indolent" course as compared with that of breast cancer patients wiîh liver and lung metastases (10-12), we assessed the ability of human osteoblast-like cells and osteoblast-derived growth factors to influence chemotherapycytotoxkity, in vitro. We documented that pharmacologicd dose of adriamycin (LOO nM) produced an arrest of MCF-7 cells at GVGO phase and G2/M phase in the ce11 cycle. In addition, adriamycin (100 n M and 10 pMJ did not produce apoptosis of MCF-7 cells, as assessed by trypan blue exclusion, flow cytomeûy and analysis of DNA fragmentation on agarose gel. Therefore, adnarnycincytostasis rather adnamycin-apoptosis decreased the number and reduced the A,D ratio of MCF-7 cells (Fig. 1-3). Because the suprapharmacological dose of adnamycin (10 pM) resulted in a peculiar increase in the distribution of the MCF-7 cells at S phase in the ceU cycle, it is conceivable that Werent molecular pathways mediate 100 nM vs 10 p M adnamycin-cytostasis of MCF-7 cells. Under our experimentd conditions, adriamycin (100 nM) did not produce apoptosis of MG-63 osteoblast-like human osteosarcoma cells despite the fact that it effectively blocked MG43 cells at G2/M phase in the ce11 cycle. The latter was more evident in (+E2) MG63 cultures. Suprapharmacological dose of adriamycin (10 pM) produced apoptosis of MG-63 cells supplemented with 100 nM of E2. Suprapharmacologicd dose of adnamycin produced dso a pecuiiar increase in the distriïution of the MG63 cells at the S phase in the cell cycle. Apparently, MG63 ceIIs were relatively resistant to adriamycin (100 nM)apoptosis and various doses of adnamycin (10 mM vs 100 nM) acted via diEerent molecular mechanisms to produce cytostasis and apoptosis depending on the supplementation of MG-63 cells with E2 (Table 4). The molecular mechanism which connected adriamycin (1 0 CLM)-apoptosis with increased distribution at S phase in the cell cycle of (+E2) MG-63 cultures is cmently under investigation in our laboratov. It is known that relative low concentrations (50 up to 500 nM) of adnamycin interferes with DNA unwinding (27), 1 p M of adriamycin inhiiits topoisornerase II expression (28), and supraphamacological concentrations (5 up to 10 CiM) of adriamycin produce non-protein associated DNA-strand breaks, suggestive of free-radical mediated apoptosis (29). It is noteworthy that chronic exposure to relative low concentrations (50-1 00 nM) of adriarnycin that is typically sustained in the peripherai blood for up to 12 hr following i.v. administration of adnamycin in breast cancer patients, it appears to engage a unique growth/ceU arrest death pathway involving damage to nascent DNA, endoreduplication of DNA, and differentiationinduction expressed as an increased phase distribution at GI/GO phase in the ce11 cycle and associated with gradual reduction of expression of the c-myc oncogene in MCF-7 breast cancer cells (30). These data were in concert with adriamycin-cytostasis (1 00 Rhrl) and blockade of (+E2) MCF-7 cultures at the GUGO phase in the ce11 cycle documented in our study. Notably, adnamycin (100 nM)-cytostasis was enhanced by exogenous MG63 CM and TGFBI in both the (-E2) and (+E2) MCF-7 cultures and p d a l l y reversed by exogenous IGF I (Fig. 2). Adriamycin (100 nM) and MG-63 CM apparently had additive effects in arresting MCF-7 cells at Gl/Gû phase in the cell cycle (Table 2). DifXerentiaI expression of IGF I (up regdation) and TGFPl (down regdation) possibly mediate ER fùnction in MCF-7 cells (Table 1). Because exogenous IGF I partially neutralized only the adnamycin-cytostasis of (-E2) MCF-7 cultures, it is conceivable that (+E2) MCF-7 cultures expressing already high levels of endogenous IGF 1 contained MCF-7 cells with desensitized or down regulated type I IGF receptors. In contrast, exogenous TGFB 1 particdarly blocked the (+E2) MCF-7 cells at Gl/GO phase in the ce11 cycle. Notably, TGFP 1 had no effect on (-E2) MCF-7 cells (Table 1). Therefore, it is possible that ER fùnction either decreases the expression of TGFBl and or increases the expression of TGFPl receptor. Because the MG-63 CM produced similar inhibiton of MCF-7 ce11 growth and it is known to contain high levels of TGFPl (15), it is conceivable that TGFP 1 mediates, at least in part, MG-63 CM-cytostasis of MCF-7 cells (Table 2 and Fig. 2). Recently. it has been docurnented that TGFP I inhibition of human breast cancer cells is mediated by IGFBP-3 action (24), which in its tum, reduces IGFs bioavailability (7,8,16). Therefore, it is conceivable b a t Merential expression of TGFB 1/TGFP receptor and type 1 IGF receptodIGF I/IGFBP-3 mediates ER function in breast cancer ceUs, thereby controlling the growth and response to chemotherapy of MCF-7 cens (14,24). These data suggested that favorable survival and an "indolent" course of breast cancer patients with bone only metastases is possibly determined by host tissue @one)-tumor interactions, locally. The importance of the host tissue-tumor ce11 interactions in bone metastases were recently documented in our 3-D system which can assess the development of the osteoblastic reaction around inoculated PC-3 prostate cancer celIs (1 7), development of rnorphological evidence of osteolysis in response to the local growth of MCF-7 and ZR-75 breast cancer cells (18), and the expression of angiogenic potential of PC-3 prostate cancer cells in the presense of stroma1 fibroblasts (3 1). In addition, endogenous interleukin 6 was found also to be a resistance factor for etoposide-mediated cytotoxicity of PC-3 and DU145 prostate cancer cells (32) and IGF I was a survival factor of PC12 cens apoptosis (33). Furthermore, the IGF 1 Uihiibition of the apoptosis of PC12 cells was associated with an ïncreased expression of the bcl-xL gene product suggesting that growth factors, such as IGF I can regulate apoptosis-related genes, thereby modulating apoptosis (33). It is noteworthy that there existed a correlation between apoptosis, tumorogenicity and expression of levels of IGF Vtype 1 IGF receptor. Therefore, exprassion of îhe IGFs/type 1 IGF receptor were implicated in the protection fiom cytotoxic hg-induced apoptosis in vivo and in vitro (34-36). Tt is noteworthy that recent data documented parîïcular checkpoints in the molecular pathways of apoptosis which meet with the growth factor-signal transduction pathways (37,38). These checkpoints implicated serine phosphorylation-elimination of a death agonist Bad gene product as response to surMval factors (39). Because bone matrix is the leading source of TGFPl in humans, excluding platelets, our data suggested that osteoblast-derived "enhancers" of chemotherapy-cytostasis, such as TGFBI cm potentiate the efficacy of adriamycin (100 nM), thereby mediating favorable survival of breast cancer patients with bone only metastases. However, other host tissue growth factors, such as IGF 1 c m reverse adriamycin-cytostasis of ER-positive MCF-7 breast cancer cells, in vitro. Conceivably, fiiture therapeutic targeting of bone-derived "survivd factors", such as IGF I or "enhancers" of chemotherapy-cytostasis, such as TGFP 1 can optimize efficiency and efficacy of hormone and cytotoxic h g chemotherapy in patients with advanced breast cancer as it apparently does in advanced prostate cancer cells (16). ACKNOLEDGEMENTS Michael Koutsiliens is a scholar fkom the "Fondsde la Recherche en Santé du Q U ~ ~ ~ C - ' ~ F F and ~ SCarlos Q " Reyes-Moreno holds a student Award fiom the FRSQ. The authors thank Mr. Maurice Dufour for excellent technical assistance in 80w cytometry and Dr. Charles Doillon for the supply of type 1 collagen gel. We would also thank the directors of the Departrnents of Obstetics-Gynecology and Molecdar Research Center, C m - C H U Q , Drs R. Maheux and F. Labrie, respectively, for continuhg support of this research. REFERENCES 1) BORING, C. C.,SQUIRES, T. S., and TONG, T. Cancer statistics. CA Cancer J. Clin., 43 :7-26, 1993. 2) KOENDERS, P.G., BEEX, L.V.A.M., LANGENS, R., KLOPPENBORG, P.W.C., SMALS, A.G.H., BENRAAD, TL, and the Breast Cancer Study Group. Steroid hormone receptor activity of primary human breast cancer and pattern of fkst metastasis. Breast Cancer Res. and Treat., 18: 27-32, 1991. 3 ) THERIAULT, R.L., HORTOBAGYL, G.N. Bone metastasis in breast cancer. Anti-Cancer Drugs, 3 :455-462, 1992. 4) GALASCO, C. S. B. Mechanisms of lytic and blastic metastatic disease of bone. Clin. Orthopecl Re[. Res.. 12: 20-27, 1982. 5 ) EVANS, C.E., WARD, C., and BRADMAN, 1. P. Breast carcinomas synthesize factors which innuence osteoblast-like cells independently of osteoclast in vitro. J. of Endocrinologv. 128: R5-R8, 1991 6 ) TAUBE, T., ELOMAA, L, BLOMQVTST, C., BENETON, M. N. C., and KANIS, J.A. Histomorphemetric evidence for osteoclast-mediated bone resorption in metastatic breast cancer. Bone, 15,2, 16 1-166, 1994. 7) GR0NDHA.L-HANSEB, J., CHRISTENSEN, J., ROSENQUIST, C., BRUM\JER, N., MOURIDSEN, H. T., DANO, K., BLICHERT-TOFT, M. High level of urobase-type plasmimgen activator and its inhibitor PAL1 in cytosolic extracts of breast carcinomas are associated with poor prognosis. Cancer Res., 53: 2513-2521,1993. 8) KOUTSILIERIS, M., and POLYCHRONAKOS, C.. Proteolytic activity against IGF-binding proteins involved in paracrine interactions prostate adenocarcinorna celIs and osteobIasts. Anticancer Res., 12: 905-910, 1992. 9) KOUTSILIERIS, M., ]FRENETTE, G., LAZURE, C.,LEHOm, J. G., GOVINDAN, M. V., and POLYCHRONAKOS, C. Urokinase-type plasminogen activator: a p a r a c ~ efactor regulating the bioavailability of IGFs in PA-III cell-induced osteoblastic metastases. Anricancer Res., 13 : 48 1-486, 1993. 10) SHERRY, M. M., GRECO, A. F., JOHNSON, D. H., HAINSMORTH, J. D. Metastatic breast cancer confined to the skeletal system. 7?zeAmer. J. of Med., 81: 381-386, 1986. 1 1 ) COLEMAN, R.E., RUBENS, R. D. The clinical course of bone metastases fiom breast cancer. Br. J. Cancer, 5 5 : 6 1 -66, 1987. 12) DEL, 1. J., KAUFMAN, M., GOERNER, R.,COSTA, S. D.,KAUL, S., BASTERT, G. Detection of turnor cells in bone marrow of patients with primary breast cancer: A prognostic factor for distant metatasis. J. of Clin. Oncol., 10: 215344539, 1992. 13) KYPRIANOU, N., ENGLISH, H. F., DAVIDSON, N. E., and ISAACS, J.T. Programmed ce11 death during regression of the MCF-7 hurnan breast cancer foilowing estrogen ablation. Cancer Res., 53 : 162- 166, 1991. 14) TEIXEIRA, C., REED, J. C., P U T T , M. A. C . Estrogen promotes chemotherapeutic dmg resistance by a mechanism uivoiving Bcl-2 protooncogene expression in human breast cancer cells. Cancer Res., 55: 39023907,1995. 15) BOULANGER, J., REYES-MORENO, C., and KOUTSILIERIS, M.. Mediation of the glucocorticoid receptor (GR) funetion by the activation of latent transforming growth factor beta 1 in MG-63 osteoblasts-like osteosarcorna cells. Int. J. Cancer, 62: 692-697, 1995. KOUTSILIERIS, M., REYES-MORENO, C., SOURLq A., DIMITRIADOU, V.,and CHOKI, 1.. Growth factors mediate glucvocorticoid receptor b c t i o n and dexamethasone-induced regression of osteoblastic lesions in hormone rebctory prostate cancer. Anticuncer Res., 17: 14611465, 1997. 16) 17) KOUTSILZERIS, M.,SOURLq A., PELLETIER, G., and DOILLON, C... Threedimensional type 1 collagen gel system for the study of osteoblastic metastases produced by metastastic prostate cancer. J. Bone Miner. Res. 9: 1823-1832, 1994. . 18) SOURLA A., DOILLON, C., and KOUTSILIERIS, M.. Threedimensional type I collagen gel system containing MG63 osteoblasts-like celIs as a mode1 for studying local bone reaction caused by metastatic cancer cells. Anricancer Res., 16: 2773-2780, 1996. 19) BORNER, M.M., MYERS, C.E., SANTOR, O.,SEI, Y., TOKO, T., TREPEL, J.B., and SCHNEIDER, E. hg-ùiduced apoptosis is not necessarily depend on macromolecola. synthesis or proMeration in the p53 negaiive human prostate cancer cell line PC-3. Cancer Res., 55: 2 122-2 128, 1995. 20) POLLACK, A., and CIANCO, G. Cell cycle phase-specific analysis of ceU viability using Hoechst 33342 and propidium iodide after ethanol preservation. In: Flow cytometry, 2. Darzynkiewicz and H. A. Crissman editors. Academic Press, San Diego. 19-24, 1991 . 2 1) CLEMMONS, D. R.,CAMACHO-HOBNER, C., CORONADO, E., and OSBORNE, K. Insulin-like growth factor binding protein secretion by breast carcinoma ceIl lines: Correlation with estrogen recepteur statu. Endoct?nology, 127,6,2679-2686, 1990. 22) REDDY, K. B., MANGOLD, G. L, TANDON, A. K., YONEDA, T., MUNDY, G. R., ZILBERSTEIN, A., and OSBORNE, C. K. Inhibition of breast cancer ce11 growth in vitro by a tyrosine kinase inhtibitor. Cancer Res., 52: 3636-3641, 1992. 23) BASERGA, R. The insulin-like growth factor I receptor: Akey to tumor growîh? Cancer Res., 55: 249-252, 1995. 24) OH, Y.,MULLER, H. L., NG, L., and ROSENFELD, R. Transfonning growth factor-b-induced celI growth inhibition in human breast cancer cells is mediated through insulin-like growth factor-binding protein-3 action. me Journal of bzological chemistry, 270,23, 13589-13592, 1995. 25) SIWECK, B., LACROIX, M., dePOLLACK, C., MARIE, P., and BODY, J-J. Secretoq products of breast cancer c e k specificdy affect human ostoblastic cells: partial purification of active factors. J. Bone Miner. 26) KOUTSILIERIS, M. 1995. Skeletal metastasis in advanced prostate cancer: cell biology and therapy . Crit. Rev. Oncol. Hernatol., 18: 5 1-64, 1994. 27) FORNARI, F. A., RANDOLPH, J. K., YALOWICH, J. C., RITKE, M. K., and GEWIRTZ, D. A. Interference with DNA unwinding by doxombicin in MCF-7 breast tumor celis. Mol. Phannacol., 46: 649-656, 1994. 28) GOLDENBERG, G. J., WANG, H., and BLAIR, G. W. Resistance to adriamycin: relationship of cytotoxicity to dmg uptake and DNA singled- and double-strand breakage in cloned ce11 lines of adriarnycin-sensitive and resistant P388 leukemia. Cancer Res., 46: 2978-2983, 1986. 29) DOROSHOW, J. H.. Revention of doxorubicin-induced killing of MCF7 human breast cancer cells by oxygen radical scavengers and iron chelating agents. Biochern. Biophys. Res. Commun., 135: 330-335, 1986. 30) FORNARI, jr, F. A., JARWS, W. D., GRANT, S., ORR, M. S.., RANDOLPH, J. K.,WHITEJ. K. H., NMMAW, V. R., LOVINGS, E. T., F R E E W , R. H., and GEWRTZ, D. A. Induction of differentiation and growth arrest associated with nascent (nonoligosomal) DNA hgmeutation and reduced c-myc expression in MCF-7 human breast himor ceUs d e r continuous exposure to a sublethal concentration of doxombich Ce22 Growrh & D@ier., 5: 723-733, 1994. 31) JANVIER, R., SOLJRLA, A., KOUTSILSRIS, M., and DOILLON, C . Stroma1 fibroblasts are required for PC-3 human prostate cancer cells to produce capillary-like formation of endothelid celIs in a threeaùnensionai CO-culturesystem. Anricancer Res., 1 7: 1 551 - 1558, 1997. 32) BORSELLINO, N., BELLDEGRUN, A., and BONAVIDA, B. Endogenous interleukin 6 is a resistance factor for cisdiamminedichloroplatinum and etoposide-mediated cytotoxicity of human prostate carcinoma cell h e s . Cancer Res.,55: 46334639, 1995. Insulin-like growth factor4 33) PARRIZAS, M., and LEROITH, D. inhibition of apoptosis is associated with increased expression of the bcl-xL gene product. EndocrznoIogy, 138: 1355-1358, 1997. 34) RESNICOFF, M., BURGAUD, J-L., ROTMAN, H. L., ABRAHAM:, D., and BASERGA, R. Correlation betwem apoptosis, tumorïgenesis, and bels of Insulin-Iike growth factor 1receptor. Cancer Res., 55: 3739-374 1, 1995. 35) SELL, C., and BASERGA, R., Rubin R. Insulin-Iike growth factor I (IGF-1) and the IGF-1 receptor prevent etoposide-induced apoptosis. Cancer Res., 55: 302-306, 1995. 36) RESNICOFF, M., ABRAHAM, D., YUTANAUrIBOONCHAI, W., ROTMAN, H. L., KAJSTURq J., RUBIN, R., ZOLTICK, P., and BASERGA R. The Insulin-like growth factor I receptor protects tumor cells f?om apoptosis in vivo. Cancer Res., 55: 2463-2469, 1995. 37) OLTVAI, Z., N.,and KORSMEYER, S. J. Checkpoints of dueling m e r s foi1 death wishes. Cell79: 189-192, 1996. 38) GAJEWSKI, T., F., and. THOMPSON, C . B. Apoptosis meets signal transduction: elimination of a BAD influence. Cell86: 589-592, 1996. 39) ZHA, J., W A , H., YANG, E., JOCKEL, J., and S. KORSMEYER, J. Serine phosphorylation of death agonist Bad in response to survival factor results in binding 10 14-3-3 not Bcl-xL. Ce22 87: 6 19-628, 1996. LEGENDS TO THE FIGURES . Figure 1: The effects of adnamycin (100 n M and 10 pMJ on the number of MCF-7 cells (upper panel) and MG-63 ceUs (lower panel) in monolayer cultures supplemented with (+E2; ) and without (-E2; 0) 100 nM of 17B-estradio1 (E2). The MCF-7 and MG63 cells were cdtured using phenol red-fiee DMEME- 12 media supplemented with 5% calf semm (CS) decoated charcoal treated @CC-CS) and exposed to adriamycin for 48 hr, as described in the Methods section. Control (adriamycin-fiee) cultures supplemented with 5% CS contained higher nurnber of MCF-7 cells in (+E2) cultures as cornpared with that of (-E2) cultures. Adriamycin exposure significantly decreased the number of MCF-7 (upper panel) and MG-63 cells (lower panel) in a dose-dependent marner. . Figure 2: The effects of 50 pdml of MG-63 conditioned media (MG63 CM), 50 n g h l of insulin-like growth factor 1 (IGF I), 25 ng/ml of transformuig growth factor beta 1 (TGFP 1), and adnamycin (100 nM; and 10 pM; ) on the dive (A) versus (vs) dead (D) ratio (ND ratio) of MCF-7 cells grown in (-E2) [upper panel] and (+E2) power panel] culture conditions. The MCF-7 cells were cultured using phenol red-free DMEM/F12 media supplemented with 5% DCC-CS for 48 hr (details in the Methods section). Adnamycin decreased the A D ratio in (-E2) and (+E2) MCF-7 cultures. The MG-63 CM, TGFP 1 enhancedwhile IGF I partially reversed phannacological adriamycin (1 00 nM)-cytostasis of MCF-7 cells. IGF 1, TGFP 1 and MG-63 CM partially reversed suprapharmacological adriamycin (10 pM)-cytostasis, of (-E2) and (+E2) MCF-7 cultures. Figure 3: An example of the changes produced by 100 n M and 10 p M of adriamycin in the phase disniution of MCF-7 cells in the cell cycle as assessed by flow cytometry (details in the Methods section). The 48 hr exposure to 100 n M of adrïamycin arrested MCF-7 cells at G2M phase in the cell cycle without producing apoptosis in either (-E2) and (+E2) cultures. Notably, lOOnM of adriamycin increased the distribution of ceIls at GVGO phase in the cell cycle of ody the (+E2) MCF-7 celIs. The 48hr exposure to 10pM of adnamycin arrested MCF-7 cells at G2/M phase and surprisingly increased the distribution of MCF-7 ceIls at the S phase in the ce11 cycle without produchg apoptosis of both the (-E2) and (+E2) MCF-7 cultures. Figure 4: Adnamycin-apoptosis as assessed by the analysis of DNA fragmentation simple agarose gel. The PC-3, MG-63 and MCF-7 ceUs were maîntained in phenol red-fiee DMEM/F-12 media supplemented with 5% DCC-CS and exposed to 100 nM of adriamycin for 48 hr; then DNA was extracted and analyzed as described in the Methods section of this manuscript. The presence of -180 bp DNA ladders @NA fragmentation) marks the apoptotic deaîh, in vitro. Notably, only the PC-3 extracts presented with evidence of DNA fiagmentation associated with adriamycin (100 nM) exposure. Apparently, MG-63 and MCF-7 cells were relatively resistant to adriamycin (1O0 nM)-apoptosis, in vitro. Figure 5: An exarnple of the changes produced by 100 nM and 10 p M of adnamycin at the phase distribution in the cell cycle of MG63 cells as documented by £Iow cytometry (details in the Methods section). The 48 hr exposure to adnamycin arrested MG-63 cells at G2/M phase in the ce11 cycle without producing adnamycin-apoptosis. The blockade at G2/M phase was more evident in (+E2) MG-63 cultures. Adriamycin (10 CLM) increased the distribution at S phase in the cell cycle and produced apoptosis MG-63 cells Figure 6: An example of the adriamycin-apoptosis in PC-3, MCF-7 and MG63 cells grown in type 1 collagen gel system as documented by TUNEL assay (for details see the Methods section). MG-63 (panel A) and MCF-7 cells (panel B), PC-3 (panel C; positive control) grown in 3-D system were exposed to 100 nM of adrïamycin for 48 hr. Only the PC-3 cells underwent detectable apoptosis. Panel D is the negative control of TUNNEL assay. Figure 7: An example of the adnamycin-cytostasis of the MG-63 (panel A l =adriamycin-fiee vs panel A2 = 100 n M adriamycin) and MCF-7 ceUs [panel Bl=adriamycin-kee vs panel B2= 100 n M adriamycin) in 3-dimensional type 1 collagen system (details in the Material and Method section). Note that the number of MG-63 and MCF-7 cells in 3-D systems which were exposed to 100 n M of adnamycin for 48 hr was remarkably lower than that of adrïamycin-fiee cultures (MG-63 cells= 50% reduction and MCF-7 ceus= 60% reduction. Coculture of MG43 and MCF-7 cells in the 3-D system resulted in a decreasing number of both ceIl types (panel Cl; MCF-7 ceus= 50% reduction; MG-63 cells= 90% reduction), as compared with that of 3-D systerns containing only one ceU type under adriamycin-fiee conditions (panel CI vs panel Al and BI). Notably, the coculture-mediated reduction of the number of MG-63 cells was more significant than that of the MCF-7 cells (50%). It is noteworthy that 3-D coculture systems contained an identical total number of cells per ml of collagen with that of 3-D systems containing only MG-63 (panel A) and MCF-7 cells (panel B), thereby suggesting that coculture resulted in a remarkable inhibition of the growth rate in both the ce11 types. In addition, coculture-mediated cytostasis of MG-63 and MCF-7 cells was potentiated by exposure to 100 nM of adriamycin (panel C2= MG63/MCF-7 cells exposed to 100 n M of adriamycin vs panel Cl= coculture in adriamycin-£ieeconditions). Ratio of alive vs Dead MCF-7 Cells (AlW 0 h 0 ) O P t 0 0 0 n 0 0 Control Control CM (50uglml CM (SOug/ml IGF 1 (SOnglml TGFb 1 (25ngiml) IGF 1 (SOnghl TGFb 1 (25nghnl) A+CM A+IGF I A+TGFb 1 ADRIAMYCIN (1OUM) AtCM A+IGF I A+TGFb 1 ADRIAMYCIN (10uM) 0 0 0 FIGURE 3 1023 O Control FIGURE 4 MG43 ce1Is MCF-7 cells MCF-7 ceHs (k.107W (-Q PC-3 cells Control ADR (100nM) ADR (10uM) FIGURE 6 IRE TABLE 1 TABLE 1: Apoptosis ( 4 1 ; % of Total Ce11 Nurnber) and Phase Distribution (%) of MCF-7 Cells into the Cell Cycle (X+SD) CONTROtS ( 4 2 1 4 1 22t-9 : GIIGO :82M.7 S 12M. (-EZ) plus IGF 1 (5ûnglml) G2/M SSrO.7 CONTROIS (42) 4 1 1-2 : GllGO : 6ï5*1 S 26.îk1.4 cG1 : GtIGO m . 4 : 64SSl.7 S 28.0128 û2iM 9.W.7 (42) plusTGF bl(2Snqlml) cG1 2.495 (+E2) plus IGF 1 (50ng/mI) G2lM 6.5d.7 <G1 : GIlGO 1.8i02 : 66.59.1 S 253-21 GZM 8.0f0.1 : G1GO : t32ûi9.8 S GZmR 1 2 . ~ ~ 8 6.M.1 pIu, TGF bl(25nqfml) cG1 2.79.5 : GTlGO : 78.010.1 S G a 16W.7 5.5û.7 MCF-7 cells were cultured in phenol red-free DMEJWF-12 supplemented with 5-0% C-DCC-treated for CS 48hr; E2=107M. TABLE 2 TABLE 2: Apoptosis &G7; % of Total Cell Nvmber) and Phase Distribution (76) of MCF-7 Cells into the Ce!] Cycle (SD) (42)PIUS MG63 CM (+€2) plu8 MG43 CM MCF-7 cel1s were cultured in phenoi red-free DMEiWF-12 supplemented with 5.0Y0 C-DCC-treated for CS 48 hr; E2=lD7M TABLE 3 TABLE 3: Apoptosis (<Gy; % of Total Cell Number) and Phase Distribuion (%) of MCF-7 Cells into the Cell Cycle (XfSD) MCF-7 cells were cultured in phenol red-free DMEWF-12 supplemented with 5.0% C-DCC-treated for CS 48hr; E2=IO-'M TABLE 4 TABLE 4: Apoptasis (eG1; % of Total Cell Nvmber) and Phase Distribution (%) of MG43 C e h into the Ce11 Cycle (X+SD) MG43 cslls were cultured in phenol tcd-tfee DMEM/F-12 suppkmented with 5.0% C-DCC-treattd for CS 40hr; E2=1û-'M Dans notre étude, nous avons montre que l'oestradiol stimulait la prolifération des cellules MCF-7. Nous avons aussi démontré que I'ADR (100nM) cfiminuait la croissance des deux lignées cellulaires, in vitro. Cet agent thérapeutique entraine un bIocage des cellules MCF-7 dans les phases G1/GO en présence d'oestradiol et G2/M du cycle cellulaire et ne déclenche pas I'apoptose, tel que démontré respectivement par la cytométrie en flux, l'analyse de L'ADN sur gel d'agame et par l'essai dit de TUNEL, après la coculture des MCF-7 avec les ostéoblastes dans le système 3-D. Nous avons aussi observé que le MG-63 CM potentialise l'effet de l'adriamycine au niveau de la phase GUGO et antagonise le blocage exercé par l'adriamycine au niveau de la phase G2/M du cycle cellulaire en présence ou en absence d'oestradiol. Notre objectif initial était de déterminer l'effet de I'ADR sur les cellules MCF7 et de mieux comprendre le rôle de l'environnement osseux dans les effets de l'adriamycine sur les cellules MCF-7. A la lumère de nos résultats, nous pouvons avancer que l'ADR (1 00n.M) provoque un effet cytostatique plutôt qu'un effet cytotoxique sur Les cellules MCF-7 du cancer du sein et augmente possiblement l'état de Merenciation de cette lignée cellulaire en augmentant le nombre des cellules en phase Gl/GO. De plus, les facteurs de croissance, tel le TGFP 1, dérivés des ostéoblastes peuvent modifier les effets de I'ADR sur les cellules MCF-7, in vitro. A la lumière de ces résultats, il est concevable que les interactions cellulecellule, dans les sites de métastases du cancer du sein, puissent être responsables de la biologie tumorale altérée dans les métastases osseuses. BIBLIOGRAPHIE 1) De Maublanc, M.A. Cytopathologie des tumeurs malignes du sein: valeur diagnostique et pronostique. Editions Techniques. Encycl. Méd. Chir. (paris-France).Gynécologie, 865 E, 199 1,4 p. 2) Marty, M., Extra, J-M., Espié M., and Calvo F. Biologie du cancer du sein. Editions Techniques. Encycl. Méd. Chip. (Paris-France). Gynécologie, 8654-20, 1994,6p. 3) Katzenellenbogen, B.S. Editorial: A new actor in the estrogen receptor Drama-Enter er-B. fie endocrine sociev 138,3,86 1-862, 1997 . 4. Kuiper, G.G.J., Carlsson, B., Grandien, K., Enmark, E., Haggblad, J., Nilsson, S., and Gustafsson, .LA. Comparaison of the ligand binding specificity and transcript tissue distri'bution of the estrogen receptor a and P. n e endocrine society 138,3,863-870, 1997 5) Koenders, P.G., Beex, L.V.A.M., Langens, R., Kloppenborg, P.W.C., Smals, A.G.H., Benraad, Th.J., and the Breast Cancer Study Group. Steroid hormone receptor activity of primary human breast cancer and pattern of e s t metastasis. Breast Cancer Research and Treatement: 1 8,27-32, 1991. 6 ) Brémond, A. Traitement du cancer du sein non métastatique: formes habituelles. EncycI. Méd Chzr. (Elsevier, Paris) Gynécologie, 870-A- 10, 1997,6 p. 7) Theriault, R.L., Hortobagyl, G.N. Bone metastasis in breast cancer. AntzCancer Drugs: 3,455-462, 1992. 8) Sherry, M.M., Greco, A.F., Johnson, D.H., Hainsworth, J.D. Breast cancer confined to the skeletal system. 7he A M 8 1,38 1-386, 1985. 9) Coleman, R.E. & Rubens. R.D. The clinical course of bone metastases from breast cancer. Breast J. Cancer: 5 5 , 6 1-66,1987. 10) Bemiti, A., OseUa, G., Raucci, C.A., Roncari, A., and Dogliotti, L. Transient increase in total serum alkaline phosphatase predicts radiological response to systemic therapy in breast cancer patients with osteolytic and mixed bone rnetastases.Ocology 50,2 18-221, 1993 . 1 1) Taube, T., Elomaa, I., Blomqvist, C., Beneton, M.N.C., and Kanis, J.A. Histomorphometric evidence for osteoclast-mediated bone resorption in metastatic breast cancer. Bone 15, 2, 161-166, 1994 . 12) Hartwell, L.H., and Kastan, M.B. Ce11 cycle control and cancer. Science 266, 182191828, 1994. 13) Solary, E., Bertrand, R., and Pommier, Y. Le rôle de I'apoptose dans la genèse et le traitement du cancer .Medeczne~science9,667675,1993 . 14) Piirrhs, M., and Leroith, D. Insulin-like growth factor4 inhibition of apoptosis is associated with increased expression of the bcl-xL gene product. Endocrznologv, 138: 1355-1358, 1997. 15) Oberhammer, F., Wilson, J. W., Dive, C., Moms, I.D., Hichan, .LA-, Walkeluig, A.E., Waker, FR.,and Sirkoska, M. Apoptotic death in epithelial cells: claevage of DEA to 300 andor 50kb fragments pnor to or in the absence of intemucleosomal kagmentation. The EMBO Journal 12,9, 36793684, 1993. 16) Mccarthy, M. and Bore, J. Treatment of Breast Cancer in two Teachïng Hospitals: a Cornparison with Consensus Guidelines. Eur. J. Cancer: 27, 5, 579-582, 1991. 17) Guastalla, JP., Catimel, G, Blay, JY,Heltie, S, Rebattu, P, Brémond, A, Merrouche, Y et Barbet N. Traitement du cancer du sein métastatique et des fonnes cliniques particulières. Encycl. Méd Chir. (Elsevier. Pans) Gynécologie, 871-A4 O, 1997, 14 p. 18) Doroshow, J.H. Prevention of doxombicin-induced of MCF-7 human breast cancer ceus by oxigen radical scavengers and iron chelatings agents. Biochem ical and Biophysical Research Communications: 1 35, 1, 330-3 35, 1986. 19) Cumming, J. The Molecular Pharmacology of Doxorubicin in vivo. Eur. J. Cancer: 27,5, 532-535,1991. 20) Fornari jr, F.A., Jarvis, W.D., Grant, S., Orr, M.S., Randolph, J.K., White, F.K.H., Murnaw, V.R., Lovings, E.T., Freernan, R.H., and Gewirtz, D.A. Induction of differentiation and growth arrest associated wih nascent (nonoligasomal) h a fkagmentation and reduced c-myc expression in MCF-7 human breast tumor cells d e r continuous exposure to a sublethal concentration of doxombicin. Cell growth & Drffer. 5: 723-733, 1994. 21) Fomari Jr, F.A., Jarvis, W.D.,Grant, S., On; M.S., Randofph, J.K., White, F.K.H., and Ge*. D.A. Growth arrest and non-apoptotic ceH death associated with the suppression of c-myc expression in MCF-7 breast tumor celk following acute to doxombicin. Biochemzcal phamacology 5 1, 93 1-940, 1996. TEST T A R G ~( ~ ~ 1 3 ) - APPLfEDA IMAGE. lnc -----* 1653 East Main Street Rochester, NY 14609 USA Phone: 71W482-0300 F a 7161'288-5989 O 1993. ApOlled Image. lm. Ali Rightl, Resemâ
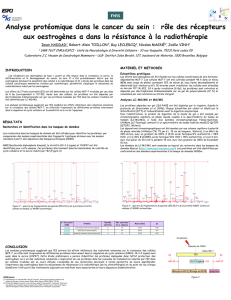



![Poster CIMNA journée CHOISIR [PPT - 8 Mo ]](http://s1.studylibfr.com/store/data/003496163_1-211ccc570e9e2c72f5d6b6c5d46b9530-300x300.png)






